国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:_______ 。
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_______ 。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_______ 。
(4)化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。
①在如下图所示步骤中,发生氧化反应的是_______ (填序号,下同),发生还原反应的是_______ ,既没发生氧化反应又没发生还原反应的是_______ 。(提示:铬元素的化合价有+6、+3)_______ 。
_______K2Cr2O7+_______HCl=_______Cl2↑+_______KCl+_______CrCl3+_______
(5)已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
①请用双线桥法标出电子转移的方向和数目_______ 。
②上述反应中氧化产物和还原产物的质量比为_______ 。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
(4)化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。
①在如下图所示步骤中,发生氧化反应的是
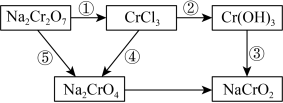
_______K2Cr2O7+_______HCl=_______Cl2↑+_______KCl+_______CrCl3+_______
(5)已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
①请用双线桥法标出电子转移的方向和数目
②上述反应中氧化产物和还原产物的质量比为
更新时间:2024-04-24 11:10:49
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有以下物质:①Cu ②熔融NaCl ③醋酸 ④NaHSO4固体 ⑤NH3 ⑥蔗糖 ⑦KHCO3溶液 ⑧CaO ⑨Ca(OH)2 ⑩盐酸,请按下列分类标准回答问题(用序号填写)。
(1)能导电的是_______________ ;
(2)属于电解质的是________________ ,属于非电解质的是________________ ;
(3)写出NaHSO4在水溶液中的电离方程式____________ ;
(4)向KHCO3溶液中滴加Ba(OH)2溶液至过量的离子方程式为_______________________ 。
(1)能导电的是
(2)属于电解质的是
(3)写出NaHSO4在水溶液中的电离方程式
(4)向KHCO3溶液中滴加Ba(OH)2溶液至过量的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】在常温常压下,有以下9种物质,请回答下列问题:
①干冰 ②氯化钠 ③蔗糖 ④稀硫酸 ⑤ 溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧氯化氢 ⑨
溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧氯化氢 ⑨
(1)其中能导电的是___________ (填写序号,下同);属于电解质的是___________ ;
(2)写出物质⑤在水中的电离方程式:___________ 。
(3)写出物质⑤和⑥在水中发生反应的离子方程式:___________ 。
①干冰 ②氯化钠 ③蔗糖 ④稀硫酸 ⑤
 溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧氯化氢 ⑨
溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧氯化氢 ⑨
(1)其中能导电的是
(2)写出物质⑤在水中的电离方程式:
(3)写出物质⑤和⑥在水中发生反应的离子方程式:
您最近半年使用:0次
【推荐3】(一)现有下列6种物质:①盐酸;②硫酸钠;③二氧化碳;④蔗糖;⑤熔融NaOH;⑥食盐水
(1)上述物质中属于电解质的是__________ (填序号,下同),属于非电解质的是__________ ,
(2)写出②在水中的电离方程式__________ ,请设计实验检验溶液②中的阴离子__________ 。
(二)自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。
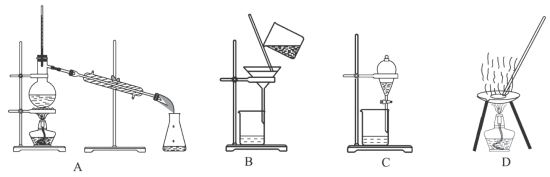
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置,将A、B、C、D序号填入适当的空格中。
(3)碳酸钙悬浊液中分离出碳酸钙__________ ;
(4)分离酒精和水__________ ;
(5)分离植物油和水__________ ;
(6)氯化钠溶液中分离出氯化钠__________ ;
(7)氯化钠溶液中分离出水__________ 。
(1)上述物质中属于电解质的是
(2)写出②在水中的电离方程式
(二)自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。

请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置,将A、B、C、D序号填入适当的空格中。
(3)碳酸钙悬浊液中分离出碳酸钙
(4)分离酒精和水
(5)分离植物油和水
(6)氯化钠溶液中分离出氯化钠
(7)氯化钠溶液中分离出水
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ 中。
(2)除去碳酸钠固体中碳酸氢钠的方法是______________ 。
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”)。
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______________ 。
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于__________ (填“碱性”或“两性”)氧化物。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)除去碳酸钠固体中碳酸氢钠的方法是
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求写出对应方程式:
(1)NaHCO3的电离方程式____
(2)向FeI2溶液中通少量Cl2的离子方程式____
(3)向NaHCO3溶液中逐滴加Ba(OH)2溶液至恰好沉淀完全的离子方程式:___
(1)NaHCO3的电离方程式
(2)向FeI2溶液中通少量Cl2的离子方程式
(3)向NaHCO3溶液中逐滴加Ba(OH)2溶液至恰好沉淀完全的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮元素的常见化合价及其化合价对应的常见物质的化学式如下表,试回答下列问题:
(1)从化合价上看,N2O5具有_______ (填“氧化”或“还原”)性。
(2)下列试剂不能用于干燥NH3的是_______(填标号)。
(3)NO与NO2中氮元素的价态均处于中间价态,则NO与NO2均既有氧化性又有还原性。
①NO极易与氧气反应,NO表现_______ 性;在一定条件下NO与氨气发生归中反应生成N2,其化学方程式为_______ 。
②NO2可与H2O发生自身歧化反应,反应中氧化剂和还原剂的物质的量之比为_______ ;NO2与NaOH溶液反应可生成两种盐,其中一种是NaNO2,写出NO2与NaOH溶液反应的化学方程式:_______ 。
③汽车排气管上装有催化转化器,可减少尾气对环境的污染,将汽车尾气中的有害气体CO和NO转化为无害气体排放,写出相关反应的化学方程式:_______ 。
④工业生产中利用氨水吸收SO2和NO2,原理如图所示:
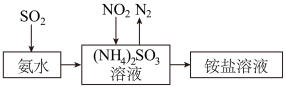
写出NO2被吸收过程中的离子方程式:_______ 。
| 化合价 | -3 | +1 | +2 | +3 | +4 | +5 |
| 化学式 | NH3 | N2O | NO | N2O3 | NO2 | N2O5 |
(1)从化合价上看,N2O5具有
(2)下列试剂不能用于干燥NH3的是_______(填标号)。
| A.浓硫酸 | B.碱石灰 | C.NaOH固体 | D.CaCl2固体 |
①NO极易与氧气反应,NO表现
②NO2可与H2O发生自身歧化反应,反应中氧化剂和还原剂的物质的量之比为
③汽车排气管上装有催化转化器,可减少尾气对环境的污染,将汽车尾气中的有害气体CO和NO转化为无害气体排放,写出相关反应的化学方程式:
④工业生产中利用氨水吸收SO2和NO2,原理如图所示:

写出NO2被吸收过程中的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】实验现象如图:
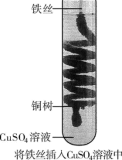
问题:为什么会发生上述现象______ ?该反应中Fe起到的作用是_______ ?说明Fe、Cu的还原性强弱有何关系__________ ?

问题:为什么会发生上述现象
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】金属及其化合物在许多领域有着广泛的应用。
(1)Na2CO3和NaHCO3都是厨房常用物质,与澄清石灰水反应均能产生白色沉淀,请写出往足量NaHCO3溶液中滴加少量石灰水发生反应的离子方程式:___ 。
(2)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。反应中氧化剂是___ (填化学式)。
(3)绿矾(FeSO4·7H2O)是一种良好的絮凝剂。将绿矾溶于水后,加入适量NaOH浴液可观察到的现象为___ ;若将少量Na2O2固体加入FeSO4溶液中,发生的反应为4Na2O2+4Fe2++6H2O=4Fe(OH)3↓+8Na++O2↑,反应中被氧化的元素为___ (填元素符号)。
(4)“钢是虎,钒是翼,钢含钒犹如虎添翼",钒是“现代工业味精”。V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO ),溶于强酸生成含钒氧离子(VO
),溶于强酸生成含钒氧离子(VO )的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:___ 、___ 。
(1)Na2CO3和NaHCO3都是厨房常用物质,与澄清石灰水反应均能产生白色沉淀,请写出往足量NaHCO3溶液中滴加少量石灰水发生反应的离子方程式:
(2)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。反应中氧化剂是
(3)绿矾(FeSO4·7H2O)是一种良好的絮凝剂。将绿矾溶于水后,加入适量NaOH浴液可观察到的现象为
(4)“钢是虎,钒是翼,钢含钒犹如虎添翼",钒是“现代工业味精”。V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO
 ),溶于强酸生成含钒氧离子(VO
),溶于强酸生成含钒氧离子(VO )的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】用化学用语表达。
(1)小苏打受热易分解,化学方程式为_______ 。
(2)氯化铁溶液可用于刻蚀铜制的印刷电路板,反应的离子方程式为_______ 。
(3)工业上用氯气和熟石灰制备漂白粉,化学方程式为_______ 。
(4)过氧化钠和二氧化碳反应的化学方程式_______ ;过氧化钠和水反应的化学方程式 _______
(5)沾有水的铁制器皿在高温火焰上会发黑,发生反应的化学方程式是_______ 。
(1)小苏打受热易分解,化学方程式为
(2)氯化铁溶液可用于刻蚀铜制的印刷电路板,反应的离子方程式为
(3)工业上用氯气和熟石灰制备漂白粉,化学方程式为
(4)过氧化钠和二氧化碳反应的化学方程式
(5)沾有水的铁制器皿在高温火焰上会发黑,发生反应的化学方程式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】写出下列有关反应的离子方程式
(1)碳酸氢钠与偏铝酸钠溶液混合_______ 。
(2)向Ba(OH)2溶液中滴加NaHSO4溶液至Ba2+沉淀完成_______ ,继续滴加NaHSO4溶液_______ 。
(3)足量氯气通入溴化亚铁溶液中_______ 。
(4)磁性氧化铁溶于氢碘酸中_______ 。
(5)过氧化钠与水反应_______ 。
(6)金属钠与硫酸铜溶液反应_______ 。
(1)碳酸氢钠与偏铝酸钠溶液混合
(2)向Ba(OH)2溶液中滴加NaHSO4溶液至Ba2+沉淀完成
(3)足量氯气通入溴化亚铁溶液中
(4)磁性氧化铁溶于氢碘酸中
(5)过氧化钠与水反应
(6)金属钠与硫酸铜溶液反应
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】过氧化钠是一种淡黄色固体,它能与二氧化碳反应,在潜水艇中用作制氧剂,供人类呼吸之用。某学生为了验证这一实验,以足量 的大理石、足量 的盐酸和一定量过氧化钠样品为原料,制取O2,设计出如下实验装置:
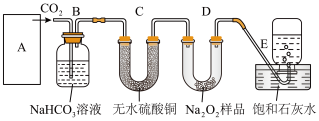
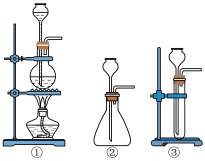
(1)A是制取CO2 的装置,应从下列图①、②、③中最好选哪个图:_______ ;
(2)B装置的作用是吸收A装置中产生的盐酸酸雾,C装置的作用是_______ ;C装置内可能出现什么现象?_______ ;
(3)在取出集气瓶后,如何检验E中收集到的气体_______ 。


(1)A是制取CO2 的装置,应从下列图①、②、③中最好选哪个图:
(2)B装置的作用是吸收A装置中产生的盐酸酸雾,C装置的作用是
(3)在取出集气瓶后,如何检验E中收集到的气体
您最近半年使用:0次



