二氧化氯在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯化物。制备ClO2的方法是:
_____NaClO3+_______HCl=______ClO2↑+______Cl2↑+______NaCl+_______H2O
(1)试配平上述化学方程式,并用标出电子转移的方向和数目___________ 。
(2)该反应中HCl体现的性质是___________。
(3)在标准状况下,每生成10.08L气体,转移的电子数为___________ 。
(4)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒无害的两种气体,自身被还原为Cl-。处理含CN-相同时的电镀废水,所需Cl2的物质的量是ClO2的___________ 倍。
_____NaClO3+_______HCl=______ClO2↑+______Cl2↑+______NaCl+_______H2O
(1)试配平上述化学方程式,并用标出电子转移的方向和数目
(2)该反应中HCl体现的性质是___________。
| A.氧化性 | B.还原性 | C.酸性 | D.挥发性 |
(4)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒无害的两种气体,自身被还原为Cl-。处理含CN-相同时的电镀废水,所需Cl2的物质的量是ClO2的
更新时间:2024-01-02 20:46:42
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将24.8g铜铁合金与足量稀硝酸完全反应,放出6. 72LNO气体(标况下),请计算:
(1)转移电子数为_______ 。
(2)向反应后的溶液中加入NaOH溶液至完全沉淀,得到沉淀的质量为_______ 。
(1)转移电子数为
(2)向反应后的溶液中加入NaOH溶液至完全沉淀,得到沉淀的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请按要求回答下列问题:
(1)氯气和水反应的化学方程式:___________ 。
(2)长期置于空气中的钠,最后形成的物质与氢氧化钡溶液混合后,发生反应的离子方程式为:___________ 。
(3)现有8种物质:①熔融 ②氯气③
②氯气③ ④葡萄糖⑤
④葡萄糖⑤ ⑥稀硫酸⑦
⑥稀硫酸⑦ ⑧
⑧ 。属于电解质的是
。属于电解质的是___________ ,能导电是___________ 。
(4)高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
)是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
①该反应的还原剂是___________ ;
②若生成1
 ,则反应转移的电子数为
,则反应转移的电子数为___________  。
。
(1)氯气和水反应的化学方程式:
(2)长期置于空气中的钠,最后形成的物质与氢氧化钡溶液混合后,发生反应的离子方程式为:
(3)现有8种物质:①熔融
 ②氯气③
②氯气③ ④葡萄糖⑤
④葡萄糖⑤ ⑥稀硫酸⑦
⑥稀硫酸⑦ ⑧
⑧ 。属于电解质的是
。属于电解质的是(4)高铁酸钠(
 )是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
)是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
①该反应的还原剂是
②若生成1

 ,则反应转移的电子数为
,则反应转移的电子数为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有个成语叫“物以类聚”,本意就是物质的分类。对物质进行分类,我们不仅能够根据类别通性预测物质的性质,还能探索各类物质的共性和特性。化学家根据需要将众多物质进行分类,现有下列几种物质:①冰水混合物 ②N2 ③CO ④Fe(OH)3胶体 ⑤Mg ⑥熔融Ca(OH)2 ⑦漂白粉 ⑧乙醇 ⑨盐酸。
(1)属于非电解质的是_______ (填序号,下同);属于强电解质的是_______ ;上述物质中弱电解质的电离方程式:_______ 。
(2)写出实验室制取④的化学方程式:_______ 。
(3)生活中“84”消毒液(有效成分为NaClO)和洁厕灵(主要成分是⑨ )不能混合使用,原因是_______ (用离子方程式表示)。
(4)新型陶瓷氮化铝可用氧化铝高温还原法制备: (未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为
(未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为_______ mol。
(1)属于非电解质的是
(2)写出实验室制取④的化学方程式:
(3)生活中“84”消毒液(有效成分为NaClO)和洁厕灵(主要成分是⑨ )不能混合使用,原因是
(4)新型陶瓷氮化铝可用氧化铝高温还原法制备:
 (未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为
(未配平),若反应中共转移3.01×1023个电子,则产生CO气体的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】I.有以下物质:
①石墨;②铝;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氯化氢气体。
(1)其中能导电的是___________________ ;
属于非电解质的是_________________ ;
属于强电解质的是__________________ ;
属于弱电解质的是________________ 。
(2)写出物质⑥溶于水的电离方程式:__________________________ 。
(3)写出物质⑥和⑧在水中反应的离子方程式:___________________ 。
Ⅱ.今有K2SO4和Al2(SO4)3的混合溶液,已知其中K+浓度是0.2mol•L-1,SO42- 的浓度是0.7mol•L-1。
(4)则 Al3+ 物质的量浓度应等于________________________ 。
Ⅲ.根据反应8NH3+3Cl2 =6NH4Cl+N2,回答下列问题:
(5)该反应中氧化剂是_________ ,氧化产物是__________ 。
(6)该反应中被氧化的物质与被还原的物质物质的量之比为______________ 。
(7)用单线桥法标出电子转移的方向与数目___________ 。
IV.有一包白色固体,可能含有K2CO3、NaNO3、KCl、BaSO4、CuSO4。按下列步骤实验:①取少量固体溶于水,得到无色溶液;②在所得的溶液中滴加硝酸银溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解,并有气体产生。根据上述实验现象判断:
(8)一定存在的物质是_____________ ;
(9)一定不存在的物质是________________ ;
(10)可能存在的物质是_____________ ;
①石墨;②铝;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氯化氢气体。
(1)其中能导电的是
属于非电解质的是
属于强电解质的是
属于弱电解质的是
(2)写出物质⑥溶于水的电离方程式:
(3)写出物质⑥和⑧在水中反应的离子方程式:
Ⅱ.今有K2SO4和Al2(SO4)3的混合溶液,已知其中K+浓度是0.2mol•L-1,SO42- 的浓度是0.7mol•L-1。
(4)则 Al3+ 物质的量浓度应等于
Ⅲ.根据反应8NH3+3Cl2 =6NH4Cl+N2,回答下列问题:
(5)该反应中氧化剂是
(6)该反应中被氧化的物质与被还原的物质物质的量之比为
(7)用单线桥法标出电子转移的方向与数目
IV.有一包白色固体,可能含有K2CO3、NaNO3、KCl、BaSO4、CuSO4。按下列步骤实验:①取少量固体溶于水,得到无色溶液;②在所得的溶液中滴加硝酸银溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解,并有气体产生。根据上述实验现象判断:
(8)一定存在的物质是
(9)一定不存在的物质是
(10)可能存在的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】
(1)维生素C又称为抗坏血酸,在人体内有重要的功能。例如,帮助人体将食物中摄取的不易吸收的Fe3+变为易吸收的Fe2+。这说明维生素C具有________ (填“氧化性”或“还原性”)。
(2)2Na+O2 Na2O2反应中,
Na2O2反应中,
①________ 被氧化,________ 是氧化剂,氧化产物是_______ ,过氧化钠中氧元素的化合价是_______ 。
②此反应中若转移了2 mol的电子,则需要氧气________ mol。
③用单线桥或双线桥法表示反应中电子转移的方向和数目:______________________ 。
(3)根据反应①2FeCl3+2KI=2FeCl2+2KCl+I2,②2FeCl2+Cl2=2FeCl3,判断下列物质的氧化性由强到弱的顺序中,正确的是____________ 。
A.Fe3+>Cl2>I2 B.Cl2>I2>Fe3+
C.I2>Cl2>Fe3+ D.Cl2>Fe3+>I2
(1)维生素C又称为抗坏血酸,在人体内有重要的功能。例如,帮助人体将食物中摄取的不易吸收的Fe3+变为易吸收的Fe2+。这说明维生素C具有
(2)2Na+O2
 Na2O2反应中,
Na2O2反应中,①
②此反应中若转移了2 mol的电子,则需要氧气
③用单线桥或双线桥法表示反应中电子转移的方向和数目:
(3)根据反应①2FeCl3+2KI=2FeCl2+2KCl+I2,②2FeCl2+Cl2=2FeCl3,判断下列物质的氧化性由强到弱的顺序中,正确的是
A.Fe3+>Cl2>I2 B.Cl2>I2>Fe3+
C.I2>Cl2>Fe3+ D.Cl2>Fe3+>I2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中,H2O2只发生如下过程:H2O2→O2。
(1)该物质H2O2在反应中表现出__________ (填写编号)。
a、氧化性 b、还原性 c、氧化性和还原性 d、均不正确
(2)若反应转移了5.418×1023个电子,则产生的气体在标准状况下的体积是________ L。
(3)将氧化剂和还原剂的化学式及配平后的系数填入下列方框中,并求出电子转移的数目: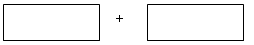
_______
(1)该物质H2O2在反应中表现出
a、氧化性 b、还原性 c、氧化性和还原性 d、均不正确
(2)若反应转移了5.418×1023个电子,则产生的气体在标准状况下的体积是
(3)将氧化剂和还原剂的化学式及配平后的系数填入下列方框中,并求出电子转移的数目:
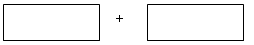
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】H2S是严重危害环境的气体,吸收H2S并加以利用是当前科学研究的热点。
(1)“沉淀吸收法”:将H2S用氨水溶液吸收得到 溶液,写出该过程的离子反应方程式
溶液,写出该过程的离子反应方程式_______ ;白色CuCl悬浊液中加入 溶液中,得到
溶液中,得到 黑色固体,该过程的化学反应方程式为
黑色固体,该过程的化学反应方程式为_______ 。
(2)“铁盐氧化吸收法”:用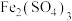 溶液吸收H2S,溶液中有淡黄色的固体析出,反应的原理用离子方程式表示为
溶液吸收H2S,溶液中有淡黄色的固体析出,反应的原理用离子方程式表示为___ ;反应后的溶液在硫杆菌作用下进行再生,反应为: ,若反应温度过高,反应速率下降,其原因是
,若反应温度过高,反应速率下降,其原因是_ 。
(3)“ 氧化吸收法”:一定条件下将H2S通入双氧水中,随着参加反应的
氧化吸收法”:一定条件下将H2S通入双氧水中,随着参加反应的 变化,产物发生变化。若产物中
变化,产物发生变化。若产物中 ,则理论上消耗的
,则理论上消耗的
_______ 。
(4)“循环吸收法”:将H2S和空气的混合气体通入 、
、 、
、 的混合溶液中反应回收S,其物质转化如图所示。空白圆圈内的物质的化学式为
的混合溶液中反应回收S,其物质转化如图所示。空白圆圈内的物质的化学式为_______ 。

(1)“沉淀吸收法”:将H2S用氨水溶液吸收得到
 溶液,写出该过程的离子反应方程式
溶液,写出该过程的离子反应方程式 溶液中,得到
溶液中,得到 黑色固体,该过程的化学反应方程式为
黑色固体,该过程的化学反应方程式为(2)“铁盐氧化吸收法”:用
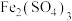 溶液吸收H2S,溶液中有淡黄色的固体析出,反应的原理用离子方程式表示为
溶液吸收H2S,溶液中有淡黄色的固体析出,反应的原理用离子方程式表示为 ,若反应温度过高,反应速率下降,其原因是
,若反应温度过高,反应速率下降,其原因是(3)“
 氧化吸收法”:一定条件下将H2S通入双氧水中,随着参加反应的
氧化吸收法”:一定条件下将H2S通入双氧水中,随着参加反应的 变化,产物发生变化。若产物中
变化,产物发生变化。若产物中 ,则理论上消耗的
,则理论上消耗的
(4)“循环吸收法”:将H2S和空气的混合气体通入
 、
、 、
、 的混合溶液中反应回收S,其物质转化如图所示。空白圆圈内的物质的化学式为
的混合溶液中反应回收S,其物质转化如图所示。空白圆圈内的物质的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知反应:①SO2+H2O=H2SO3;②2SO2+O2=2SO3;③SO2+2H2S=3S↓+2H2O。
(1)上述反应中不属于氧化还原反应的是_____ ;SO2做还原剂的是_____ ,SO2做氧化剂的是______ 。
(2)反应③中,参与反应的氧化剂与还原剂的质量比是______ 。
(3)误食亚硝酸钠(NaNO2)会使人体血液中的Fe2+转化为Fe3+而引起中毒,服用维生素C可使Fe3+转化为Fe2+,从而达到解毒的目的。由此可见,在解毒反应中,维生素C表现__________ 性。
(1)上述反应中不属于氧化还原反应的是
(2)反应③中,参与反应的氧化剂与还原剂的质量比是
(3)误食亚硝酸钠(NaNO2)会使人体血液中的Fe2+转化为Fe3+而引起中毒,服用维生素C可使Fe3+转化为Fe2+,从而达到解毒的目的。由此可见,在解毒反应中,维生素C表现
您最近一年使用:0次

 CuCl2。反应中每生成1 mol CuCl2,消耗Cu的物质的量是
CuCl2。反应中每生成1 mol CuCl2,消耗Cu的物质的量是

