现有下列物质:
①熔融NaCl;② 溶液;③氯气;④
溶液;③氯气;④ ;⑤NaOH溶液;⑥氢氧化铁胶体;⑦
;⑤NaOH溶液;⑥氢氧化铁胶体;⑦ ;⑧铜; ⑨ 过氧化钠; ⑩
;⑧铜; ⑨ 过氧化钠; ⑩
(1)上述物质中属于电解质的是___________ (填标号)。
(2)将②逐滴加入⑥中的现象是___________ 。
(3)④加入过量的氢氧化钡溶液中,发生反应的离子方程式为___________ 。
(4)③通入石灰乳中,发生反应的化学方程式为___________ 。
(5)⑦与⑨反应的化学方程式为:___________ ,该反应生成标准状况下22.4L氧气,转移的电子数目为___________ 。
①熔融NaCl;②
 溶液;③氯气;④
溶液;③氯气;④ ;⑤NaOH溶液;⑥氢氧化铁胶体;⑦
;⑤NaOH溶液;⑥氢氧化铁胶体;⑦ ;⑧铜; ⑨ 过氧化钠; ⑩
;⑧铜; ⑨ 过氧化钠; ⑩
(1)上述物质中属于电解质的是
(2)将②逐滴加入⑥中的现象是
(3)④加入过量的氢氧化钡溶液中,发生反应的离子方程式为
(4)③通入石灰乳中,发生反应的化学方程式为
(5)⑦与⑨反应的化学方程式为:
更新时间:2024-01-18 16:46:13
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列填空
(1)现有下列八种物质:①纯硝酸、②NaHSO4晶体、③熔融的NaCl、④CO2、⑤金属铝、⑥Ba(OH)2固体、⑦氢氧化铁胶体、⑧氨水
a.上述八种物质中,属于电解质且在给定条件下能导电有____ (填序号,下同)。属于非电解质,但溶于水能导电的有___ 。
b.有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,该反应的化学方程式为:___ 。
c.向Ba(OH)2溶液中滴加NaHSO4溶液至溶液呈中性,该反应的离子方程式为:____ 。
(2)向盛有沸水的烧杯中滴加饱和FeCl3溶液,继续加热可制得Fe(OH)3胶体。
①欲验证FeCl3溶液已转化为胶体的实验方法是___ 。
②利用如图所示装置可除去Fe(OH)3胶体中的杂质,实验中需不断____ 。

(3)在室温下,发生下列几种反应:①16H++10Z-+2XO =2X2++5Z2+8H2O②2A2++B2=2A3++2B-③2B-+Z2=B2+2Z-
=2X2++5Z2+8H2O②2A2++B2=2A3++2B-③2B-+Z2=B2+2Z-
a.在溶液中以下反应:8H++5A2++XO =X2++5A3++4H2O能否发生?
=X2++5A3++4H2O能否发生?___ (填“是”或“否”)。
b.要氧化除去含有A2+、Z-、B-混合溶液中的A2+,应加入___ (所需物质在以上方程式中寻找)。
(1)现有下列八种物质:①纯硝酸、②NaHSO4晶体、③熔融的NaCl、④CO2、⑤金属铝、⑥Ba(OH)2固体、⑦氢氧化铁胶体、⑧氨水
a.上述八种物质中,属于电解质且在给定条件下能导电有
b.有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,该反应的化学方程式为:
c.向Ba(OH)2溶液中滴加NaHSO4溶液至溶液呈中性,该反应的离子方程式为:
(2)向盛有沸水的烧杯中滴加饱和FeCl3溶液,继续加热可制得Fe(OH)3胶体。
①欲验证FeCl3溶液已转化为胶体的实验方法是
②利用如图所示装置可除去Fe(OH)3胶体中的杂质,实验中需不断

(3)在室温下,发生下列几种反应:①16H++10Z-+2XO
 =2X2++5Z2+8H2O②2A2++B2=2A3++2B-③2B-+Z2=B2+2Z-
=2X2++5Z2+8H2O②2A2++B2=2A3++2B-③2B-+Z2=B2+2Z-a.在溶液中以下反应:8H++5A2++XO
 =X2++5A3++4H2O能否发生?
=X2++5A3++4H2O能否发生?b.要氧化除去含有A2+、Z-、B-混合溶液中的A2+,应加入
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铁是地壳中占比较高的元素,其化合物在自然界十分常见。
(1)某铁原子可表示为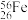 ,其核内中子数是
,其核内中子数是___________ 。
(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为___________ ;设阿伏加德罗常数的值为 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为___________ 。
(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入___________ 溶液并振荡,若滤液变为红色,则药品已变质。
(4)现有甲、乙、丙三名同学分别进行制备 胶体的实验。甲同学向
胶体的实验。甲同学向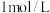 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
①操作正确的同学是___________ 。
②写出制备胶体过程中的离子方程式___________ 。欲除去胶体中混有的 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是___________ 。
③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为___________ 。
(1)某铁原子可表示为
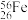 ,其核内中子数是
,其核内中子数是(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为
 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入
(4)现有甲、乙、丙三名同学分别进行制备
 胶体的实验。甲同学向
胶体的实验。甲同学向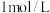 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。①操作正确的同学是
②写出制备胶体过程中的离子方程式
 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)现有以下物质:① 溶液;②液氨:③
溶液;②液氨:③ 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑧铜;⑦
胶体;⑧铜;⑦ ;⑧
;⑧ ;⑨蔗糖;⑩矿泉水,以上物质中属于电解质的是
;⑨蔗糖;⑩矿泉水,以上物质中属于电解质的是_______ (填序号),属于非电解质的是:_______ (填序号)。写出④在该条件下的电离方程式:_______ ,⑧在水溶液条件下的电离方程式:_______ 。
(2)明胶的水浴液和 溶液共同具备的性质是
溶液共同具备的性质是_______ (填序号)。
a.都不稳定,密封放置会产生沉淀 b.分散质粒子可通过滤纸 c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的_______ (填序号)。
A. B.
B.  C.
C. 
(4)实验室常用向煮沸的蒸馏水中滴加饱和 溶液制备
溶液制备 胶体,证明有胶体生成的最常用的检验方法是
胶体,证明有胶体生成的最常用的检验方法是_______ 。
(5)现有10 明胶的水溶液与5
明胶的水溶液与5
 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜进入溶液:
能够透过半透膜进入溶液:_______ 。
(1)现有以下物质:①
 溶液;②液氨:③
溶液;②液氨:③ 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑧铜;⑦
胶体;⑧铜;⑦ ;⑧
;⑧ ;⑨蔗糖;⑩矿泉水,以上物质中属于电解质的是
;⑨蔗糖;⑩矿泉水,以上物质中属于电解质的是(2)明胶的水浴液和
 溶液共同具备的性质是
溶液共同具备的性质是a.都不稳定,密封放置会产生沉淀 b.分散质粒子可通过滤纸 c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的
A.
 B.
B.  C.
C. 
(4)实验室常用向煮沸的蒸馏水中滴加饱和
 溶液制备
溶液制备 胶体,证明有胶体生成的最常用的检验方法是
胶体,证明有胶体生成的最常用的检验方法是(5)现有10
 明胶的水溶液与5
明胶的水溶液与5
 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜进入溶液:
能够透过半透膜进入溶液:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:____________________
(2)该反应中氧化剂和还原剂的物质的量之比为______________ ;
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为____________ ;
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:
(2)该反应中氧化剂和还原剂的物质的量之比为
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.钛及其合金具有密度小,强度高,耐腐蚀等优良性能,被广泛用于航天、航空、航海、石油化工、医药等部门,因此,钛被誉为第三金属和战略金属。从钛铁矿提取金属钛(海绵钛)的主要工艺过程如下:
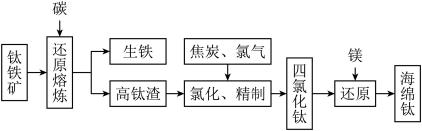
(1)钛铁矿的主要成分是 ,第一步发生的反应:
,第一步发生的反应: ,在钛酸亚铁中,钛的化合价为
,在钛酸亚铁中,钛的化合价为___________ 。
(2)第二步:二氧化钛在高温下与焦炭、氯气反应生成四氯化钛和一氧化碳,该反应的氧化产物是___________ ,氧化剂和还原剂的化学计量数之比是___________ 。
Ⅱ.高铁酸钾 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比 、
、 、
、 、
、 氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。
至饱和,使高铁酸钾析出。
(3)干法制备高铁酸钠的主要反应为: 该反应中还原剂是
该反应中还原剂是___________ (填化学式)。
(4)湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。
。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:___________ 。
②每生成 转移
转移___________  电子,若反应过程中转移了
电子,若反应过程中转移了 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为___________ mol。

(1)钛铁矿的主要成分是
 ,第一步发生的反应:
,第一步发生的反应: ,在钛酸亚铁中,钛的化合价为
,在钛酸亚铁中,钛的化合价为(2)第二步:二氧化钛在高温下与焦炭、氯气反应生成四氯化钛和一氧化碳,该反应的氧化产物是
Ⅱ.高铁酸钾
 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比 、
、 、
、 、
、 氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。
至饱和,使高铁酸钾析出。(3)干法制备高铁酸钠的主要反应为:
 该反应中还原剂是
该反应中还原剂是(4)湿法制备高铁酸钾(
 )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。
。①请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
②每生成
 转移
转移 电子,若反应过程中转移了
电子,若反应过程中转移了 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有下列物质:①NaOH、②氨水、③蔗糖、④氯化铁、⑤氯气、⑥SO2、⑦硫酸铜溶液、⑧氢氧化铝胶体。
(1)属于强电解质的是___ (填序号,下同);属于非电解质的是___ 。
(2)区分⑦与⑧的实验方法是___ (填方法名称)。
(3)写出氯化铁溶于水的电离方程式:___ 。
(4)写出①的溶液与⑥反应的化学方程式:___ 。
(1)属于强电解质的是
(2)区分⑦与⑧的实验方法是
(3)写出氯化铁溶于水的电离方程式:
(4)写出①的溶液与⑥反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ、掌握电解质和非电解质的概念,能熟练判断一种物质是否是电解质,是认识电解质的性质的前提:以下有①~⑩种物质:①石墨②液氯③氨水④ ⑤
⑤ ⑥
⑥ ⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融
⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融 ⑩蔗糖
⑩蔗糖
(1)上述物质属于电解质的是___________ ;(填序号,多写不给分,下同)属于非电解质的是___________ 。
(2)下列制备⑦的操作方法正确的是___________。(填字母)
(3)向盛有⑦的烧杯中还滴加入盐酸至过量,会出现一系列变化,现象为:___________ 。
(4)写出⑥溶液中加入⑨溶液至 完全沉淀的离子反应方程式
完全沉淀的离子反应方程式___________ 。
Ⅱ、高铁酸钠 是一种新型的净水剂,可以通过下述反应制取(未配平):
是一种新型的净水剂,可以通过下述反应制取(未配平):
(5)配平下面方程式并用单线桥标出电子转移情况:___________ 。
 。
。
 ⑤
⑤ ⑥
⑥ ⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融
⑦红褐色的氢氧化铁胶体⑧稀硫酸⑨熔融 ⑩蔗糖
⑩蔗糖(1)上述物质属于电解质的是
(2)下列制备⑦的操作方法正确的是___________。(填字母)
| A.向饱和氯化铁溶液中滴加适量的氢氧化钠稀溶液 |
| B.加热煮沸氯化铁饱和溶液 |
| C.在氨水中滴加氯化铁浓溶液 |
| D.在沸水中滴加饱和氯化铁溶液,煮沸至出现红褐色液体 |
(4)写出⑥溶液中加入⑨溶液至
 完全沉淀的离子反应方程式
完全沉淀的离子反应方程式Ⅱ、高铁酸钠
 是一种新型的净水剂,可以通过下述反应制取(未配平):
是一种新型的净水剂,可以通过下述反应制取(未配平):(5)配平下面方程式并用单线桥标出电子转移情况:
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】分类思想在化学中有重要的应用,通常会对物质及反应进行分类研究。
(1)①空气②氧气③食盐水④氢氧化钾⑤铜⑥碳酸氢钠⑦蔗糖⑧酒精。以上物质中,属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)SO2是一种酸性氧化物,可制取Na2SO3,从括号内所给试剂(NaCl溶液、NaOH溶液、Na2SO4溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:___________ 。
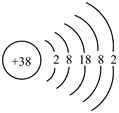
(3)锶( )原子的结构示意图如图所示,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:
)原子的结构示意图如图所示,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:___________ 。
(4)MnO2可经过如图所示的转化制取MnCO3。已知“反应Ⅱ”为复分解反应。
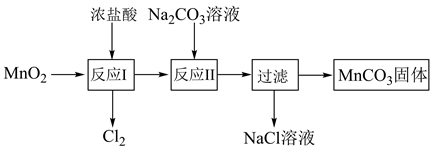
①写出“反应Ⅱ”的离子方程式:___________ 。
②过滤操作需要的玻璃仪器有烧杯、___________ 、___________ 。
③过滤后对沉淀进行洗涤,检验沉淀是否洗涤干净的操作为___________ 。
(1)①空气②氧气③食盐水④氢氧化钾⑤铜⑥碳酸氢钠⑦蔗糖⑧酒精。以上物质中,属于电解质的是
(2)SO2是一种酸性氧化物,可制取Na2SO3,从括号内所给试剂(NaCl溶液、NaOH溶液、Na2SO4溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:
(3)锶(
 )原子的结构示意图如图所示,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:
)原子的结构示意图如图所示,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:
(4)MnO2可经过如图所示的转化制取MnCO3。已知“反应Ⅱ”为复分解反应。

①写出“反应Ⅱ”的离子方程式:
②过滤操作需要的玻璃仪器有烧杯、
③过滤后对沉淀进行洗涤,检验沉淀是否洗涤干净的操作为
您最近一年使用:0次



