名校
1 . Ⅰ.钛及其合金具有密度小,强度高,耐腐蚀等优良性能,被广泛用于航天、航空、航海、石油化工、医药等部门,因此,钛被誉为第三金属和战略金属。从钛铁矿提取金属钛(海绵钛)的主要工艺过程如下:
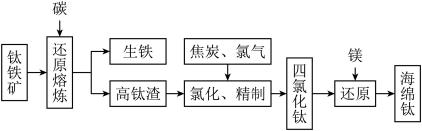
(1)钛铁矿的主要成分是 ,第一步发生的反应:
,第一步发生的反应: ,在钛酸亚铁中,钛的化合价为
,在钛酸亚铁中,钛的化合价为___________ 。
(2)第二步:二氧化钛在高温下与焦炭、氯气反应生成四氯化钛和一氧化碳,该反应的氧化产物是___________ ,氧化剂和还原剂的化学计量数之比是___________ 。
Ⅱ.高铁酸钾 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比 、
、 、
、 、
、 氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。
至饱和,使高铁酸钾析出。
(3)干法制备高铁酸钠的主要反应为: 该反应中还原剂是
该反应中还原剂是___________ (填化学式)。
(4)湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。
。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:___________ 。
②每生成 转移
转移___________  电子,若反应过程中转移了
电子,若反应过程中转移了 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为___________ mol。

(1)钛铁矿的主要成分是
 ,第一步发生的反应:
,第一步发生的反应: ,在钛酸亚铁中,钛的化合价为
,在钛酸亚铁中,钛的化合价为(2)第二步:二氧化钛在高温下与焦炭、氯气反应生成四氯化钛和一氧化碳,该反应的氧化产物是
Ⅱ.高铁酸钾
 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比 、
、 、
、 、
、 氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。
至饱和,使高铁酸钾析出。(3)干法制备高铁酸钠的主要反应为:
 该反应中还原剂是
该反应中还原剂是(4)湿法制备高铁酸钾(
 )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。
。①请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
②每生成
 转移
转移 电子,若反应过程中转移了
电子,若反应过程中转移了 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为
您最近一年使用:0次
2023-07-17更新
|
333次组卷
|
3卷引用:安徽省阜阳市阜南县2022-2023学年高一上学期期末联考化学试题
名校
2 . 化学与人类生活密切相关。按要求回答下列问题:
(1)将新鲜的花瓣放入干燥的氯气中可观察到的现象是___________ ,原因是___________ 。
(2)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸___________ ,反应的化学方程式为___________ 。
(3) 是一种重要的净水剂,可用下列方法制得:
是一种重要的净水剂,可用下列方法制得: 。当反应中有1mol
。当反应中有1mol 生成时,消耗
生成时,消耗 在标况下的体积为
在标况下的体积为___________ L,转移电子数为___________ 。
(1)将新鲜的花瓣放入干燥的氯气中可观察到的现象是
(2)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸
(3)
 是一种重要的净水剂,可用下列方法制得:
是一种重要的净水剂,可用下列方法制得: 。当反应中有1mol
。当反应中有1mol 生成时,消耗
生成时,消耗 在标况下的体积为
在标况下的体积为
您最近一年使用:0次
3 . 航天员王亚平在“天宫课堂”中介绍了空间站中的生活,在轨演示了水球变气球等一系列炫酷又好玩的实验。
I.“天宫”中水和氧气最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。
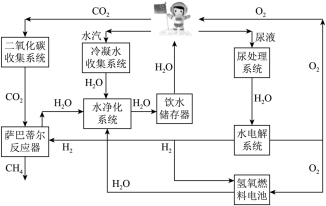
(1)“水电解系统”中产生氧气发生反应的化学方程式为_______ ,每转移8mol电子,生成_______ g的 O2。
(2)在水净化系统中,用臭氧(O3)消毒,臭氧在一定条件下转化为氧气的化学方程式为_______ ,该反应_______ (填“是”或“否”)氧化还原反应。
(3)一定条件 “萨巴蒂尔反应器”可除去CO2,该反应化学方程式为_______ 。
II.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不逸出,使水球越来越大。
(4)泡腾片在水中发生了如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3_______ (补全化学方程式)。
(5)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的_______ (填序号)。
A. B.
B. C.
C.
I.“天宫”中水和氧气最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。

(1)“水电解系统”中产生氧气发生反应的化学方程式为
(2)在水净化系统中,用臭氧(O3)消毒,臭氧在一定条件下转化为氧气的化学方程式为
(3)一定条件 “萨巴蒂尔反应器”可除去CO2,该反应化学方程式为
II.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不逸出,使水球越来越大。
(4)泡腾片在水中发生了如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3
(5)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的
A.
 B.
B. C.
C.
您最近一年使用:0次
名校
4 . 已知硫可与热的KOH溶液发生反应,反应的化学方程式如下: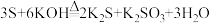 ,据此回答以下问题:
,据此回答以下问题:
(1)在上述反应中,氧化剂是_______ ,还原产物是_______ 。
(2)硫单质是一种_______ 色的固体,不溶于水,微溶于酒精,易溶于 ,根据以上溶解性,可以用
,根据以上溶解性,可以用_______ 除去附着在试管内壁的硫单质。
(3)在上述反应中,若有3mol硫单质参与反应,则转移电子的物质的量是_______ mol。
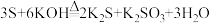 ,据此回答以下问题:
,据此回答以下问题:(1)在上述反应中,氧化剂是
(2)硫单质是一种
 ,根据以上溶解性,可以用
,根据以上溶解性,可以用(3)在上述反应中,若有3mol硫单质参与反应,则转移电子的物质的量是
您最近一年使用:0次
5 . 根据下列物质的转化关系请完成下列空白。
C CO2
CO2 H2CO3
H2CO3 CaCO3
CaCO3 CO2
CO2
(1)转化反应中属于复分解反应的是_______ (填反应序号,下同),氧化还原 反应的是_______ 。
(2)上述氧化还原反应中氧化剂的名称是_______ ,若标准状况下生成11.2L CO2 ,则转移 电子数为_______ ,生成还原产物的质量为_______ 。
(3)写出反应③的离子方程式_______ 。
C
 CO2
CO2 H2CO3
H2CO3 CaCO3
CaCO3 CO2
CO2(1)转化反应中属于复分解反应的是
(2)上述氧化还原反应中氧化剂的名称是
(3)写出反应③的离子方程式
您最近一年使用:0次
名校
解题方法
6 . 某兴趣小组设计如下装置进行氯气与金属钠的反应,先将钠预热,在钠熔融成小球时,撤火,并通入氯气发生反应。

(1)实验室制备氯气的化学方程式为_______ 。
(2) 与Na反应会产生大量白烟,白烟的成分是
与Na反应会产生大量白烟,白烟的成分是_______ (填化学式)。
(3)浸有淀粉-KI溶液的棉球变为蓝色,是因为 与KI发生置换反应,该反应的化学方程式为
与KI发生置换反应,该反应的化学方程式为_______ 。
(4)浸有NaOH溶液的棉球的作用是_______ 。若将 通入热的烧碱溶液中,可以得到NaCl、NaClO和
通入热的烧碱溶液中,可以得到NaCl、NaClO和 的混合液。当NaCl和
的混合液。当NaCl和 的物质的量之比为8︰1时,混合液中NaClO和
的物质的量之比为8︰1时,混合液中NaClO和 的物质的量之比为
的物质的量之比为_______ 。

(1)实验室制备氯气的化学方程式为
(2)
 与Na反应会产生大量白烟,白烟的成分是
与Na反应会产生大量白烟,白烟的成分是(3)浸有淀粉-KI溶液的棉球变为蓝色,是因为
 与KI发生置换反应,该反应的化学方程式为
与KI发生置换反应,该反应的化学方程式为(4)浸有NaOH溶液的棉球的作用是
 通入热的烧碱溶液中,可以得到NaCl、NaClO和
通入热的烧碱溶液中,可以得到NaCl、NaClO和 的混合液。当NaCl和
的混合液。当NaCl和 的物质的量之比为8︰1时,混合液中NaClO和
的物质的量之比为8︰1时,混合液中NaClO和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
2022-12-08更新
|
230次组卷
|
2卷引用:北京市第五中学2022-2023学年高一上学期第二次阶段检测化学试题
名校
7 . 实验室里用软锰矿(含MnO2质量分数为60%)与浓盐酸反应来制取适量的氯气,反应方程式如下: (假设HCl全部参加反应,杂质不参与反应)。
(假设HCl全部参加反应,杂质不参与反应)。
(1)用双线桥标出该反应中电子转移的方向和数目_______ 。
(2)若生成5个Cl2分子,计算转移电子总数_______ 。
(3)产生7.1g氯气时,计算所需软锰矿的质量_______ ,被氧化的HCl的质量_______ 。
 (假设HCl全部参加反应,杂质不参与反应)。
(假设HCl全部参加反应,杂质不参与反应)。(1)用双线桥标出该反应中电子转移的方向和数目
(2)若生成5个Cl2分子,计算转移电子总数
(3)产生7.1g氯气时,计算所需软锰矿的质量
您最近一年使用:0次
21-22高一下·浙江·期中
名校
解题方法
8 . 将24.8g铜铁合金与足量稀硝酸完全反应,放出6. 72LNO气体(标况下),请计算:
(1)转移电子数为_______ 。
(2)向反应后的溶液中加入NaOH溶液至完全沉淀,得到沉淀的质量为_______ 。
(1)转移电子数为
(2)向反应后的溶液中加入NaOH溶液至完全沉淀,得到沉淀的质量为
您最近一年使用:0次
解题方法
9 . 已知反应2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O,若有44.8 L Cl2(已换算为标准状况)生成,求:
(1)被氧化的HCl为________ g,转移电子数目为________ 。
(2)用“双线桥”和“单线桥”标出上述反应的电子转移方向和数目________ 。
(1)被氧化的HCl为
(2)用“双线桥”和“单线桥”标出上述反应的电子转移方向和数目
您最近一年使用:0次
21-22高一·全国·课时练习
解题方法
10 . 将0.3molCu与足量的稀硝酸反应,被还原的硝酸为_______ mol,转移的电子数为_______ 个。
您最近一年使用:0次



