解题方法
1 . 请同学们仔细思考并回答下列问题:
(1)过氧化钠与二氧化碳反应的化学方程式为___________ ;39g过氧化钠完全反应,转移的电子数为___________ ,生成___________ L(换算成标准状况下)氧气。
(2) 与
与___________  所含的原子数目相等。
所含的原子数目相等。
(3)如图所示,将等质量的气体m和气体n充入带有活塞(可自由移动且厚度不计)的密闭容器中,最终活塞停留在图示位置,则m与n的摩尔质量之比为___________ 。

(4)实验室可用 固体与浓盐酸常温下反应制备氯气。
固体与浓盐酸常温下反应制备氯气。

该反应的氧化剂为___________ ,写出配平后的上述反应的化学方程式:___________ 。
(1)过氧化钠与二氧化碳反应的化学方程式为
(2)
 与
与 所含的原子数目相等。
所含的原子数目相等。(3)如图所示,将等质量的气体m和气体n充入带有活塞(可自由移动且厚度不计)的密闭容器中,最终活塞停留在图示位置,则m与n的摩尔质量之比为

(4)实验室可用
 固体与浓盐酸常温下反应制备氯气。
固体与浓盐酸常温下反应制备氯气。
该反应的氧化剂为
您最近一年使用:0次
名校
2 . 化学与人类生活密切相关。按要求回答下列问题:
(1)将新鲜的花瓣放入干燥的氯气中可观察到的现象是___________ ,原因是___________ 。
(2)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸___________ ,反应的化学方程式为___________ 。
(3) 是一种重要的净水剂,可用下列方法制得:
是一种重要的净水剂,可用下列方法制得: 。当反应中有1mol
。当反应中有1mol 生成时,消耗
生成时,消耗 在标况下的体积为
在标况下的体积为___________ L,转移电子数为___________ 。
(1)将新鲜的花瓣放入干燥的氯气中可观察到的现象是
(2)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸
(3)
 是一种重要的净水剂,可用下列方法制得:
是一种重要的净水剂,可用下列方法制得: 。当反应中有1mol
。当反应中有1mol 生成时,消耗
生成时,消耗 在标况下的体积为
在标况下的体积为
您最近一年使用:0次
名校
3 . 已知硫可与热的KOH溶液发生反应,反应的化学方程式如下: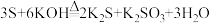 ,据此回答以下问题:
,据此回答以下问题:
(1)在上述反应中,氧化剂是_______ ,还原产物是_______ 。
(2)硫单质是一种_______ 色的固体,不溶于水,微溶于酒精,易溶于 ,根据以上溶解性,可以用
,根据以上溶解性,可以用_______ 除去附着在试管内壁的硫单质。
(3)在上述反应中,若有3mol硫单质参与反应,则转移电子的物质的量是_______ mol。
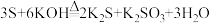 ,据此回答以下问题:
,据此回答以下问题:(1)在上述反应中,氧化剂是
(2)硫单质是一种
 ,根据以上溶解性,可以用
,根据以上溶解性,可以用(3)在上述反应中,若有3mol硫单质参与反应,则转移电子的物质的量是
您最近一年使用:0次
4 . 根据下列物质的转化关系请完成下列空白。
C CO2
CO2 H2CO3
H2CO3 CaCO3
CaCO3 CO2
CO2
(1)转化反应中属于复分解反应的是_______ (填反应序号,下同),氧化还原 反应的是_______ 。
(2)上述氧化还原反应中氧化剂的名称是_______ ,若标准状况下生成11.2L CO2 ,则转移 电子数为_______ ,生成还原产物的质量为_______ 。
(3)写出反应③的离子方程式_______ 。
C
 CO2
CO2 H2CO3
H2CO3 CaCO3
CaCO3 CO2
CO2(1)转化反应中属于复分解反应的是
(2)上述氧化还原反应中氧化剂的名称是
(3)写出反应③的离子方程式
您最近一年使用:0次
5 . 常温下KMnO4氧化浓HCl的反应如下:KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O
(1)请配平上述反应方程式,系数依次为_______ 。
(2)盐酸在反应中显示出来的性质是_______ 。
(3)有63.2g高锰酸钾参加反应,则被氧化的HCl的物质的量为_______ mol,转移的电子数为_______ ,产生的Cl2在标准状况下的体积约为_______ L。
(1)请配平上述反应方程式,系数依次为
(2)盐酸在反应中显示出来的性质是
(3)有63.2g高锰酸钾参加反应,则被氧化的HCl的物质的量为
您最近一年使用:0次
21-22高一·全国·课时练习
解题方法
6 . 将0.3molCu与足量的稀硝酸反应,被还原的硝酸为_______ mol,转移的电子数为_______ 个。
您最近一年使用:0次
解题方法
7 . 在碱性介质中有利于卤素单质的歧化反应,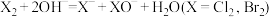 ,
, 在碱性介质中也会发生歧化反应,其反应速率与温度有关,如
在碱性介质中也会发生歧化反应,其反应速率与温度有关,如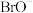 在
在 左右歧化反应很慢,在
左右歧化反应很慢,在 则全部转化为
则全部转化为 和
和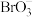 。
。
(1)某温度下,含 的溴水与
的溴水与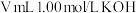 溶液恰好完全反应,则
溶液恰好完全反应,则
_______ 。
(2)某温度下,含 的溴水与
的溴水与 溶液恰好完全反应,若反应后
溶液恰好完全反应,若反应后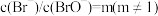 ,则反应转移电子数
,则反应转移电子数
_______ 。(用含m的式子表示)
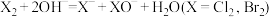 ,
, 在碱性介质中也会发生歧化反应,其反应速率与温度有关,如
在碱性介质中也会发生歧化反应,其反应速率与温度有关,如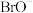 在
在 左右歧化反应很慢,在
左右歧化反应很慢,在 则全部转化为
则全部转化为 和
和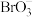 。
。(1)某温度下,含
 的溴水与
的溴水与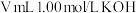 溶液恰好完全反应,则
溶液恰好完全反应,则
(2)某温度下,含
 的溴水与
的溴水与 溶液恰好完全反应,若反应后
溶液恰好完全反应,若反应后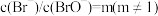 ,则反应转移电子数
,则反应转移电子数
您最近一年使用:0次
8 . 已知MnO2与浓盐酸反应的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:
(1)该反应的离子方程式为_______ 。
(2)用单线桥表示出电子的转移和数目_______
(3)该反应中HCl体现的性质是_______ ,氧化产物是_______ ,反应中氧化剂和还原剂的物质的量之比_______ 。
(4)当有1molCl2生成时,则被氧化的HCl的质量是_______ g,该反应转移的电子数为_______ (设NA为阿伏加德罗常数的值)。
 MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:(1)该反应的离子方程式为
(2)用单线桥表示出电子的转移和数目
(3)该反应中HCl体现的性质是
(4)当有1molCl2生成时,则被氧化的HCl的质量是
您最近一年使用:0次
解题方法
9 . 用NA表示阿伏加德罗常数,判断下列说法是否正确。
1.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA。(_______)
2.常温下,密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA。(_______)
3.常温下,56 g铁片投入足量浓H2SO4中生成NA个SO2分子。(_______)
4.一定条件下,用 1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA。(_______)
5.标准状况下,将22.4 L Cl2通入足量水中充分反应,转移电子数小于NA。(_______)
1.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA。(_______)
2.常温下,密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA。(_______)
3.常温下,56 g铁片投入足量浓H2SO4中生成NA个SO2分子。(_______)
4.一定条件下,用 1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA。(_______)
5.标准状况下,将22.4 L Cl2通入足量水中充分反应,转移电子数小于NA。(_______)
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
10 . 含2molH2SO4的浓硫酸与足量的铜片在加热条件下完全反应,可产生NA个SO2气体分子___
您最近一年使用:0次



