完成下列计算:
(1)若ag CO2含b个原子,则阿伏加德罗常数为___________ mol-1。
(2)含0.6molCl-的氯化镁的质量是___________ g。
(3)已知4.8g CO2和CO混合气体中含分子数为0.15NA,该混合气体的平均摩尔质量为___________ ,CO2和CO的物质的量之比是___________ 。
(1)若ag CO2含b个原子,则阿伏加德罗常数为
(2)含0.6molCl-的氯化镁的质量是
(3)已知4.8g CO2和CO混合气体中含分子数为0.15NA,该混合气体的平均摩尔质量为
更新时间:2022-11-24 17:29:25
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】物质的量是高中化学中常用的物理量,请按要求完成下列各小题。
(1)9.03×1023个NH3含___________ mol氢原子,___________ mol质子,在标准状况下的体积约为___________ L,氮原子与氢原子个数比___________ 。
(2)___________ molCO2分子中含有的氧原子数与1.806×1024个H2O中含有的氧原子数相同。
(3)在NaCl、MgCl2、MgSO4形成的混合溶液中,C(Na+)=0.10mol·L-1,C(Mg2+)=0.25mol·L-1,C(Cl-)=0.20mol·L-1,则C(S )为
)为___________ 。
(1)9.03×1023个NH3含
(2)
(3)在NaCl、MgCl2、MgSO4形成的混合溶液中,C(Na+)=0.10mol·L-1,C(Mg2+)=0.25mol·L-1,C(Cl-)=0.20mol·L-1,则C(S
 )为
)为
您最近一年使用:0次
【推荐2】(1)在标况下,___ LCO2中含有1molO原子,其质量是___ 。
(2)质量之比为16:7:6的三种气体SO2、CO、NO,其氧原子数之比为___ 。
(3)在标准状况下,有CH4和CO的混和气体共6.72L,其质量为6g,该混和气体中CH4的物质的量为___ ,CO的分子数为___ 。
(2)质量之比为16:7:6的三种气体SO2、CO、NO,其氧原子数之比为
(3)在标准状况下,有CH4和CO的混和气体共6.72L,其质量为6g,该混和气体中CH4的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】采用电镀法进行阿伏加德罗常数的测定。通过手持技术测定电量Q、用分析天平测定电镀前后镀件的质量m。在250mL电解槽中注入200mL饱和硫酸铜溶液,插入洁净的铜电极,连接直流电源及检测仪器。实验得到如下数据:
已知:单个电子的电荷量e= 1.6 ×10-19C。
(1)计算阿伏加德罗常数(NA )的表达式为: NA=___________ (用Q、△m及e表示)。
(2)列式计算阿伏加德罗常数(NA )_______ 。
| 实验序号 | 电量Q/C | m1/g | m2/g | Δm |
| 1 | 122.6 | 12.962 0 | 13.004 1 | 0.042 0 |
| 2 | 123.2 | 12.958 1 | 13.0041 | 0.042 0 |
| 3 | 122.6 | 12.964 0 | 13.005 1 | 0.041 1 |
已知:单个电子的电荷量e= 1.6 ×10-19C。
(1)计算阿伏加德罗常数(NA )的表达式为: NA=
(2)列式计算阿伏加德罗常数(NA )
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)如图为物质B(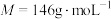 )在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。
)在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。

①80℃时,100g水做溶剂,达到饱和时,溶解的B的质量为_______ g,物质的量为_______ mol;
②80℃时,物质饱和溶液的物质的量浓度为_______ mol∙L-1。
(2)某小组利用如图装置测定常温常压下的气体摩尔体积。取0.112g已去除氧化膜的铁片放入烧瓶中,调节量气管与水准管液面相平,再用注射器向烧瓶中注入10mL 硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。
硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。

计算:
①反应后溶液中c(H+)=_______ mol∙L-1 (忽略反应前后溶液体积变化);
②计算常温常压下的气体摩尔体积_______ L∙mol-1。
(1)如图为物质B(
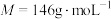 )在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。
)在水中的溶解度曲线(g∙g-1),80℃时B的饱和溶液的密度为ρ g∙ml-1。
①80℃时,100g水做溶剂,达到饱和时,溶解的B的质量为
②80℃时,物质饱和溶液的物质的量浓度为
(2)某小组利用如图装置测定常温常压下的气体摩尔体积。取0.112g已去除氧化膜的铁片放入烧瓶中,调节量气管与水准管液面相平,再用注射器向烧瓶中注入10mL
 硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。
硫酸溶液,充分反应后冷却至室温,再次调节量气管与水准管液面相平,测得量气管中前后读数差为58mL。
计算:
①反应后溶液中c(H+)=
②计算常温常压下的气体摩尔体积
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某100mL的CuCl2溶液中,已知溶液中的Cl-的浓度为0.2 mol·L-1。现将一定量的铁粉投入到该溶液中,回答下列问题:
(1)原溶液中Cu2+的浓度为___________ ;
(2)反应后测得Cl-的浓度为___________ mol·L-1;
(3)若反应后测得Fe2+的溶液为0.05 mol·L-1,则反应生成铜单质的质量为______ g;
(4)剩余的Cu2+的浓度为_____________ 。
(1)原溶液中Cu2+的浓度为
(2)反应后测得Cl-的浓度为
(3)若反应后测得Fe2+的溶液为0.05 mol·L-1,则反应生成铜单质的质量为
(4)剩余的Cu2+的浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)相同质量的氢气、甲烷(CH4)、水,其中含分子数最多的是________ ;等物质的量的三种物质含氢原子最多的是________ 。
(2)某气体氧化物的化学式为RO2,在标准状况下,0.92 g该氧化物的体积为448 mL,则该氧化物的物质的量为______ ,该氧化物的摩尔质量为______ 。
(3)某化学兴趣小组对某品牌矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,Mg2+的物质的量浓度为______ 。
(4)现有0.1 mol·L-1 Na2SO4和0.3 mol·L-1 H2SO4的混合溶液100 mL,向其中逐滴加入0.2 mol·L-1的Ba(OH)2溶液,并不断搅拌,使反应充分进行。(忽略混合过程中的体积变化)
①当加入50 mL Ba(OH)2溶液时,所得溶液中SO42-离子的物质的量浓度为________ mol·L-1。
②当溶液中沉淀量达到最大时,所加Ba(OH)2溶液的体积为________ mL。
(2)某气体氧化物的化学式为RO2,在标准状况下,0.92 g该氧化物的体积为448 mL,则该氧化物的物质的量为
(3)某化学兴趣小组对某品牌矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,Mg2+的物质的量浓度为
(4)现有0.1 mol·L-1 Na2SO4和0.3 mol·L-1 H2SO4的混合溶液100 mL,向其中逐滴加入0.2 mol·L-1的Ba(OH)2溶液,并不断搅拌,使反应充分进行。(忽略混合过程中的体积变化)
①当加入50 mL Ba(OH)2溶液时,所得溶液中SO42-离子的物质的量浓度为
②当溶液中沉淀量达到最大时,所加Ba(OH)2溶液的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】按要求填空:
(1)有相同温度和压强下的两种气体12C18O和14N2,若两种气体的质量相同,则两种气体所含的质子数之比为__________ ,若两种气体的原子数相等,则两种气体所含中子数之比_________ ,若两种气体的体积相同,则两种气体的密度之比为_________ 。
(2)10.8 g R2O5中氧原子的数目为3.01×1023,则元素R的相对原子质量为________ 。
(3)将10 mL1.00 mol/L Na2CO3溶液与10 mL1.00 mol/L CaCl2溶液相混和,则混和溶液中Na+的物质的量浓度为___________ (忽略混合前后溶液体积的变化)。
(4)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是_________ 。
(5)在空气中煅烧CoC2O4生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为_______________ 。
(1)有相同温度和压强下的两种气体12C18O和14N2,若两种气体的质量相同,则两种气体所含的质子数之比为
(2)10.8 g R2O5中氧原子的数目为3.01×1023,则元素R的相对原子质量为
(3)将10 mL1.00 mol/L Na2CO3溶液与10 mL1.00 mol/L CaCl2溶液相混和,则混和溶液中Na+的物质的量浓度为
(4)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是
(5)在空气中煅烧CoC2O4生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)现有14.4gCO和CO2的混合气体,在标准状况下所占的体积约为8.96L,该混合气体的平均摩尔质量为________ 。
(2)将上述混合气体依次通过如图装置,最后收集在气球中。
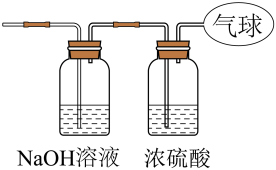
①标准状况下,气球中收集到的气体的体积为_________ 。
②气球中收集到的气体所含的电子总数为_________ 。(阿伏加德罗常数用NA表示)
(2)将上述混合气体依次通过如图装置,最后收集在气球中。

①标准状况下,气球中收集到的气体的体积为
②气球中收集到的气体所含的电子总数为
您最近一年使用:0次



