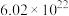名校
解题方法
1 . 请根据物质的量的相关概念及计算公式,完成下列各题:
(1)请填写下表:
(2)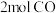 与
与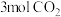 的质量之比
的质量之比__________ ;分子数之比为__________ ;含氧原子的数目之比为__________ 。
(3)将含杂质软锰矿粉末 与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得
与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得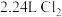 (标准状况下)。请回答下列问题:
(标准状况下)。请回答下列问题:
反应中被氧化的 的物质的量为
的物质的量为__________ mol,软锰矿中 的质量分数为
的质量分数为__________ 。
(1)请填写下表:
物质 | 摩尔质量 | 物质的量 | 质量 | 分子或离子数目 |
|
| |||
|
|
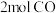 与
与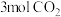 的质量之比
的质量之比(3)将含杂质软锰矿粉末
 与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得
与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得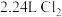 (标准状况下)。请回答下列问题:
(标准状况下)。请回答下列问题:反应中被氧化的
 的物质的量为
的物质的量为 的质量分数为
的质量分数为
您最近一年使用:0次
名校
2 . 计算
(1)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为_______ 。
(2)标准状况下,44.8L氯气通入足量NaOH溶液中,转移的电子数目为_______ 。
(3)标准状况下,甲烷和一氧化碳的混合气体共8.96 L,其质量为7.6 g,则混合气体中甲烷的物质的量为_______ 。
(4)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:称取m g样品放入烧杯内加水溶解,加入过量的氯化钙溶液充分反应,过滤、洗涤、干燥,称量沉淀的质量为n g。则样品中Na2CO3的质量分数为_______ 。
(1)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为
(2)标准状况下,44.8L氯气通入足量NaOH溶液中,转移的电子数目为
(3)标准状况下,甲烷和一氧化碳的混合气体共8.96 L,其质量为7.6 g,则混合气体中甲烷的物质的量为
(4)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:称取m g样品放入烧杯内加水溶解,加入过量的氯化钙溶液充分反应,过滤、洗涤、干燥,称量沉淀的质量为n g。则样品中Na2CO3的质量分数为
您最近一年使用:0次
名校
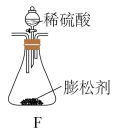
3 . 某食品膨松剂作用物质为 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
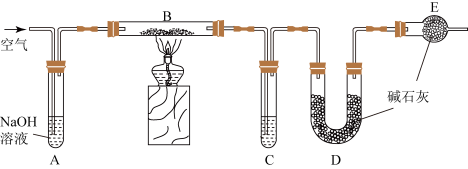
已知:碱石灰是固体氢氧化钠和氧化钙的混合物: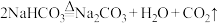 。
。
(1)A装置中 溶液的作用是除去空气中的
溶液的作用是除去空气中的________ ,C装置内所盛试剂是________ ,E装置的作用是________________________ ;
(2)若没有E装置,测定的结果________ (填“偏高”、“偏低”或“无影响”);若没有A装置,B装置左侧用橡皮塞封闭,实验结果将________ (填“偏高”、“偏低”或“无影响”)。
(3)取a克 与
与 混合物进行下列三组实验,其中能测定
混合物进行下列三组实验,其中能测定 质量分数的是
质量分数的是________ (填序号)。
A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氧化钙吸收,增重b克
 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。

已知:碱石灰是固体氢氧化钠和氧化钙的混合物:
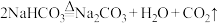 。
。(1)A装置中
 溶液的作用是除去空气中的
溶液的作用是除去空气中的(2)若没有E装置,测定的结果
(3)取a克
 与
与 混合物进行下列三组实验,其中能测定
混合物进行下列三组实验,其中能测定 质量分数的是
质量分数的是A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氧化钙吸收,增重b克
您最近一年使用:0次
名校
解题方法
4 . 将某碳酸钠和碳酸氢钠混合物2.43g加热到质量不再变化时,剩余物质的质量为2.12g,求:
(1)写出加热过程中发生反应的化学方程式_______ 。
(2)碳酸氢钠的质量为_______ 克?
(3)碳酸钠的质量分数为_______ (保留三位有效数字)?
(1)写出加热过程中发生反应的化学方程式
(2)碳酸氢钠的质量为
(3)碳酸钠的质量分数为
您最近一年使用:0次
2022-11-19更新
|
292次组卷
|
3卷引用:广东省汕尾华大实验学校2022-2023学年高一上学期12月月考化学试题
解题方法
5 . 现将2.3克的金属钠投入到过量水中,完全反应,按照下列要求进行计算(可能用到的相对原子质量:H—1,O—16,Na—23)
(1)生成的氢气质量为多少?___________
(2)若最终有100克溶液,此时氢氧化钠的质量分数为多少?___________
(1)生成的氢气质量为多少?
(2)若最终有100克溶液,此时氢氧化钠的质量分数为多少?
您最近一年使用:0次
名校
解题方法
6 . I.现有下列十种物质:①硫酸 ②石墨 ③纯碱 ④二氧化碳 ⑤葡萄糖 ⑥氨水 ⑦小苏打⑧NaOH溶液 ⑨Al2O3 ⑩硫酸铁溶液
上述十种物质中能导电的物质有___________ ,属于电解质的有___________ (填序号)。
Ⅱ.(1)14 g C2H4与C4H8的混合物所含质子的物质的量为___________ 。
(2)Cl﹣浓度为0.4mol•L﹣1的BaCl2溶液的物质的量浓度为___________ ,200mL该BaCl2溶液中含Ba2+的数目为___________ 。
(3)50mL质量分数为98%、密度为1.84g·cm-3的硫酸中,H2SO4的物质的量浓度为___________ 。
(4)3.1g Na2X含有Na+ 0.1 mol,则Na2X的摩尔质量为___________ ,X的相对原子质量为___________ 。
上述十种物质中能导电的物质有
Ⅱ.(1)14 g C2H4与C4H8的混合物所含质子的物质的量为
(2)Cl﹣浓度为0.4mol•L﹣1的BaCl2溶液的物质的量浓度为
(3)50mL质量分数为98%、密度为1.84g·cm-3的硫酸中,H2SO4的物质的量浓度为
(4)3.1g Na2X含有Na+ 0.1 mol,则Na2X的摩尔质量为
您最近一年使用:0次
名校
解题方法
7 . (1)某气态氧化物的化学式为RO2,在标准状况下,1.6g该氧化物的体积为560mL,则R的摩尔质量为_________ 。
(2)已知CO、SO2的混合气体质量共20.8g,标准状况下体积为8.96L,则可推知该混合气体的平均相对分子质量为__________ 。
(3)标准状况下9.03×1023个CH4所占的体积为________ ;与________ 个NH3含有相同数目的氢原子。
(4)与112gN2H4所含有分子数相同的氧气的体积(标准状况)是_________ L。
(5)质量比为85:28的NH3、CO所含质子数之比为_________ 。
(6)配制100ml 1mol/L的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g/ml,质量分数为98%)的体积为_____ mL.
(7)某常见气体在标准状况下的密度为1.25g/L,若该气体的分子式为A2型,则其名称是_____________ 。
(8)在27g某二价金属的氯化物中含有0.4mol,此氯化物的摩尔质量为_____ 。
(2)已知CO、SO2的混合气体质量共20.8g,标准状况下体积为8.96L,则可推知该混合气体的平均相对分子质量为
(3)标准状况下9.03×1023个CH4所占的体积为
(4)与112gN2H4所含有分子数相同的氧气的体积(标准状况)是
(5)质量比为85:28的NH3、CO所含质子数之比为
(6)配制100ml 1mol/L的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g/ml,质量分数为98%)的体积为
(7)某常见气体在标准状况下的密度为1.25g/L,若该气体的分子式为A2型,则其名称是
(8)在27g某二价金属的氯化物中含有0.4mol,此氯化物的摩尔质量为
您最近一年使用:0次
名校
8 . 1774年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。现将23.2g
MnCl2+Cl2↑+2H2O。现将23.2g
含MnO2的质量分数为75%的软锰矿石与足量10mol/L浓盐酸完全反应(杂质不参加反应)。把反应后所得溶液稀释成200ml。计算:
(1)参加反应的MnO2的质量____ 。
(2)生成的Cl2的体积(标准状况)____ 。
(3)稀释后溶液中MnCl2的物质的量浓度____ 。
 MnCl2+Cl2↑+2H2O。现将23.2g
MnCl2+Cl2↑+2H2O。现将23.2g含MnO2的质量分数为75%的软锰矿石与足量10mol/L浓盐酸完全反应(杂质不参加反应)。把反应后所得溶液稀释成200ml。计算:
(1)参加反应的MnO2的质量
(2)生成的Cl2的体积(标准状况)
(3)稀释后溶液中MnCl2的物质的量浓度
您最近一年使用:0次
2020-10-17更新
|
777次组卷
|
5卷引用:广东省大埔县虎山中学2018-2019学年高一上学期期中考试化学试题
解题方法
9 . 把11.1 g铝镁合金的粉末放入200 mL某盐酸中,恰好完全反应并得到11.2 L H2(标准状况下)。试计算:
(1) 上述反应过程中,转移电子的物质的量______ 。
(2) 该合金中铝的质量分数______ 。
(1) 上述反应过程中,转移电子的物质的量
(2) 该合金中铝的质量分数
您最近一年使用:0次
名校
10 . 如图为某品牌84消毒液的部分产品说明,完成下列问题
(1)该消毒液中c(Na+)浓度约为(保留整数)________ 。
(2)欲制取该品牌消毒液理论上需标准状况下的Cl2 L________ 。
| 84消毒液 (有效成分)NaClO (规格)1000 mL (质量分数)25% (密度)1.19 g·cm-3 |
(1)该消毒液中c(Na+)浓度约为(保留整数)
(2)欲制取该品牌消毒液理论上需标准状况下的Cl2 L
您最近一年使用:0次