1 . 随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
(1)把煤作为燃料可通过下列两种途径:

途径Ⅰ:C(s)+O2(g)=CO2(g)ΔH1<0①
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g)ΔH2>0②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g)ΔH3<0③
2H2(g)+O2(g)=2H2O(g)ΔH4<0④
则途径Ⅰ放出的热量___ (填“大于”“等于”或“小于”)途径Ⅱ放出的热量;ΔH1、ΔH2、ΔH3、ΔH4的数学关系式是___ 。
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用如下方法合成甲醇:
方法一CO(g)+2H2(g)⇌CH3OH(g)
方法二CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
在25℃、101kPa下,1克甲醇完全燃料放热22.68kJ,写出甲醇燃烧热的热化学方程式:___ 。
(3)金属钛冶炼过程中其中一步反应是将原料金红石转化:TiO2(金红石)+2C+2Cl2 TiCl4+2CO
TiCl4+2CO
已知:
C(s)+O2(g)=CO2(g)ΔH=-393.5kJ•mol-1
2CO(g)+O2(g)=2CO2(g)ΔH=-566kJ•mol-1
TiO2(s)+2Cl2(g)=TiCl(s)+O2(g)ΔH=+141kJ•mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=___ 。
(4)臭氧可用于净化空气、饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:6Ag(s)+O3(g)=3Ag2O(s)ΔH=-235.8kJ•mol-1
已知:2Ag2O(s)=4Ag(s)+O2(g)ΔH=+62.2kJ•mol-1则O3转化为O2的热化学方程式为___ 。
(1)把煤作为燃料可通过下列两种途径:

途径Ⅰ:C(s)+O2(g)=CO2(g)ΔH1<0①
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g)ΔH2>0②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g)ΔH3<0③
2H2(g)+O2(g)=2H2O(g)ΔH4<0④
则途径Ⅰ放出的热量
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用如下方法合成甲醇:
方法一CO(g)+2H2(g)⇌CH3OH(g)
方法二CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
在25℃、101kPa下,1克甲醇完全燃料放热22.68kJ,写出甲醇燃烧热的热化学方程式:
(3)金属钛冶炼过程中其中一步反应是将原料金红石转化:TiO2(金红石)+2C+2Cl2
 TiCl4+2CO
TiCl4+2CO已知:
C(s)+O2(g)=CO2(g)ΔH=-393.5kJ•mol-1
2CO(g)+O2(g)=2CO2(g)ΔH=-566kJ•mol-1
TiO2(s)+2Cl2(g)=TiCl(s)+O2(g)ΔH=+141kJ•mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
(4)臭氧可用于净化空气、饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:6Ag(s)+O3(g)=3Ag2O(s)ΔH=-235.8kJ•mol-1
已知:2Ag2O(s)=4Ag(s)+O2(g)ΔH=+62.2kJ•mol-1则O3转化为O2的热化学方程式为
您最近一年使用:0次
2020-11-06更新
|
293次组卷
|
2卷引用:广东省佛山市萌茵实验学校2019-2020学年高二上学期第一次月考化学(理)试题
13-14高三上·广东中山·期末
2 . (1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应化学方程式为:
C+ K2Cr2O7+ H2SO4 ═ CO2↑+ K2SO4+ Cr2(SO4)3+ H2O
请完成并配平上述化学方程式.其中氧化剂是 ,氧化产物是
(2)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+2H2(g)⇌CH3OH(g) △H1=﹣116kJ•mol﹣1
①已知:2CO(g)+O2(g)=2CO2(g) △H2=﹣566kJ•mol﹣1
2H2(g)+O2(g)=2H2O(g) △H3=﹣484kJ•mol﹣1
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为 ;
②在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律.如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系.请回答:
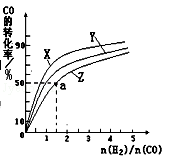
A)在上述三种温度中,曲线Z对应的温度是
B)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)⇌CH3OH(g)的平衡常数K= .(写明单位)
③在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol•L﹣1)变化如下表所示:
若5min~10min只改变了某一条件,所改变的条件是 ;且该条件所改变的量是 .
C+ K2Cr2O7+ H2SO4 ═ CO2↑+ K2SO4+ Cr2(SO4)3+ H2O
请完成并配平上述化学方程式.其中氧化剂是 ,氧化产物是
(2)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+2H2(g)⇌CH3OH(g) △H1=﹣116kJ•mol﹣1
①已知:2CO(g)+O2(g)=2CO2(g) △H2=﹣566kJ•mol﹣1
2H2(g)+O2(g)=2H2O(g) △H3=﹣484kJ•mol﹣1
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为 ;
②在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律.如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系.请回答:

A)在上述三种温度中,曲线Z对应的温度是
B)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)⇌CH3OH(g)的平衡常数K= .(写明单位)
③在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol•L﹣1)变化如下表所示:
| 0min | 5min | 10min | |
| CO | 0.1 | 0.05 | |
| H2 | 0.2 | 0.2 | |
| CH3OH | 0 | 0.04 | 0.05 |
若5min~10min只改变了某一条件,所改变的条件是 ;且该条件所改变的量是 .
您最近一年使用:0次



