2024高三·全国·专题练习
1 . 下列关于元素及其化合物的性质说法错误的是
| A.浓硫酸遇胆矾变“白”,体现了浓硫酸的吸水性 |
| B.硝酸见光受热易分解,一般保存在棕色试剂瓶中,放置在阴凉处 |
| C.燃油发动机产生的NO2、NO与CO反应能生成N2和CO2,因此可以直接排放 |
| D.铝制餐具不宜用来蒸煮或长时间存放酸性或者碱性食物 |
您最近半年使用:0次
解题方法
2 . 利用废镍催化剂(主要含金属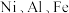 及其氧化物)合成硫酸镍晶体的一种工艺流程如下:
及其氧化物)合成硫酸镍晶体的一种工艺流程如下: 如表所示:
如表所示:
回答下列问题:
(1)“碱浸”时发生的主要反应的离子方程式为___________ 。
(2)“滤液②”中含有的金属离子是___________ 。
(3)若“转化”后的溶液中 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是___________ 。
(4)资料显示,硫酸镍结晶水合物的形态与温度有如下关系。
由 溶液获得稳定的
溶液获得稳定的 晶体的操作依次是蒸发浓缩、
晶体的操作依次是蒸发浓缩、___________ 、过滤、洗涤、干燥。
(5)①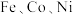 三种元素二价离子的硫酸盐晶体的晶胞类型相同,其熔点由高到低的顺序为
三种元素二价离子的硫酸盐晶体的晶胞类型相同,其熔点由高到低的顺序为___________ ;
② 中阴离子的空间构型为
中阴离子的空间构型为___________ ;
③丁二酮肟常用于检验 。在稀氨水中,丁二酮肟与
。在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示:
反应生成鲜红色沉淀,其结构如图所示: 的配位数为
的配位数为___________ ;丁二酮肟分子中所含的第二周期元素的第一电离能由大到小的顺序为___________ 。
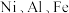 及其氧化物)合成硫酸镍晶体的一种工艺流程如下:
及其氧化物)合成硫酸镍晶体的一种工艺流程如下: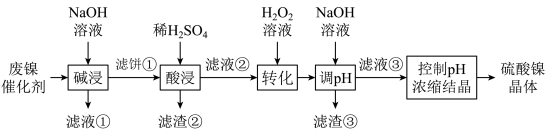
 如表所示:
如表所示:| 金属离子 |  |  |  |  |
开始沉淀时 的 的 | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时 的 的 | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”时发生的主要反应的离子方程式为
(2)“滤液②”中含有的金属离子是
(3)若“转化”后的溶液中
 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是(4)资料显示,硫酸镍结晶水合物的形态与温度有如下关系。
| 温度 | 低于30.8℃ | 30.8~53.8℃ | 53.8~280℃ | 高于280℃ |
| 晶体形态 |  |  | 多种结晶水合物 |  |
 溶液获得稳定的
溶液获得稳定的 晶体的操作依次是蒸发浓缩、
晶体的操作依次是蒸发浓缩、(5)①
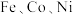 三种元素二价离子的硫酸盐晶体的晶胞类型相同,其熔点由高到低的顺序为
三种元素二价离子的硫酸盐晶体的晶胞类型相同,其熔点由高到低的顺序为②
 中阴离子的空间构型为
中阴离子的空间构型为③丁二酮肟常用于检验
 。在稀氨水中,丁二酮肟与
。在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示:
反应生成鲜红色沉淀,其结构如图所示: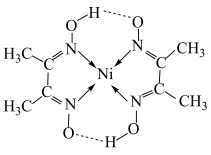
 的配位数为
的配位数为
您最近半年使用:0次
3 . 下列劳动项目与所述的化学知识没有关联的是
选项 | 劳动项目 | 化学知识 |
A | 用氢氟酸刻蚀玻璃器皿 | 氢氟酸是弱酸 |
B | 用草木灰对农作物施肥 | 草木灰含有钾元素 |
C | 利用铝热反应焊接钢轨 | 高温下铝能还原氧化铁 |
D | 将锌块镶嵌在轮船底部防腐 | 锌的金属性比铁强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
4 . 下列物质及其变化与对应的方程式不匹配的是
A.工业上用 处理废水中的 处理废水中的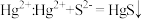 |
B.用 与水反应制备 与水反应制备 |
C.用铝粉和 溶液反应制取少量 溶液反应制取少量 |
D.用 溶液检测溶液中的 溶液检测溶液中的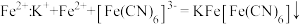 |
您最近半年使用:0次
名校
解题方法
5 . 下列离子组在指定条件下能大量共存的是
A.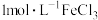 溶液中: 溶液中: 、 、 、 、 、 、 |
B.使酚酞变红的溶液中: 、 、 、 、 、 、 |
C.久置氯水中: 、 、 、 、 、 、 |
D.加入铝粉有气体生成的溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
解题方法
6 . 铝是典型的两性金属,既能与酸反应,又能与强碱溶液反应。回答下列问题:
(1)在铝分别与盐酸和氢氧化钠溶液的反应中,铝元素化合价的变化都是___________ (升高/降低),还原剂都是___________ 。
(2)1mol的铝分别与足量的稀盐酸和氢氧化钠溶液反应,生成氢气的体积在相同状况下比值为___________ ,消耗氯化氢和氢氧化钠的物质的量之比为___________ 。
甲、乙两个烧杯中分别盛有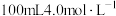 的盐酸和
的盐酸和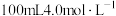 氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为___________ 。反应中消耗的NaOH与HCl的物质的量之比为___________ 。
(1)在铝分别与盐酸和氢氧化钠溶液的反应中,铝元素化合价的变化都是
(2)1mol的铝分别与足量的稀盐酸和氢氧化钠溶液反应,生成氢气的体积在相同状况下比值为
甲、乙两个烧杯中分别盛有
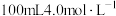 的盐酸和
的盐酸和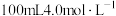 氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
您最近半年使用:0次
解题方法
7 . 取两份铝片,分别加入足量的硫酸溶液和氢氧化钠溶液,产生气体的物质的量相同,下列有关说法正确的是
| A.产生气体成分不相同 | B.反应的离子方程式相同 |
| C.参加反应的铝片的质量相同 | D.消耗的硫酸和氢氧化钠的物质的量相同 |
您最近半年使用:0次
解题方法
8 . 下列离子在溶液中一定能大量共存的是
A.无色溶液中: 、 、 、 、 |
B.酸性溶液中: 、 、 、 、 |
C.加入 粉产生 粉产生 的溶液中: 的溶液中: 、 、 、 、 |
D.加入酚酞变红的溶液中: 、 、 、 、 |
您最近半年使用:0次
名校
9 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离出的c(H+)=1.0×10-13mol/L的溶液中:Na+、 、Cl-、 、Cl-、 |
B.与Al反应放出H2的溶液:Mg2+、Cu2+、 、 、 |
C.加入少量KSCN后变为红色的溶液中:K+、Mg2+、I-、 |
D.无色透明的溶液中:CH3COO-、 、K+、Na+ 、K+、Na+ |
您最近半年使用:0次
名校
10 . 下列实验目的、实验操作及现象与对应结论都正确的是
选项 | 实验目的 | 实验操作及现象 | 结论 |
A | 检验蔗糖是否水解 | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 ,无砖红色沉淀 ,无砖红色沉淀 | 蔗糖未发生水解 |
B | 探究镁和铝的金属活泼性 | 向盛有浓 溶液的两支试管中分别加入除去氧化膜的镁带和铝片,加入镁带的试管中迅速产生红棕色气体,加入铝片试管中无明显现象 溶液的两支试管中分别加入除去氧化膜的镁带和铝片,加入镁带的试管中迅速产生红棕色气体,加入铝片试管中无明显现象 | 金属活泼性: 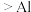 |
C | 探究氢离子浓度对 、 、 相互转化的影响 相互转化的影响 | 向 溶液中缓慢滴加浓硫酸,溶液黄色变为橙红色 溶液中缓慢滴加浓硫酸,溶液黄色变为橙红色 | 增大氢离子浓度,平衡向生成 的方向移动 的方向移动 |
D | 探究在相同条件下 和 和 的溶解度大小 的溶解度大小 | 向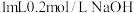 溶液中滴入2滴 溶液中滴入2滴 溶液,产生白色沉淀后,再滴加2滴 溶液,产生白色沉淀后,再滴加2滴 溶液,又生成红褐色沉淀 溶液,又生成红褐色沉淀 | 证明在相同条件下,溶解度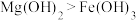 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



