1 . 下列说法不正确 的是
| A.石墨烯可看作单层石墨,其电阻率低、热导性高,可用于生产电池、光电器件 |
B.储氢合金是一类能够大量吸收 ,并与 ,并与 结合成金属氢化物的材料 结合成金属氢化物的材料 |
| C.铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物 |
| D.二氧化硅可以制成计算机的芯片和硅太阳能电池 |
您最近一年使用:0次
2023-08-20更新
|
301次组卷
|
2卷引用:浙江省Z20名校联盟(浙江省名校新高考研究联盟)2023届高三上学期第二次联考化学试题
2 . 下列离子方程式书写正确的是
A.向稀 中滴加少量 中滴加少量 溶液: 溶液: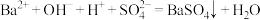 |
B.向 中滴加稀盐酸: 中滴加稀盐酸: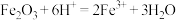 |
C.向 溶液中通入过量 溶液中通入过量 : : |
D.将打磨后的铝片放入NaOH溶液: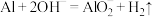 |
您最近一年使用:0次
名校
3 . 回答下列问题:
Ⅰ.有以下物质①石墨;②铝;③酒精;④二氧化硫;⑤液态氯化氢;⑥碳酸氢钠固体;⑦氢氧化钠溶液。
(1)其中能导电的是___________ ;属于非电解质的是___________ 。
(2)写出⑥在水溶液中的电离方程式___________ 。
(3)写出②与⑦反应的化学方程式___________ 。
Ⅱ.双碱法脱硫过程如下图所示。
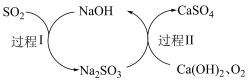
(4)过程Ⅰ的离子方程式是___________ 。
(5)双碱法脱硫过程中,循环利用的物质是___________ (填化学式)。
Ⅰ.有以下物质①石墨;②铝;③酒精;④二氧化硫;⑤液态氯化氢;⑥碳酸氢钠固体;⑦氢氧化钠溶液。
(1)其中能导电的是
(2)写出⑥在水溶液中的电离方程式
(3)写出②与⑦反应的化学方程式
Ⅱ.双碱法脱硫过程如下图所示。

(4)过程Ⅰ的离子方程式是
(5)双碱法脱硫过程中,循环利用的物质是
您最近一年使用:0次
名校
4 . 下列溶液中一定能大量共存的离子组是
A.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.在 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.能与 反应产生 反应产生 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.使无色酚酞溶液变红的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2023-08-20更新
|
264次组卷
|
3卷引用:江西省赣州教育发展联盟2022-2023学年高一上学期12月月考化学试题
名校
解题方法
5 . 一定质量的钠铝合金投入水中,充分反应后测得产生4 mol气体且固体有剩余,将相同质量的钠铝合金投入足量氢氧化钠溶液中,充分反应后产生5.5 mol气体,下列正确的是
| A.铝的质量为81 g | B.钠和铝的质量比为23:27 |
| C.剩余固体的物质的量为1.5 mol | D.两次实验中转移电子数之比为8:11 |
您最近一年使用:0次
6 . 下列金属冶炼的方程式(未配平)错误的是
A. | B. |
C.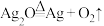 | D. |
您最近一年使用:0次
2023高三·全国·专题练习
7 . 工业上,金属的制取有多种方法,选择何种方法与金属的性质密切相关。
(1)金属Na、Mg、Al等的制取常采用电解法。写出以铂为电极电解熔融氯化镁制镁的电极反应式。
阳极___________ ;阴极___________ 。
(2)金属钾因为易溶于盐而不易分离,且电解时有副反应发生,工业上通常用钠与氯化钾在高温下反应制取,该反应为:Na(l)+KCl(l) NaCl(l)+K(g);ΔH>0,根据下表有关数据回答下列问题:
NaCl(l)+K(g);ΔH>0,根据下表有关数据回答下列问题:
①制取钾的适宜温度范围为___________ 。
②制取钾的条件为___________ 。
A.适当高温高压 B.适当低温低压 C.适当高温低压 D.适当低温高压
③工业上采用此法制得的钾往往不纯,最可能含有的杂质是___________ ,检验方法为___________ 。
(3)用铝热反应方法将Fe3O4中的铁还原出来,写出该反应的化学方程式:__________ ,若用此法制得0.84t Fe,则转移电子___________ mol。
(1)金属Na、Mg、Al等的制取常采用电解法。写出以铂为电极电解熔融氯化镁制镁的电极反应式。
阳极
(2)金属钾因为易溶于盐而不易分离,且电解时有副反应发生,工业上通常用钠与氯化钾在高温下反应制取,该反应为:Na(l)+KCl(l)
 NaCl(l)+K(g);ΔH>0,根据下表有关数据回答下列问题:
NaCl(l)+K(g);ΔH>0,根据下表有关数据回答下列问题:| 物质 | 密度(g/cm3) | 熔点(℃) | 沸点(℃) |
| Na | 0.97 | 97.81 | 890 |
| K | 0.86 | 63.65 | 770 |
| NaCl | 801 | 1465 | |
| KCl | 776 | 1437 |
①制取钾的适宜温度范围为
②制取钾的条件为
A.适当高温高压 B.适当低温低压 C.适当高温低压 D.适当低温高压
③工业上采用此法制得的钾往往不纯,最可能含有的杂质是
(3)用铝热反应方法将Fe3O4中的铁还原出来,写出该反应的化学方程式:
您最近一年使用:0次
名校
8 . 某同学按图示装置进行实验,大头针固定固体,塑料瓶盛放液体试剂。实验时先打开止水夹,手指压紧小孔并挤压塑料瓶,使液体试剂沿玻璃管上升至完全充满,排尽玻璃管中空气,立即关闭止水夹,一会儿后,手指堵住小孔,打开止水夹。下列所加液体试剂、对应现象及结论均正确的是


| 选项 | 固体 | 液体试剂 | 现象 | 结论 |
| A | 钠块 | 水 | 钠块熔化成小球并浮在水面上;打开止水夹,点燃气体,火焰呈淡蓝色 | 钠块与水反应产生氢气 |
| B | 铝条 |  溶液 溶液 | 先有沉淀生成,后沉淀溶解;打开止水夹,点燃气体,火焰呈淡蓝色 | 铝条与氢氧化钠溶液反应产生氢气 |
| C | 铜丝 | 稀 | 产生红棕色气体,溶液呈蓝色 | 铜丝与稀硝酸反应产生 |
| D | 铁丝 | 食盐水 | 打开止水夹,并松开小孔片刻,关闭止水夹,发现塑料瓶中液面下降 | 铁丝发生了析氢腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-19更新
|
720次组卷
|
3卷引用:辽宁省大连市第八中学2023届高三高考适应性测试化学试题
2023高三·全国·专题练习
9 . JerryWoodall教授经研究发现,含有95%的铝和5%的镓、铟及锡组成的新型合金与水能快速反应制得氢气,由于整个反应中,只消耗铝,而反应生成的Al2O3可回收再利用,这样不仅降低了制氢气的成本,而且方便快捷,这一发现将燃氢汽车的研发推向新的里程碑。据此,下列说法不正确的是
| A.铝作为燃料,有资源丰富的优势 |
| B.组成合金的几种金属元素都位于周期表第ⅢA族 |
| C.合金与水反应的总反应式为:2Al+3H2O=Al2O3+3H2↑ |
| D.合金中的镓、铟及锡对铝与水的反应起到催化作用 |
您最近一年使用:0次
名校
解题方法
10 . 下列除去杂质的方法不正确的是
| A.用过量铜除去 Cu2+溶液中的 Fe3+ |
| B.Na2CO3 中混有少量NaHCO3:加热灼烧至恒重 |
| C.干燥的 CO2 气体中混有少量 O2:通过灼热的铜网 |
| D.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 |
您最近一年使用:0次



