一定质量的钠铝合金投入水中,充分反应后测得产生4 mol气体且固体有剩余,将相同质量的钠铝合金投入足量氢氧化钠溶液中,充分反应后产生5.5 mol气体,下列正确的是
| A.铝的质量为81 g | B.钠和铝的质量比为23:27 |
| C.剩余固体的物质的量为1.5 mol | D.两次实验中转移电子数之比为8:11 |
更新时间:2023-08-20 14:48:19
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】有一种不纯的K2CO3固体,可能含有Na2CO3、MgCO3、CuSO4、NaCl中的一种或几种。取该样品13.8g加入100g稀盐酸,恰好完全反应得到无色溶液,同时产生气体4.4g。下列判断正确的是
| A.完全反应得到无色溶液,样品中一定没有CuSO4 |
| B.NaCl不与盐酸反应,样品中一定没有NaCl |
| C.所加稀盐酸中溶质的质量分数为7.3% |
| D.根据产生气体的量分析,样品中Na2CO3和MgCO3不可能同时存在 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】Mg、Al组成的混合物与足量盐酸反应,产生标准状况下的氢气4.48 L,下列推断中不正确 的是
| A.参加反应的Mg、Al共0.2 mol |
| B.参加反应的HCl为0.4 mol |
| C.Mg、Al与盐酸的反应属于氧化还原反应 |
| D.若与足量的稀硫酸反应能产生0.4 mol H2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛。水热法制备Fe3O4磁性纳米颗粒的反应是 。下列叙述不正确的是
。下列叙述不正确的是
 。下列叙述不正确的是
。下列叙述不正确的是A.水热法制备Fe3O4磁性纳米颗粒的反应中,还原剂是 、 、 |
| B.离子方程式中x4 |
| C.生成水分子和转移电子总数之间的关系为1:1 |
| D.将制得的Fe3O4颗粒均匀分散在水中能产生丁达尔效应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】测定某溶液中甲醇含量的部分过程如下:
①碱性 溶液处理:CH3OH+MnO
溶液处理:CH3OH+MnO +OH-→CO
+OH-→CO +MnO
+MnO +H2O (末配平,下同)
+H2O (末配平,下同)
②酸化处理:MnO +H+→MnO2↓+ MnO
+H+→MnO2↓+ MnO +H2O
+H2O
下列说法错误的是
①碱性
 溶液处理:CH3OH+MnO
溶液处理:CH3OH+MnO +OH-→CO
+OH-→CO +MnO
+MnO +H2O (末配平,下同)
+H2O (末配平,下同)②酸化处理:MnO
 +H+→MnO2↓+ MnO
+H+→MnO2↓+ MnO +H2O
+H2O下列说法错误的是
A.“反应①”中氧化剂与还原剂的物质的量之比为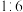 |
B.“反应①”中氧化性:MnO > CO > CO |
| C.“反应②”中,可用硫酸进行酸化 |
D.“反应②”消耗59.5g MnO 时,反应中转移0.5mole- 时,反应中转移0.5mole- |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】反应①是自海藻灰中提取碘的主要反应,反应②是自智利硝石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4→2NaHSO4+MnSO4+2H2O+I2;
②2NaIO3+5NaHSO3→2Na2SO4+3NaHSO4+H2O+I2
下列有关说法正确的是( )
①2NaI+MnO2+3H2SO4→2NaHSO4+MnSO4+2H2O+I2;
②2NaIO3+5NaHSO3→2Na2SO4+3NaHSO4+H2O+I2
下列有关说法正确的是( )
| A.NaI和NaIO3在一定条件下能反应生成I2 |
| B.I2在反应①中是还原产物,在反应②中是氧化产物 |
| C.两个反应中生成等量的I2时转移的电子数为1:5 |
D.氧化性:MnO2>IO >I2>SO >I2>SO >Mn2+ >Mn2+ |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】向分别盛有100mL水、100mL0.1mol·L-1盐酸、100mL0.01mol·L-1NaOH溶液的X、Y、Z三个烧杯中各投入0.05molNa.下列有关说法正确的是
| A.三个烧杯中发生的离子反应均为2Na+2H2O=2Na++2OH-+H2↑ |
| B.三个烧杯中钠均在液面上剧烈反应,且Y烧杯中反应最剧烈 |
| C.反应后,三个烧杯中NaOH的物质的量浓度相同 |
| D.反应后,三个烧杯中生成的气体的质量一定相同 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】将等物质的量的金属Na、Mg、Al分别与100mL2mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是
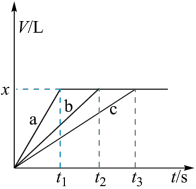

| A.x=2.24 |
| B.曲线c为Mg与盐酸反应的图像 |
| C.反应时,Na、Mg、Al均过量 |
| D.钠的物质的量为0.2mol |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子二次电池正极铝钴膜主要含有LiCoO2、A1等,处理该废料的一种工艺如下图所示,下列说法正确的是
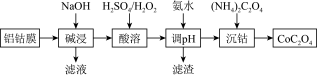

| A.酸溶时H2O2做氧化剂,且温度不宜过高 |
| B.加氨水调pH的目的是除铝 |
| C.沉钴的离子方程式为:Co2++C2O42-=CoC2O4↓ |
| D.在空气中加热4.41gCoC2O4得到钴的氧化物2.41g,则该氧化物的化学式为Co3O4 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列除杂试剂的选择及除杂操作均正确的是(括号内为杂质)
| 选项 | 物质 | 除杂试剂 | 除杂操作 |
| A | Al(Fe) | NaOH溶液 | 加入过量NaOH溶液并过滤 |
| B | NO( ) ) | 水、浓硫酸 | 将气体依次通过装有水和浓硫酸的洗气瓶 |
| C |  溶液( 溶液( ) ) | Zn | 加入过量的锌粉,充分反应后过滤 |
| D |  固体(KCl固体) 固体(KCl固体) | 蒸馏水 | 溶解、过滤、洗涤、干燥 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次





