解题方法
1 . 工业上常以铝土矿为原料来冶炼金属铝。已知:铝土矿的主要成分是 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:
①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。___________ 。
(2)最后所得不溶于NaOH溶液的沉淀的化学式为___________ ,其物质的量为___________ 。
(3)该铝土矿样中 的质量分数为
的质量分数为___________ 。
 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入
 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。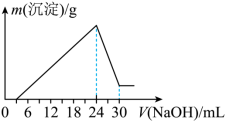
(2)最后所得不溶于NaOH溶液的沉淀的化学式为
(3)该铝土矿样中
 的质量分数为
的质量分数为
您最近一年使用:0次
解题方法
2 . 将18g铁铝合金投入足量NaOH溶液中,完全反应后生成2.24L氢气(标准状况),请计算此铁铝合金中铝的质量分数。(假设合金中其他成分不与NaOH反应)_______
您最近一年使用:0次
3 . 要冶炼出纯度为98%的生铁4800t,至少需要含氧化铁(Fe2O3)质量分数为80%的赤铁矿_______ 吨。
您最近一年使用:0次
名校
4 . 有一块表面已被氧化为 的钠块10.8g,将其投入100mL水中,产生标准状况下2.24L气体(溶液体积的变化可以忽略不计)。
的钠块10.8g,将其投入100mL水中,产生标准状况下2.24L气体(溶液体积的变化可以忽略不计)。
(1)这块钠块中所含单质钠的质量分数是多少__________ ?
(2)所得溶液中溶质的物质的量浓度为多少__________ ?
 的钠块10.8g,将其投入100mL水中,产生标准状况下2.24L气体(溶液体积的变化可以忽略不计)。
的钠块10.8g,将其投入100mL水中,产生标准状况下2.24L气体(溶液体积的变化可以忽略不计)。(1)这块钠块中所含单质钠的质量分数是多少
(2)所得溶液中溶质的物质的量浓度为多少
您最近一年使用:0次
5 . 把13.4g镁铝铜合金的粉末加入过量的盐酸中,在标准状况下放出氢气11.2L,反应后过滤得沉淀3.2g。试计算:
(1)该合金中镁的质量分数(保留小数点后一位数);___________
(2)该合金中镁、铝、铜的物质的量之比。___________
(1)该合金中镁的质量分数(保留小数点后一位数);
(2)该合金中镁、铝、铜的物质的量之比。
您最近一年使用:0次
6 . 在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol·L-1,请填写下列空白:
xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol·L-1,请填写下列空白:
(1)x值等于______ ;
(2)A的转化率为_____ ;
(3)生成D的反应速率为______ ;
(4)如果增大反应体系的压强,则平衡体系中C的质量分数____ (增大、减小、不变)
(5)写出该反应的平衡常数表达式____ ,并计算在该温度下的平衡常数为_____ 。
 xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol·L-1,请填写下列空白:
xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol·L-1,请填写下列空白:(1)x值等于
(2)A的转化率为
(3)生成D的反应速率为
(4)如果增大反应体系的压强,则平衡体系中C的质量分数
(5)写出该反应的平衡常数表达式
您最近一年使用:0次
名校
7 . 将一块质量为10.8g表面已被氧化的金属钠投入100g水中,产生0.20g气体,求:
①氧化钠的质量_______ ;
②所得溶液的质量分数_______ (请写出计算过程)
①氧化钠的质量
②所得溶液的质量分数
您最近一年使用:0次
2020-09-30更新
|
115次组卷
|
2卷引用:山西省运城市景胜中学2020-2021学年高一9月月考化学试题
名校
8 . 将24.4gNaOH固体溶于水,配成100mL溶液,其密度为1.22g/mL,请回答下列问题。
(1)从该溶液中取出10mL,其中NaOH的物质的量浓度为________ ,NaOH的质量分数为___________ ,溶液的密度为________ ,含NaOH的物质的量为_________ ;将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为_______ 。
(2)用等体积的0.2mol·Lˉ1的BaCl2溶液,可使相同体积的Na2SO4、KAl(SO4)2、Fe2(SO4)3三种溶液中的SO42ˉ完全沉淀,则三种硫酸盐的物质的量浓度之比为____ 。
(1)从该溶液中取出10mL,其中NaOH的物质的量浓度为
(2)用等体积的0.2mol·Lˉ1的BaCl2溶液,可使相同体积的Na2SO4、KAl(SO4)2、Fe2(SO4)3三种溶液中的SO42ˉ完全沉淀,则三种硫酸盐的物质的量浓度之比为
您最近一年使用:0次
9 . (1)从1L1mol/LNaOH溶液中取出100mL,则这100mLNaOH溶液的物质的量浓度是____ mol/L,含NaOH的质量____ g。
(2)某同学将标准状况下44.8L的HCl气体溶于水,配成500mL的溶液,该HCl气体的物质的量为______ ,可知所配成的盐酸溶液的物质的量浓度为_____ 。
(3)在标准状况下15gCO与CO2的混合气体,体积为11.2L。则:
①混合气体的密度是_____ 。
②混合气体的平均摩尔质量是______ 。
③CO2和CO的体积之比是_______ 。
④CO的体积分数是______ 。
⑤CO2和CO的质量之比是_______ 。
⑥CO的质量分数是______ 。
⑦混合气体中所含氧原子的物质的量是_____ 。
(2)某同学将标准状况下44.8L的HCl气体溶于水,配成500mL的溶液,该HCl气体的物质的量为
(3)在标准状况下15gCO与CO2的混合气体,体积为11.2L。则:
①混合气体的密度是
②混合气体的平均摩尔质量是
③CO2和CO的体积之比是
④CO的体积分数是
⑤CO2和CO的质量之比是
⑥CO的质量分数是
⑦混合气体中所含氧原子的物质的量是
您最近一年使用:0次
2019-06-13更新
|
550次组卷
|
2卷引用:山西省运城市空港新区一中2019-2020学年高一9月月考化学试题
10 . 将24.4gNaOH固体溶于水配成100 mL溶液,其密度为1.219g/mL。
(1)该溶液中NaOH的物质的量浓度为____ 。
(2)该溶液中 NaOH的质量分数为___ 。
(3)从该溶液中取出10mL,其中NaOH的物质的量浓度为____ ,NaOH的质量分数为____ ,含NaOH的质量为___ ,含NaOH的物质的量为___ 。
(4)将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为___ 。
(1)该溶液中NaOH的物质的量浓度为
(2)该溶液中 NaOH的质量分数为
(3)从该溶液中取出10mL,其中NaOH的物质的量浓度为
(4)将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为
您最近一年使用:0次



