解题方法
1 . 食品包装中的铁系脱氧剂由还原铁粉、氯化钠和炭粉等组成,利用铁的吸氧腐蚀除去氧气,主要反应有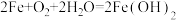 ,
,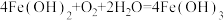 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:
(1)还原铁粉的物质的量是_______ mol。
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是_______ mol。
(3)在25 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理_______ mL包装盒中的空气。
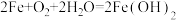 ,
,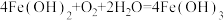 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:(1)还原铁粉的物质的量是
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是
(3)在25
 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
您最近一年使用:0次
名校
解题方法
2 . 把1L 1.0mol/L 溶液和1L 1.0mol/L
溶液和1L 1.0mol/L 溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:
溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:
(1)溶液混合前 的物质的量是
的物质的量是___________ mol。
(2)反应后 的物质的量浓度是
的物质的量浓度是___________ mol/L。
(3)反应中消耗铁粉的质量是___________ g。
 溶液和1L 1.0mol/L
溶液和1L 1.0mol/L 溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:
溶液混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,经过足量的时间,铁粉有剩余。请计算:(1)溶液混合前
 的物质的量是
的物质的量是(2)反应后
 的物质的量浓度是
的物质的量浓度是(3)反应中消耗铁粉的质量是
您最近一年使用:0次
解题方法
3 . 现有一份部分被氧化的铜片(氧化产物为CuO),称取4.32g铜片,溶于一定体积1.00mol•L-1稀硝酸中,反应恰好完全进行,收集到无色气体448mL(已折算为标准状况)。
(1)该稀硝酸中所含HNO3的物质的量为___________ ;
(2)该铜片被氧化的百分数为___________ 。
(1)该稀硝酸中所含HNO3的物质的量为
(2)该铜片被氧化的百分数为
您最近一年使用:0次
4 . 某 样品露置在空气中部分变质生成
样品露置在空气中部分变质生成 ,为确定其中
,为确定其中 和
和 的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸
的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸 ,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
(1)样品中物质的量之比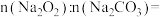
___________ 。
(2)盐酸的物质的量浓度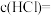
___________ 。
 样品露置在空气中部分变质生成
样品露置在空气中部分变质生成 ,为确定其中
,为确定其中 和
和 的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸
的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸 ,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 盐酸体积/mL | 100.0 | 100.0 | 100.0 | 100.0 |
| 样品质量/g | 2.62 | 3.93 | 5.24 | 6.55 |
| 气体总体积/mL | 448 | 560 | 448 | 560 |
(1)样品中物质的量之比
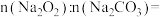
(2)盐酸的物质的量浓度
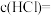
您最近一年使用:0次
5 . 实验室一瓶硫酸亚铁和硫酸铁混合物,取一定量样品溶于水,配成100mL溶液。所得溶液分成二份,在第一份溶液中加入0.5mol·Lˉ1氯化钡220mL恰好完全反应;在第二份溶液中通入标准状况下的氯气0.896L,可使Fe2+全部变成Fe3+。
(1)所取样品中硫酸铁物质的量是
(2)若在第一份溶液完全反应后所得溶液中再加入足量氢氧化钠溶液,所得沉淀经洗涤,在空气中充分灼烧,最后残渣的质量是
您最近一年使用:0次
6 . 在100mL稀盐酸中加入混合均匀的 和
和 固体粉末,充分反应后使气体全部逸出。下图是加入粉末的质量与产生
固体粉末,充分反应后使气体全部逸出。下图是加入粉末的质量与产生 (该状况下,气体的密度为
(该状况下,气体的密度为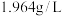 )体积的关系。请计算:
)体积的关系。请计算:
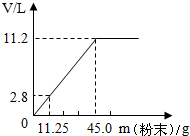
(1)该盐酸中HCl的质量为___________ 。
(2)若该盐酸为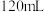 时,加入粉末为
时,加入粉末为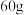 ,产生
,产生 的体积为
的体积为___________ 。
(3)若粉末的质量为 ,该盐酸的体积为
,该盐酸的体积为 ,产生的
,产生的 体积为
体积为 。试写出粉末质量
。试写出粉末质量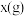 与产生
与产生 体积
体积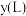 之间的关系:
之间的关系:___________ 。
 和
和 固体粉末,充分反应后使气体全部逸出。下图是加入粉末的质量与产生
固体粉末,充分反应后使气体全部逸出。下图是加入粉末的质量与产生 (该状况下,气体的密度为
(该状况下,气体的密度为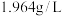 )体积的关系。请计算:
)体积的关系。请计算:
(1)该盐酸中HCl的质量为
(2)若该盐酸为
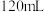 时,加入粉末为
时,加入粉末为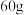 ,产生
,产生 的体积为
的体积为(3)若粉末的质量为
 ,该盐酸的体积为
,该盐酸的体积为 ,产生的
,产生的 体积为
体积为 。试写出粉末质量
。试写出粉末质量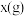 与产生
与产生 体积
体积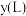 之间的关系:
之间的关系:
您最近一年使用:0次
解题方法
7 . “孤蓬自振”学习小组向一定质量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol/L的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,溶液体积仍为100mL,所得溶液中滴加几滴KSCN溶液,溶液未显红色。请回答:
(1)加盐酸后所得溶液的溶质是______ (填化学式),物质的量浓度是______ mol/L。
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是______ g。
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=______ 。
(1)加盐酸后所得溶液的溶质是
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=
您最近一年使用:0次
解题方法
8 . 3.20 g部分被氧化的镁条和100 mL的某浓度的盐酸恰好完全反应,生成标准状况下的氢气2.24 L。
(1)H2的物质的量是___________ mol。
(2)盐酸的浓度为___________ mol/L。
(3)被氧化之前镁条的质量是___________ g。
(1)H2的物质的量是
(2)盐酸的浓度为
(3)被氧化之前镁条的质量是
您最近一年使用:0次
9 . 现有Na2CO3和NaHCO3的混合物共48.6g,加入足量盐酸时放出11.2L(标准状况)CO2,请求出:
(1)产生二氧化碳的物质的量是___________ ;
(2)混合物中Na2CO3和NaHCO3的物质的量之比为___________ 。
(1)产生二氧化碳的物质的量是
(2)混合物中Na2CO3和NaHCO3的物质的量之比为
您最近一年使用:0次
10 . 在标准状况下,8.96LH2和O2的混合气体共9.8g,求混合气体中H2和O2的物质的量之比是_______ 。
您最近一年使用:0次



