解题方法
1 . 将 和
和 混合物29.6g,充分加热到固体质量不再发生变化后,收集到
混合物29.6g,充分加热到固体质量不再发生变化后,收集到 1.12L(标准状况),冷却后将剩余固体溶于水配成500mL溶液,求:
1.12L(标准状况),冷却后将剩余固体溶于水配成500mL溶液,求:
(1) 的物质的量为
的物质的量为___________ 。
(2)原混合物中 的质量为
的质量为___________ 。
(3)配制的溶液的物质的量浓度为___________ 。
 和
和 混合物29.6g,充分加热到固体质量不再发生变化后,收集到
混合物29.6g,充分加热到固体质量不再发生变化后,收集到 1.12L(标准状况),冷却后将剩余固体溶于水配成500mL溶液,求:
1.12L(标准状况),冷却后将剩余固体溶于水配成500mL溶液,求:(1)
 的物质的量为
的物质的量为(2)原混合物中
 的质量为
的质量为(3)配制的溶液的物质的量浓度为
您最近一年使用:0次
名校
解题方法
2 . 将一块质量为 表面(常温时)已被氧化的金属钠投入
表面(常温时)已被氧化的金属钠投入 水中,产生
水中,产生 气体,计算:
气体,计算:
(1)氧化钠的质量___________ g;
(2)所得溶液的质量分数___________ 。
 表面(常温时)已被氧化的金属钠投入
表面(常温时)已被氧化的金属钠投入 水中,产生
水中,产生 气体,计算:
气体,计算:(1)氧化钠的质量
(2)所得溶液的质量分数
您最近一年使用:0次
3 . 某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐渐加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量的变化关系如图所示。请计算:

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量_______ g。
(2)反应至A点时,溶液中钠元素的质量是_______ g。

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量
(2)反应至A点时,溶液中钠元素的质量是
您最近一年使用:0次
名校
解题方法
4 . 取30.0 g牛奶样品,将所含蛋白质中的氮元素全部转化为氨,用25.00 mL 1. 00 mol/L的硫酸将其完全吸收,再加入19.00mL2.00 mol/L氢氧化钠溶液恰好生成硫酸钠和硫酸铵。请计算:
(1)样品中蛋白质转化生成的氨的物质的量为_______ mol。
(2)样品蛋白质中含氮元素的质量_______ g。
(3)若蛋白质中氮元素的质量分数为14.0%,则样品中蛋白质的质量分数为_______ 。
(1)样品中蛋白质转化生成的氨的物质的量为
(2)样品蛋白质中含氮元素的质量
(3)若蛋白质中氮元素的质量分数为14.0%,则样品中蛋白质的质量分数为
您最近一年使用:0次
名校
5 . 据部分键能数据,以及热化学方程式 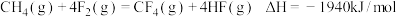 ,计算
,计算  键的键能为
键的键能为_______ 。
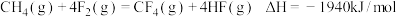 ,计算
,计算  键的键能为
键的键能为| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ/mol) | 414 | 489 | ? | 155 |
您最近一年使用:0次
2022-04-07更新
|
341次组卷
|
2卷引用:浙江省宁波市北仑区北仑中学2020-2021学年高一下学期中考试化学(选考)试题
6 . 燃烧法是测定有机化合物分子式的一种方法,准确称取某有机物样品3.0g完全燃烧,产物依次通过浓硫酸、浓碱溶液,实验结束后,称得浓硫酸质量增加1.8g,浓碱溶液质量增加4.4g。
(1)求该有机物的实验式为_______ 。
(2)若有机物相对氢气的密度为30,该有机物的核磁共振氢谱如下图所示,且该有机物能与 溶液反应产生气体,则其结构简式为
溶液反应产生气体,则其结构简式为_______ ;

(3)若该有机物既能与Na反应产生气体,又能发生银镜反应,则结构简式为_______ 。
(1)求该有机物的实验式为
(2)若有机物相对氢气的密度为30,该有机物的核磁共振氢谱如下图所示,且该有机物能与
 溶液反应产生气体,则其结构简式为
溶液反应产生气体,则其结构简式为
(3)若该有机物既能与Na反应产生气体,又能发生银镜反应,则结构简式为
您最近一年使用:0次
2022-03-18更新
|
542次组卷
|
4卷引用:浙江省精诚联盟2021-2022学年高二下学期3月联考化学试题
名校
解题方法
7 . 将氧化钠和过氧化钠组成的固体混合物溶于一定量的水中,充分反应后,收集到标准状况下的气体3.36L,同时得到0.8mol氢氧化钠,请计算
(1)原固体混合物中氧化钠和过氧化钠的质量___________ 。
(2)恰好中和所得溶液,需加入2.0mol/L H2SO4溶液的体积___________ 。
(1)原固体混合物中氧化钠和过氧化钠的质量
(2)恰好中和所得溶液,需加入2.0mol/L H2SO4溶液的体积
您最近一年使用:0次
解题方法
8 . 在标准状况下进行甲、乙、丙三组实验:各取 30 mL 同浓度的盐酸,加入不同质量的同一种镁铝合金粉末,产生气体,有关数据记录如下:
试回答:
(1)盐酸的物质的量浓度为____ mol·L-1。
(2) 镁 、铝的物质的量之比为____ 。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(g) | 0.255 | 0.385 | 0.459 |
| 生成气体体积(mL) | 280 | 336 | 336 |
试回答:
(1)盐酸的物质的量浓度为
(2) 镁 、铝的物质的量之比为
您最近一年使用:0次
21-22高一上·浙江·阶段练习
解题方法
9 . 一定体积的氢气(H2) 和氯气(Cl2)的混合气体在一定条件下反应,将反应后的混合气体用200mL 6.0 mol·L-1的KOH溶液吸收,恰好反应,测得溶液中含有一定量氯离子(Cl-)和0.40 mol ClO-(忽略其它含氯微粒)。请计算(写出计算过程);
(1)所得溶液中Cl-的物质的量浓度是_______ (忽略反应前后溶液体积变化)。
(2) H2和Cl2混合气体中的H2的物质的量_______ 。
(1)所得溶液中Cl-的物质的量浓度是
(2) H2和Cl2混合气体中的H2的物质的量
您最近一年使用:0次
19-20高一·浙江·期中
解题方法
10 . 将0.3mol氯化铝和11. 1g氯化钙组成的混合物溶于水配成200mL溶液,此溶液中C1-及氯化铝的物质的量浓度分别是多少___________ ?
您最近一年使用:0次



