名校
解题方法
1 . 将10.8gAl加入500mlNaOH溶液中,二者刚好完全反应,试计算:
(1)反应生成的氢气在标准状况下的体积为__________ 。
(2)反应所得NaOH溶液的物质的量浓度是___________ 。
(1)反应生成的氢气在标准状况下的体积为
(2)反应所得NaOH溶液的物质的量浓度是
您最近一年使用:0次
2020-11-21更新
|
166次组卷
|
2卷引用:四川省江油市第一中学2020-2021学年高一上学期期中考试化学试题
名校
解题方法
2 . 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,
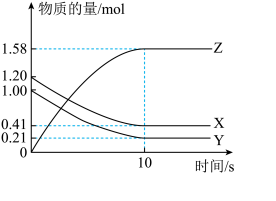
请回答下列问题:
(1)反应开始到10s,用Z表示的反应速率为___________ mol/(L·s)。
(2)反应开始到10s,X的物质的量浓度减少了_________ mol/L。
(3)反应开始到10s,Y的转化率为_________ 。
(4)反应的化学方程式为__________ 。
(5)10s之后,该反应达到________________ 状态。

请回答下列问题:
(1)反应开始到10s,用Z表示的反应速率为
(2)反应开始到10s,X的物质的量浓度减少了
(3)反应开始到10s,Y的转化率为
(4)反应的化学方程式为
(5)10s之后,该反应达到
您最近一年使用:0次
2020-07-29更新
|
818次组卷
|
4卷引用:四川省成都外国语学校2019-2020学年高一下学期期末考试化学(文)试题
名校
解题方法
3 . (1)3.1g Na2X含有Na+ 0.1mol,则Na2X的摩尔质量为__ ,X的相对原子质量为__ 。
(2)同温同压下,同体积的甲烷和氢气分子数之比为__ ,原子个数之比为__ ,质量之比为__ ,电子数之比为___ 。
(3)现有下列物质:
①CO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水
请用序号回答下列问题:能导电的是___ 。属于电解质的是___ 。属于非电解质的是___ 。
(4)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO42-浓度为0.9mol/L,则K+的物质的量浓度为___ mol/L;简述混合液中阴离子的检验方法:___ 。
(5)在标准状况下,将V L NH3溶于0.1L水中,所得溶液的密度为d g/cm3,则所得溶液的物质的量浓度为___ mol/L。
(2)同温同压下,同体积的甲烷和氢气分子数之比为
(3)现有下列物质:
①CO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水
请用序号回答下列问题:能导电的是
(4)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO42-浓度为0.9mol/L,则K+的物质的量浓度为
(5)在标准状况下,将V L NH3溶于0.1L水中,所得溶液的密度为d g/cm3,则所得溶液的物质的量浓度为
您最近一年使用:0次
名校
4 . 已知硫酸钠晶体(Na2SO4·10H2O)中钠离子数目3.01×1023,请计算填空:
(1)钠离子的物质的量是_____ ,硫酸钠晶体的物质的量是______ 。
(2)所含硫酸根离子的物质的量是______ ,硫酸根离子的数目是______ 。
(3)所含结晶水的物质的量是____ ,所含氧原子的物质的量是______ 。
(1)钠离子的物质的量是
(2)所含硫酸根离子的物质的量是
(3)所含结晶水的物质的量是
您最近一年使用:0次
5 . 将碳酸钠和碳酸氢钠的混合物27.4g,加热到质量不再变化时剩余物质的质量为21.2g。再另取试样27.4g,加入某浓度盐酸100ml,恰好完全反应。(书写计算过程,否则记零分)
(1)求混合物中Na2CO3和NaHCO3的质量。
(2)计算盐酸的物质的量浓度。
(1)求混合物中Na2CO3和NaHCO3的质量。
(2)计算盐酸的物质的量浓度。
您最近一年使用:0次



