名校
解题方法
1 . 常温下,根据表中的几种物质的电离平衡常数回答下列问题:
(1)已知 溶液呈中性。常温下,浓度均为0.1mol/L的8种溶液:①HCl溶液;②
溶液呈中性。常温下,浓度均为0.1mol/L的8种溶液:①HCl溶液;② 溶液;③
溶液;③ 溶液:④NaOH;⑤
溶液:④NaOH;⑤ 溶液;⑥CH3COONa溶液;⑦KCl溶液:⑧
溶液;⑥CH3COONa溶液;⑦KCl溶液:⑧ 溶液。这些溶液中水的电离程度最大是
溶液。这些溶液中水的电离程度最大是___________ (填序号)。
(2)Na2CO3溶液显碱性的原因___________ 。(用离子方程式表示)
(3)若取等体积的pH=2的盐酸和醋酸两种溶液分别与足量金属锌反应,产生氢气的质量较多的是_____ (填序号)。
(4)某温度下纯水的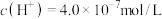 ,若温度不变,滴入稀盐酸,使
,若温度不变,滴入稀盐酸,使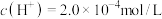 ,则此溶液中由水电离产生的
,则此溶液中由水电离产生的
_______ 。
(5)25℃时, 的
的 的
的 溶液与
溶液与 的
的 的
的 溶液混合后,溶液呈中性,则a和b满足的关系
溶液混合后,溶液呈中性,则a和b满足的关系_______ 。
(6)向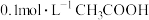 溶液中滴加
溶液中滴加 溶液至
溶液至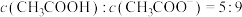 ,此时溶液
,此时溶液
_______ 。
(7)已知 的
的 ,
, 的
的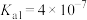 ,
,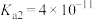 ,则反应
,则反应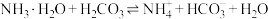 的平衡常数
的平衡常数
_______ 。
(8)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显___________ 性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=___________ 。
(9)25℃时,向0.1mol·L-1的氨水中缓缓通入少量CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是____。
| 弱酸 |  |  |  |
| 电离平衡常数 |  |  | 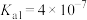 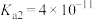 |
 溶液呈中性。常温下,浓度均为0.1mol/L的8种溶液:①HCl溶液;②
溶液呈中性。常温下,浓度均为0.1mol/L的8种溶液:①HCl溶液;② 溶液;③
溶液;③ 溶液:④NaOH;⑤
溶液:④NaOH;⑤ 溶液;⑥CH3COONa溶液;⑦KCl溶液:⑧
溶液;⑥CH3COONa溶液;⑦KCl溶液:⑧ 溶液。这些溶液中水的电离程度最大是
溶液。这些溶液中水的电离程度最大是(2)Na2CO3溶液显碱性的原因
(3)若取等体积的pH=2的盐酸和醋酸两种溶液分别与足量金属锌反应,产生氢气的质量较多的是
(4)某温度下纯水的
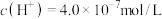 ,若温度不变,滴入稀盐酸,使
,若温度不变,滴入稀盐酸,使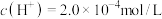 ,则此溶液中由水电离产生的
,则此溶液中由水电离产生的
(5)25℃时,
 的
的 的
的 溶液与
溶液与 的
的 的
的 溶液混合后,溶液呈中性,则a和b满足的关系
溶液混合后,溶液呈中性,则a和b满足的关系(6)向
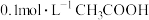 溶液中滴加
溶液中滴加 溶液至
溶液至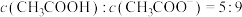 ,此时溶液
,此时溶液
(7)已知
 的
的 ,
, 的
的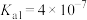 ,
,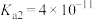 ,则反应
,则反应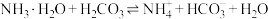 的平衡常数
的平衡常数
(8)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(9)25℃时,向0.1mol·L-1的氨水中缓缓通入少量CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是____。
A. | B. | C. | D.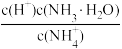 |
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题:
(1)常温下,将pH=9的NaOH溶液稀释1000倍,溶液中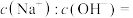
______
(2)常温下,已知醋酸的电离常数为Ka,向100mL0.1mol/L的醋酸溶液中,加入______ mL0.1mol/L的NaOH,可使反应所得的溶液pH=7(用含Ka的式子表达)
(3)常温下,100mLpH=0盐酸和硫酸的混合溶液中加入200mLpH=13的 ,恰好沉淀完全,则原溶液中c(HCl)=
,恰好沉淀完全,则原溶液中c(HCl)=______
(4)常温下,设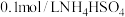 溶液的pH为a,则
溶液的pH为a,则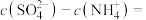
______ (用含a的精确式子表达)
(1)常温下,将pH=9的NaOH溶液稀释1000倍,溶液中
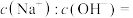
(2)常温下,已知醋酸的电离常数为Ka,向100mL0.1mol/L的醋酸溶液中,加入
(3)常温下,100mLpH=0盐酸和硫酸的混合溶液中加入200mLpH=13的
 ,恰好沉淀完全,则原溶液中c(HCl)=
,恰好沉淀完全,则原溶液中c(HCl)=(4)常温下,设
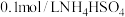 溶液的pH为a,则
溶液的pH为a,则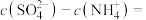
您最近一年使用:0次
3 . 请回答下列问题:
(1)标准状况下,V L氯化氢(HCl)溶解在1 L水中(水的密度近似为1 g/mL)所得溶液的密度为ρ g/mL,则所得盐酸物质的量浓度为_______
(2)将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g·mL-1,该溶液中溶质质量分数为_______
(3)在200 mL氯化镁和氯化铝的混合溶液中,c(Mg2+)为0.2 mol·L-1,c(Cl-)为1.3 mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4 mol·L-1 NaOH溶液的体积为_______
(4)某铁的氧化物(FexO)1.52 g溶于足量盐酸中,向所得溶液中通入112 mL Cl2(标准状况下),恰好将Fe2+完全氧化。x值为_______
(5)向一定量的FeO、Fe、Fe3O4的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,放出224 mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是_______
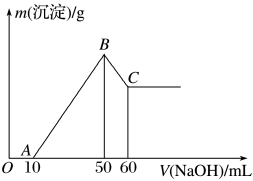
(6)某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1 mol·L-1 NaOH溶液,消耗NaOH溶液体积和生成沉淀之间的关系如下图所示。则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为_______
(1)标准状况下,V L氯化氢(HCl)溶解在1 L水中(水的密度近似为1 g/mL)所得溶液的密度为ρ g/mL,则所得盐酸物质的量浓度为
(2)将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g·mL-1,该溶液中溶质质量分数为
(3)在200 mL氯化镁和氯化铝的混合溶液中,c(Mg2+)为0.2 mol·L-1,c(Cl-)为1.3 mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4 mol·L-1 NaOH溶液的体积为
(4)某铁的氧化物(FexO)1.52 g溶于足量盐酸中,向所得溶液中通入112 mL Cl2(标准状况下),恰好将Fe2+完全氧化。x值为
(5)向一定量的FeO、Fe、Fe3O4的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,放出224 mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是
(6)某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1 mol·L-1 NaOH溶液,消耗NaOH溶液体积和生成沉淀之间的关系如下图所示。则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为

您最近一年使用:0次
2022-04-04更新
|
1306次组卷
|
3卷引用:四川省泸县第四中学2022-2023学年高一上学期第三次月考化学试题
四川省泸县第四中学2022-2023学年高一上学期第三次月考化学试题江苏省天一中学2021-2022学年高一上学期期末考试化学(强化班)试题(已下线)专题02 阿伏加德罗常数及其化学计算 (测)-2023年高考化学二轮复习讲练测(新高考专用)
4 . 60.8g铁和氧化铁的混合物恰好能完全溶解在500mL 2mol/L稀硫酸中,向反应后的溶液中加入KSCN溶液,无明显现象。试求:
(1)混合物中铁元素的质量分数是多少?(计算结果保留一位小数)________
(2)反应过程中是否有氢气产生?若有,计算在标准状况下的体积是多少L,若无,通过计算说明理由。________
(1)混合物中铁元素的质量分数是多少?(计算结果保留一位小数)
(2)反应过程中是否有氢气产生?若有,计算在标准状况下的体积是多少L,若无,通过计算说明理由。
您最近一年使用:0次
5 . Ⅰ.25℃时,0.1 mol/L的HA溶液中 =1010,0.01 mol/L的BOH溶液pH=12。
=1010,0.01 mol/L的BOH溶液pH=12。
(1)BOH是_____ (填“强电解质”或“弱电解质”),HA的电离方程式是____
(2)在加水稀释HA的过程中,随着水量的增加而减小的是_____ (填字母)。
A.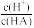 B.
B.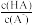 C.c(H+)与c(OH—)的乘积 D.c(OH—)
C.c(H+)与c(OH—)的乘积 D.c(OH—)
(3)在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体____ (填“多”、“少”或“相等”)。
Ⅱ.在25 ℃时,请进行有关计算(假定溶液体积有加和性)
(4)现有pH=2的HCl溶液100 mL,要使它的pH=3,如果加入蒸馏水,需要____ mL。 如果加入pH=4的HCl溶液,需加入此HCl溶液____ mL。
(5)pH=a的X体积的某强酸与pH=b的Y体积的某强碱混合后,溶液呈中性,已知a+b=15,则X:Y=_____ 。
 =1010,0.01 mol/L的BOH溶液pH=12。
=1010,0.01 mol/L的BOH溶液pH=12。(1)BOH是
(2)在加水稀释HA的过程中,随着水量的增加而减小的是
A.
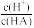 B.
B.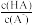 C.c(H+)与c(OH—)的乘积 D.c(OH—)
C.c(H+)与c(OH—)的乘积 D.c(OH—)(3)在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体
Ⅱ.在25 ℃时,请进行有关计算(假定溶液体积有加和性)
(4)现有pH=2的HCl溶液100 mL,要使它的pH=3,如果加入蒸馏水,需要
(5)pH=a的X体积的某强酸与pH=b的Y体积的某强碱混合后,溶液呈中性,已知a+b=15,则X:Y=
您最近一年使用:0次
2021-05-09更新
|
674次组卷
|
2卷引用:四川省阆中中学2020-2021学年高二下学期期中教学质量检测化学试题
解题方法
6 . 化学家研制出了一种复杂的铁氧化物(FexOy),取该氧化物76.0 g溶于600 mL 2.5 mol/L稀硫酸中,得到溶液X。向溶液X中加入一定体积4.0 mol/L NaOH溶液,恰好使溶液中的金属离子沉淀完全。过滤、洗涤,将沉淀加热至质量不再变化,得残渣80.0g。
回答下列问题:
(1)加热沉淀时发生反应的化学方程式为_______ ,所得残渣的颜色为_______ 。
(2)铁氧化物(FexOy)的化学式为_______ ,所加NaOH溶液的体积为_______ mL。
(3)向溶液X中加入足量铁粉制备绿矾(化学式为FeSO4·7H2O,相对分子质量278),不考虑产品损失,最多能够制备多少克绿矾?______ (无解题过程不给分)
回答下列问题:
(1)加热沉淀时发生反应的化学方程式为
(2)铁氧化物(FexOy)的化学式为
(3)向溶液X中加入足量铁粉制备绿矾(化学式为FeSO4·7H2O,相对分子质量278),不考虑产品损失,最多能够制备多少克绿矾?
您最近一年使用:0次
解题方法
7 . (1)常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为SO2的是_________ (填选项序号)。

(2)设NA为阿伏加德罗常数的数值,如果ag某气体中含有的分子数为b,那么cg该气体在标准状况下的体积约是__________ 。
(3)液态化合物在一定量的氧气中恰好完全燃烧,反应方程式为:XY2+3O2=XO2+2YO2,冷却后(产物均为气态),在标准状况下测得生成物的体积是336mL,密度是2.56g/L。
①反应前O2的体积是________ mL(标准状况),化合物XY2的摩尔质量是________ 。
②若XY2分子中X、Y两元素的质量比是3:16,则X、Y两元素分别为______ 和______ (写元素符号)。

(2)设NA为阿伏加德罗常数的数值,如果ag某气体中含有的分子数为b,那么cg该气体在标准状况下的体积约是
(3)液态化合物在一定量的氧气中恰好完全燃烧,反应方程式为:XY2+3O2=XO2+2YO2,冷却后(产物均为气态),在标准状况下测得生成物的体积是336mL,密度是2.56g/L。
①反应前O2的体积是
②若XY2分子中X、Y两元素的质量比是3:16,则X、Y两元素分别为
您最近一年使用:0次
解题方法
8 . (1)化合物A分子组成可用OxFy表示。30mLA气体在一定条件下能分解生成15mLO2和30mLF2(在同温同压下),A的化学式是__________ 。
(2)1.5mol CH3COOH所含氧原子数跟________ g H2O所含氧原子数相等。
(3)实验室现有Fe2(SO4)3溶液100mL, 的物质的量浓度为0.45 mol·L-1,则Fe3+的物质的量浓度为
的物质的量浓度为0.45 mol·L-1,则Fe3+的物质的量浓度为_________ mol·L-1,含有Fe2(SO4)3 的质量为________ g。
(4)N2和CH4的混合气体11g,在标准状况下的体积为11.2L,则混合气体的平均摩尔质量为________ ,混合气体中CH4的电子数为________ 。
(2)1.5mol CH3COOH所含氧原子数跟
(3)实验室现有Fe2(SO4)3溶液100mL,
 的物质的量浓度为0.45 mol·L-1,则Fe3+的物质的量浓度为
的物质的量浓度为0.45 mol·L-1,则Fe3+的物质的量浓度为(4)N2和CH4的混合气体11g,在标准状况下的体积为11.2L,则混合气体的平均摩尔质量为
您最近一年使用:0次
2020-10-15更新
|
257次组卷
|
2卷引用:四川省合江县马街中学校2023-2024学年高一上学期12月月考化学试题
名校
9 . 将质量为1.15g钠用刺了孔的铝箔包裹后放入水中,反应结束后共收集到0.055mol气体.请回答下列问题,写出必要的计算过程:
(1)1.15g钠与水反应,理论上生成气体的体积(标准状况)为多少_____________ ?
(2)若反应后溶液的体积为50ml,则反应后氢氧化钠溶液的浓度为多少_______________ ?
(1)1.15g钠与水反应,理论上生成气体的体积(标准状况)为多少
(2)若反应后溶液的体积为50ml,则反应后氢氧化钠溶液的浓度为多少
您最近一年使用:0次
2020-09-09更新
|
775次组卷
|
3卷引用:四川省江油中学2018-2019学年高一下学期入学考试化学试题
解题方法
10 . 完成下列两个小题
(1)将2.56gCu放入10.0mL浓HNO3中正好完全反应。随着Cu的不断减少,反应生成气体的颜色逐渐变浅,最终共生成气体1.12L(标准状况)。则该浓硝酸的物质的量浓度是_____ mol/L;若将生成的气体溶于水被全部吸收,还需要消耗标准状况下O2_____ mL。
(2)标准状况下,某气态烷烃和乙烯的混合气体11.2L,质量为10.4g。则混合气体中烷烃的分子式为_______ ;若将该混合气体通入足量的溴水,溴水的质量将增加_______ g。
(1)将2.56gCu放入10.0mL浓HNO3中正好完全反应。随着Cu的不断减少,反应生成气体的颜色逐渐变浅,最终共生成气体1.12L(标准状况)。则该浓硝酸的物质的量浓度是
(2)标准状况下,某气态烷烃和乙烯的混合气体11.2L,质量为10.4g。则混合气体中烷烃的分子式为
您最近一年使用:0次
2020-07-25更新
|
869次组卷
|
2卷引用:四川省三台中学实验学校2019-2020学年高一4月月考化学试题



