1 .  .根据下列插图,回答以下问题:
.根据下列插图,回答以下问题:___________ 。
(2)图2的每条折线代表元素周期表 中的某族元素在对应周期的简单氢化物的沸点变化。每个小黑点代表一种简单氢化物,其中
中的某族元素在对应周期的简单氢化物的沸点变化。每个小黑点代表一种简单氢化物,其中 点依次代表的物质是
点依次代表的物质是___________ 、___________ (写化学式)。
(3)图3是 在高温高压下所形成晶体的晶胞示意图,则该晶体的类型属于
在高温高压下所形成晶体的晶胞示意图,则该晶体的类型属于___________ 晶体。
 .新型超高能材料是国家核心军事力量制高点的重要标志,高性能炸药
.新型超高能材料是国家核心军事力量制高点的重要标志,高性能炸药 的结构如图:
的结构如图: 同周期的所有过渡元素的基态原子中,最外层电子数与钴不同的元素有
同周期的所有过渡元素的基态原子中,最外层电子数与钴不同的元素有___________ 种。
(5)①配体 是平面结构,图中标记“*”的N原子与O原子之间
是平面结构,图中标记“*”的N原子与O原子之间 键是由N原子的
键是由N原子的___________ 杂化轨道与O原子的___________ 轨道重叠形成的。
②请比较键角大小, 分子中
分子中
___________ (选填“>”、“<”或“=”)高性能炸药 中
中 ,其原因为
,其原因为___________ 。
(6)一种钴的化合物可用作石油脱硫的催化剂,其晶胞结构如图所示。若晶胞参数为 ,则
,则 之间的最短距离为
之间的最短距离为___________  。
。
 .根据下列插图,回答以下问题:
.根据下列插图,回答以下问题:
(2)图2的每条折线代表元素周期表
 中的某族元素在对应周期的简单氢化物的沸点变化。每个小黑点代表一种简单氢化物,其中
中的某族元素在对应周期的简单氢化物的沸点变化。每个小黑点代表一种简单氢化物,其中 点依次代表的物质是
点依次代表的物质是(3)图3是
 在高温高压下所形成晶体的晶胞示意图,则该晶体的类型属于
在高温高压下所形成晶体的晶胞示意图,则该晶体的类型属于 .新型超高能材料是国家核心军事力量制高点的重要标志,高性能炸药
.新型超高能材料是国家核心军事力量制高点的重要标志,高性能炸药 的结构如图:
的结构如图:
 同周期的所有过渡元素的基态原子中,最外层电子数与钴不同的元素有
同周期的所有过渡元素的基态原子中,最外层电子数与钴不同的元素有(5)①配体
 是平面结构,图中标记“*”的N原子与O原子之间
是平面结构,图中标记“*”的N原子与O原子之间 键是由N原子的
键是由N原子的②请比较键角大小,
 分子中
分子中
 中
中 ,其原因为
,其原因为(6)一种钴的化合物可用作石油脱硫的催化剂,其晶胞结构如图所示。若晶胞参数为
 ,则
,则 之间的最短距离为
之间的最短距离为 。
。
您最近一年使用:0次
2 .  是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含
是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含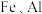 及其化合物、
及其化合物、 等杂质),生产
等杂质),生产 的工艺流程如下:
的工艺流程如下: )时的
)时的 如下表:
如下表:
② 溶液用水稀释后可生成
溶液用水稀释后可生成 沉淀。
沉淀。
(1)“酸浸”时提高浸取率的措施有___________ (写出两条)。
(2)滤渣I的主要成分是___________ (填化学式)。
(3)操作 为调节溶液的
为调节溶液的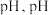 的最佳范围是
的最佳范围是___________ ,加入的物质X可以是___________ ( (填字母标号)。
A. B.
B.  C.
C.  D.
D.  溶液
溶液
(4)往滤液 中加入食盐并通入
中加入食盐并通入 可生成
可生成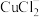 ,反应I的离子方程式为
,反应I的离子方程式为___________ ;在反应I中加入食盐并加热的目的是___________ 。
(5)实验室可以使用铜电极电解饱和食盐水得到 ,阳极的电极反应式为
,阳极的电极反应式为___________ 。
 是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含
是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含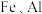 及其化合物、
及其化合物、 等杂质),生产
等杂质),生产 的工艺流程如下:
的工艺流程如下:
 )时的
)时的 如下表:
如下表:| 物质 |  |  |  |
开始沉淀时的 | 1.6 | 3.2 | 5.2 |
完全沉淀时的 | 3.1 | 4.7 | 6.7 |
 溶液用水稀释后可生成
溶液用水稀释后可生成 沉淀。
沉淀。(1)“酸浸”时提高浸取率的措施有
(2)滤渣I的主要成分是
(3)操作
 为调节溶液的
为调节溶液的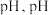 的最佳范围是
的最佳范围是A.
 B.
B.  C.
C.  D.
D.  溶液
溶液(4)往滤液
 中加入食盐并通入
中加入食盐并通入 可生成
可生成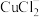 ,反应I的离子方程式为
,反应I的离子方程式为(5)实验室可以使用铜电极电解饱和食盐水得到
 ,阳极的电极反应式为
,阳极的电极反应式为
您最近一年使用:0次
3 . 2023年杭州亚运会主火炬创新使用了“零碳”甲醇作为燃料,所谓“零碳”,是指每合成1吨该甲醇可以消耗约1.375吨的二氧化碳,实现了二氧化碳的资源化利用、废碳再生。回答下列问题:
(1) 合成甲醇的工艺分两类:
合成甲醇的工艺分两类:
①直接法原理为:
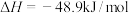
利于该反应自发进行的条件为___________ (填“高温”、“低温”或“任意温度”)。
②间接法合成原理如下:
Ⅰ.
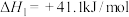
Ⅱ.

则
___________ 。该法的决速步骤为反应Ⅰ,则下列示意图中能体现上述反应反应进程与能量变化的是___________ 。___________ 。
(2)一定温度下,利用直接法合成甲醇,将二氧化碳和氢气按物质的量之比 混合并在恒定压强为44MPa条件下进行反应,达平衡时
混合并在恒定压强为44MPa条件下进行反应,达平衡时 的转化率为90%,则平衡时
的转化率为90%,则平衡时 的分压为
的分压为___________ ,该反应的分压平衡常数
___________  。
。
(3)直接甲醇燃料电池是指直接使用甲醇为电极活性物质的燃料电池,写出该电池在酸性条件下的负极反应方程式___________ 。
(4)目前有多种用于工业捕集 的方法,其中一种为以
的方法,其中一种为以 溶液吸收,若某工厂的
溶液吸收,若某工厂的 吸收液吸收一定量
吸收液吸收一定量 后测得溶液中
后测得溶液中 ,则该溶液的
,则该溶液的
___________ (已知该温度下碳酸的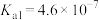 ,
,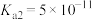 )。
)。
(1)
 合成甲醇的工艺分两类:
合成甲醇的工艺分两类:①直接法原理为:

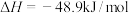
利于该反应自发进行的条件为
②间接法合成原理如下:
Ⅰ.

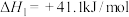
Ⅱ.


则

A. B.
B.
C. D.
D.

(2)一定温度下,利用直接法合成甲醇,将二氧化碳和氢气按物质的量之比
 混合并在恒定压强为44MPa条件下进行反应,达平衡时
混合并在恒定压强为44MPa条件下进行反应,达平衡时 的转化率为90%,则平衡时
的转化率为90%,则平衡时 的分压为
的分压为
 。
。(3)直接甲醇燃料电池是指直接使用甲醇为电极活性物质的燃料电池,写出该电池在酸性条件下的负极反应方程式
(4)目前有多种用于工业捕集
 的方法,其中一种为以
的方法,其中一种为以 溶液吸收,若某工厂的
溶液吸收,若某工厂的 吸收液吸收一定量
吸收液吸收一定量 后测得溶液中
后测得溶液中 ,则该溶液的
,则该溶液的
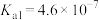 ,
,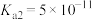 )。
)。
您最近一年使用:0次
4 . 在一定体积下,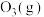 分解时相关物质的相对能量与反应历程关系如图所示[已知
分解时相关物质的相对能量与反应历程关系如图所示[已知 和
和 的相对能量为0]。下列说法错误的是
的相对能量为0]。下列说法错误的是
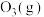 分解时相关物质的相对能量与反应历程关系如图所示[已知
分解时相关物质的相对能量与反应历程关系如图所示[已知 和
和 的相对能量为0]。下列说法错误的是
的相对能量为0]。下列说法错误的是
A.根据图像可知: |
B.形成1molCl―Cl键时释放的能量为 |
C. 的平衡转化率:历程Ⅰ=历程Ⅱ 的平衡转化率:历程Ⅰ=历程Ⅱ |
D.历程Ⅱ中快反应的热化学方程式为 , , |
您最近一年使用:0次
名校
解题方法
5 . 重铬酸钾是一种重要的化工原料,可由铬铁矿(主要成分为 ,还含有硅、铝的氧化物等杂质)制备,流程如图所示:
,还含有硅、铝的氧化物等杂质)制备,流程如图所示: 主要以
主要以 形式存在,加入酸会转为
形式存在,加入酸会转为 。
。
Ⅱ.有关物质的溶解度如图所示:______ (任写一条)。
(2)步骤①中主要反应为: ,上述反应配平后
,上述反应配平后 与
与 的系数比为
的系数比为______ 。
(3)滤渣1中含量最多的金属元素是______ ,滤渣2的主要成分是Y及含硅杂质。向滤液1通入过量 得到Y的离子方程式为
得到Y的离子方程式为______ 。
(4)步骤④将滤液2的pH调小的原因是______ (结合离子方程式和文字表述说明)。
(5)向“滤液3”中加入适量KCl,经过操作X后得到 固体。操作X为:
固体。操作X为:______ ,过滤、洗涤、干燥。
(6)某工厂用448kg铬铁矿粉( 的含量为80%)制备
的含量为80%)制备 ,最终得到产品182.4kg,则
,最终得到产品182.4kg,则 的产率为
的产率为______ %。
 ,还含有硅、铝的氧化物等杂质)制备,流程如图所示:
,还含有硅、铝的氧化物等杂质)制备,流程如图所示:
 主要以
主要以 形式存在,加入酸会转为
形式存在,加入酸会转为 。
。Ⅱ.有关物质的溶解度如图所示:

(2)步骤①中主要反应为:
 ,上述反应配平后
,上述反应配平后 与
与 的系数比为
的系数比为(3)滤渣1中含量最多的金属元素是
 得到Y的离子方程式为
得到Y的离子方程式为(4)步骤④将滤液2的pH调小的原因是
(5)向“滤液3”中加入适量KCl,经过操作X后得到
 固体。操作X为:
固体。操作X为:(6)某工厂用448kg铬铁矿粉(
 的含量为80%)制备
的含量为80%)制备 ,最终得到产品182.4kg,则
,最终得到产品182.4kg,则 的产率为
的产率为
您最近一年使用:0次
名校
解题方法
6 . 下列实验的操作、现象及结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | 向盛有未知溶液的试管中滴加足量NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中不含 |
B | 向2支分别盛有5mL | 均有气泡产生且 |
|
C | 往 | 溶液先变成血红色后无明显变化 |
|
D | 用50mL注射器抽入20mL | 混合气体的颜色先变深再变浅 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.0.1mol 含有电子数为 含有电子数为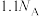 |
B.6.4gCu与0.1molS充分反应,转移电子数为 |
C.常温下,2.7g铝粉与足量浓硝酸反应,转移电子数为 |
D.1L 氨水中含有 氨水中含有 和 和 的数目之和为 的数目之和为 |
您最近一年使用:0次
名校
8 . 优良的有机溶剂对孟烷、耐热型特种高分子功能材料PMnMA的合成路线如下:
①由B生成对孟烷的反应类型是___________ 。对孟烷的一氯代物有___________ 种。
②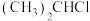 与A生成B的化学方程式是
与A生成B的化学方程式是___________ 。
③A的同系物中相对分子质量最小的物质是___________ 。
(2)1.08g的C与饱和溴水完全反应生成3.45g白色沉淀。E不能使 的
的 溶液褪色。
溶液褪色。
①F的官能团是___________ 。
②C的结构简式是___________ 。C的属于芳香化合物且具有官能团―OH的同分异构体有___________ 种。
③反应I的化学方程式是___________ 。
(3)下列说法正确的是___________。
(4)G的核磁共振氢谱有3种峰,其峰面积之比为3∶2∶1.G与 反应放出
反应放出 。
。
反应Ⅱ的化学方程式是___________ 。

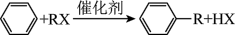 (R为烷基,X为卤原子)
(R为烷基,X为卤原子)
①由B生成对孟烷的反应类型是
②
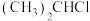 与A生成B的化学方程式是
与A生成B的化学方程式是③A的同系物中相对分子质量最小的物质是
(2)1.08g的C与饱和溴水完全反应生成3.45g白色沉淀。E不能使
 的
的 溶液褪色。
溶液褪色。①F的官能团是
②C的结构简式是
③反应I的化学方程式是
(3)下列说法正确的是___________。
| A.B可使酸性高锰酸钾溶液褪色 | B.C不存在醛类同分异构体 |
| C.D的酸性比E弱 | D.E的沸点高于对孟烷 |
(4)G的核磁共振氢谱有3种峰,其峰面积之比为3∶2∶1.G与
 反应放出
反应放出 。
。反应Ⅱ的化学方程式是
您最近一年使用:0次
名校
9 . 呼吸系统疾病药物特布他林(H)的一种合成路线如下:
回答下列问题:
(1)已知A的名称为3,5-二羟基苯甲酸,则B的名称为________ ;A→B的反应条件为________ 。
(2)B→C的化学方程式为________ ,反应类型为________ 。
(3)E的结构简式为________ ;F中含氧官能团有________ 种。
(4)检验H中酚羟基的试剂是________ ;H的同分异构体中,仅含有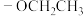 、
、 和苯环结构的有
和苯环结构的有________ 种。
(5)根据上述信息,写出以4-羟基邻苯二甲酸二乙酯为主要原料合成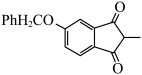 的路线:
的路线:________ 。

已知:I.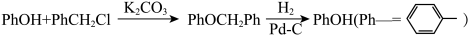
Ⅱ.
回答下列问题:
(1)已知A的名称为3,5-二羟基苯甲酸,则B的名称为
(2)B→C的化学方程式为
(3)E的结构简式为
(4)检验H中酚羟基的试剂是
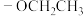 、
、 和苯环结构的有
和苯环结构的有(5)根据上述信息,写出以4-羟基邻苯二甲酸二乙酯为主要原料合成
 的路线:
的路线:
您最近一年使用:0次
解题方法
10 . 化合物E是一种具有抗肿瘤活性的分子,由丙烯酰氯A合成E的路线如下:
(1)A的官能团包括酰氯基和_____ (填名称)。
(2)由B生成C的反应类型为_____ 。G与 溶液反应的化学方程式为
溶液反应的化学方程式为_____ 。
(3)参考A的化学名称,H的化学名称为_____ 。C与H反应时,C中反应活性更高的“ ”基团是
”基团是_____ (填“a”或“b”)处。
(4)D转化成E时发生取代反应,生成的另一产物是_____ 。
(5)H的芳香同分异构体J具有手性碳(连有4个不同的原子或基团的碳原子),可以与新制 试剂产生砖红色沉淀。写出J的结构简式
试剂产生砖红色沉淀。写出J的结构简式_____ 。
(6)若上述合成路线改为 ,最终所得主要产物为
,最终所得主要产物为_____ (填数字序号)。

(1)A的官能团包括酰氯基和
(2)由B生成C的反应类型为
 溶液反应的化学方程式为
溶液反应的化学方程式为(3)参考A的化学名称,H的化学名称为
 ”基团是
”基团是(4)D转化成E时发生取代反应,生成的另一产物是
(5)H的芳香同分异构体J具有手性碳(连有4个不同的原子或基团的碳原子),可以与新制
 试剂产生砖红色沉淀。写出J的结构简式
试剂产生砖红色沉淀。写出J的结构简式(6)若上述合成路线改为
 ,最终所得主要产物为
,最终所得主要产物为① ②
② ③
③
您最近一年使用:0次

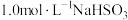 溶液的试管中同时加入2mL5%
溶液的试管中同时加入2mL5% 溶液
溶液
 溶液产生气泡快
溶液产生气泡快 溶液中滴加KSCN溶液,再加入少量
溶液中滴加KSCN溶液,再加入少量 固体
固体 的反应不可逆
的反应不可逆 和
和 混合气体,细管端用橡胶塞封闭,将针筒迅速推至10mL处
混合气体,细管端用橡胶塞封闭,将针筒迅速推至10mL处 平衡右移
平衡右移

