1 . 下列离子方程式正确的是
A.溴化亚铁溶液与等物质的量的氯气: |
B.向苯酚钠溶液中通入少量 : : |
C.铜片与某硝酸恰好生成相同量 的反应: 的反应: |
D.向次氯酸钠溶液中通入二氧化硫: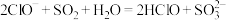 |
您最近一年使用:0次
解题方法
2 . 下列反应的离子方程式正确的是
A.向 溶液中通入少量氯气: 溶液中通入少量氯气: |
B.向稀硝酸中加入少量磁性氧化铁粉末: |
C.已知 的 的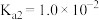 ,将硫酸铜溶解于足量浓盐酸中: ,将硫酸铜溶解于足量浓盐酸中: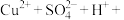 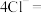 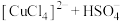 |
D.向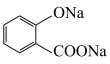 溶液中通入少量二氧化碳: 溶液中通入少量二氧化碳: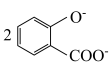  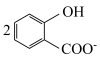  |
您最近一年使用:0次
3 . 已知: 、
、 分别为一元弱碱和一元弱酸,二者在水中电离方程式分别为:
分别为一元弱碱和一元弱酸,二者在水中电离方程式分别为: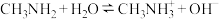 ;
;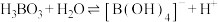 。25℃时,将10mL浓度均为
。25℃时,将10mL浓度均为 的
的 、
、 两种溶液分别加水稀释。曲线如图所示,
两种溶液分别加水稀释。曲线如图所示, 是溶液体积(mL),
是溶液体积(mL), 。下列说法正确的是
。下列说法正确的是
 、
、 分别为一元弱碱和一元弱酸,二者在水中电离方程式分别为:
分别为一元弱碱和一元弱酸,二者在水中电离方程式分别为: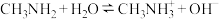 ;
;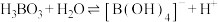 。25℃时,将10mL浓度均为
。25℃时,将10mL浓度均为 的
的 、
、 两种溶液分别加水稀释。曲线如图所示,
两种溶液分别加水稀释。曲线如图所示, 是溶液体积(mL),
是溶液体积(mL), 。下列说法正确的是
。下列说法正确的是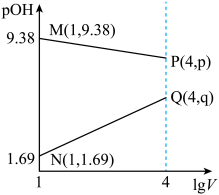
A.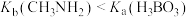 |
B.水的电离程度: |
C.溶液中的阴、阳离子总浓度: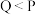 |
D.常温下,向上述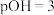 的 的 溶液加入等体积 溶液加入等体积 的盐酸后呈中性 的盐酸后呈中性 |
您最近一年使用:0次
名校
解题方法
4 . 乙醇-水催化重整可获得 。主要发生以下反应:
。主要发生以下反应:
反应Ⅰ:
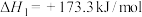
反应Ⅱ:
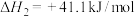
(1)反应Ⅰ自发进行的条件是_______。
(2)500℃时,向体积为VL的恒容密闭容器中充入1mol (g)和3mol
(g)和3mol  (g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%,
(g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%, 的转化率为80%。(CO的选择性=
的转化率为80%。(CO的选择性= )
)
①反应Ⅰ的
_______ (列出计算式即可)。反应Ⅰ的标准平衡常数 ,其中
,其中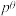 为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
②在下图中画出500℃时,乙醇平衡转化率随[ ]变化而变化的情况
]变化而变化的情况_______ 。 的平衡产率与温度、起始时
的平衡产率与温度、起始时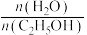 关系如图所示,每条曲线表示
关系如图所示,每条曲线表示 相同的平衡产率。
相同的平衡产率。 的平衡产率:Q点
的平衡产率:Q点_______ N点(填“>”、“=”或“<”);
②M、N两点 的平衡产率相等的原因是
的平衡产率相等的原因是_______ 。
(4)氢气的应用:氢气熔融碳酸盐燃料电池工作原理如图所示。 和
和 经催化重整生成CO和
经催化重整生成CO和 ,CO和
,CO和 全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)
全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)_______ 。
②理论上负极生成的 与正极消耗的
与正极消耗的 的物质的量之比是
的物质的量之比是_______ 。
 。主要发生以下反应:
。主要发生以下反应:反应Ⅰ:

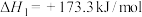
反应Ⅱ:

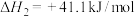
(1)反应Ⅰ自发进行的条件是_______。
| A.低温 | B.高温 | C.低压 | D.高压 |
(2)500℃时,向体积为VL的恒容密闭容器中充入1mol
 (g)和3mol
(g)和3mol  (g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%,
(g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%, 的转化率为80%。(CO的选择性=
的转化率为80%。(CO的选择性= )
)①反应Ⅰ的

 ,其中
,其中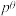 为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。②在下图中画出500℃时,乙醇平衡转化率随[
 ]变化而变化的情况
]变化而变化的情况
 的平衡产率与温度、起始时
的平衡产率与温度、起始时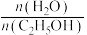 关系如图所示,每条曲线表示
关系如图所示,每条曲线表示 相同的平衡产率。
相同的平衡产率。
 的平衡产率:Q点
的平衡产率:Q点②M、N两点
 的平衡产率相等的原因是
的平衡产率相等的原因是(4)氢气的应用:氢气熔融碳酸盐燃料电池工作原理如图所示。

 和
和 经催化重整生成CO和
经催化重整生成CO和 ,CO和
,CO和 全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)
全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)②理论上负极生成的
 与正极消耗的
与正极消耗的 的物质的量之比是
的物质的量之比是
您最近一年使用:0次
解题方法
5 . 根据实验目的设计方案并进行实验,下列有关方案设计、实验现象或结论都正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 比较Cu和Fe的金属性强弱 | 取同浓度的① 、② 、② 溶液,滴加同浓度氨水 溶液,滴加同浓度氨水 | ①先沉淀后溶解,②沉淀后不溶解 | 金属性:Cu<Fe |
| B | 检验己烯中的碳碳双键 | 取少量己烯,加入溴的四氯化碳溶液,振荡 | 上下两层均无色 | 己烯中含碳碳双键 |
| C | 比较配离子的稳定性 | 向盛有少量蒸馏水的试管里加2滴 ,然后再加2滴硫氰化钾溶液 ,然后再加2滴硫氰化钾溶液 | 溶液由黄色变血红色 |  与 与 形成的配离子更稳定 形成的配离子更稳定 |
| D | 比较温度对反应速率的影响 | 将2mL 0.1mol/L  溶液(A)浸入0℃水浴中、2mL 0.05mol/L 溶液(A)浸入0℃水浴中、2mL 0.05mol/L  溶液(B)浸入50℃水浴中,再同时滴加0.1mol/L稀硫酸2mL 溶液(B)浸入50℃水浴中,再同时滴加0.1mol/L稀硫酸2mL | B溶液比A溶液先出现浑浊 | 温度越高,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 某废水处理过程中始终保持 饱和,即
饱和,即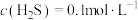 ,通过调节pH使
,通过调节pH使 和
和 形成硫化物而分离。已知:当溶液中离子浓度小于
形成硫化物而分离。已知:当溶液中离子浓度小于 时可认为沉淀完全。25℃时,
时可认为沉淀完全。25℃时, 的电离平衡常数
的电离平衡常数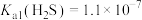 ,
, 。
。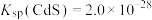 ,
,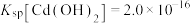 ,
,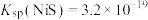 ,
,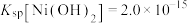 。下列说法不正确的是
。下列说法不正确的是
 饱和,即
饱和,即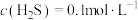 ,通过调节pH使
,通过调节pH使 和
和 形成硫化物而分离。已知:当溶液中离子浓度小于
形成硫化物而分离。已知:当溶液中离子浓度小于 时可认为沉淀完全。25℃时,
时可认为沉淀完全。25℃时, 的电离平衡常数
的电离平衡常数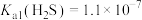 ,
, 。
。 ,
,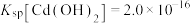 ,
,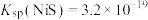 ,
,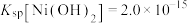 。下列说法不正确的是
。下列说法不正确的是A.CdS固液混合物中,上层清液里含硫微粒主要以 形式存在 形式存在 |
B.将 的 的 溶液稀释到 溶液稀释到 时, 时, 几乎不变 几乎不变 |
C.25℃时,调节 时,废水中的 时,废水中的 和 和 能完全转化为硫化物沉淀 能完全转化为硫化物沉淀 |
D.用NiS固体也能很好地除去溶液中的 |
您最近一年使用:0次
今日更新
|
63次组卷
|
2卷引用:浙江省强基联盟2023-2024学年高二下学期5月月考化学试题
名校
解题方法
7 . 工业上以黄铁矿为原料利用“接触法”制硫酸,并利用硫酸渣(主要含 、
、 、
、 ,其它杂质不考虑)生产铁基颜料铁黄(FeOOH)的制备流程如图所示。
,其它杂质不考虑)生产铁基颜料铁黄(FeOOH)的制备流程如图所示。 外还有
外还有_______ 。
(2)以下有关说法不正确的是_______。
(3)“氧化”中,生成FeOOH的离子方程式为_______ 。
(4)“酸溶”过程中ρ(溶液的质量浓度)及F(溶液的酸度)与w( 质量分数)之间的关系如右图所示。当F值恒定时,随溶液质量浓度增大,所需硫酸的质量分数
质量分数)之间的关系如右图所示。当F值恒定时,随溶液质量浓度增大,所需硫酸的质量分数_______ (填“增大”“减小”或“不变”)。_______ 。
 、
、 、
、 ,其它杂质不考虑)生产铁基颜料铁黄(FeOOH)的制备流程如图所示。
,其它杂质不考虑)生产铁基颜料铁黄(FeOOH)的制备流程如图所示。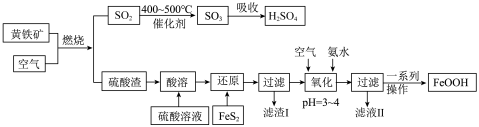
 外还有
外还有(2)以下有关说法不正确的是_______。
A.工业上用98.3%的浓硫酸吸收生成的 |
B. 和 和 都属于酸性氧化物,通到 都属于酸性氧化物,通到 溶液中都会产生白色沉淀 溶液中都会产生白色沉淀 |
C.FeOOH、 中均含有非极性共价键 中均含有非极性共价键 |
D.氟氢化钾(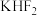 )与发烟硫酸反应可生成氟磺酸( )与发烟硫酸反应可生成氟磺酸(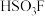 ),说明硫酸的酸性大于氟磺酸 ),说明硫酸的酸性大于氟磺酸 |
(3)“氧化”中,生成FeOOH的离子方程式为
(4)“酸溶”过程中ρ(溶液的质量浓度)及F(溶液的酸度)与w(
 质量分数)之间的关系如右图所示。当F值恒定时,随溶液质量浓度增大,所需硫酸的质量分数
质量分数)之间的关系如右图所示。当F值恒定时,随溶液质量浓度增大,所需硫酸的质量分数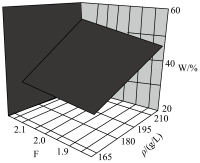
您最近一年使用:0次
名校
解题方法
8 . 下列说法或有关反应的离子方程式不正确 的是
A.与Al反应能放出H2的溶液中:NO 、Na+、Fe3+、SO 、Na+、Fe3+、SO 一定不能大量共存 一定不能大量共存 |
B.铅酸蓄电池充电时的阳极反应: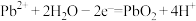 |
C.乙酰甲胺在稀盐酸中水解: |
D.向含溶质a mol的FeBr2溶液中通入b mol Cl2,充分反应,当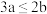 时,反应的离子方程式为: 时,反应的离子方程式为: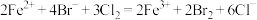 |
您最近一年使用:0次
名校
9 . 某种能将废水中苯酚氧化为 和
和 的原电池—电解池组合装置如图所示,该装置能实现发电、环保二位一体,其中生成的羟基自由基(·OH)有极强的氧化性,下列说法不正确的是
的原电池—电解池组合装置如图所示,该装置能实现发电、环保二位一体,其中生成的羟基自由基(·OH)有极强的氧化性,下列说法不正确的是
 和
和 的原电池—电解池组合装置如图所示,该装置能实现发电、环保二位一体,其中生成的羟基自由基(·OH)有极强的氧化性,下列说法不正确的是
的原电池—电解池组合装置如图所示,该装置能实现发电、环保二位一体,其中生成的羟基自由基(·OH)有极强的氧化性,下列说法不正确的是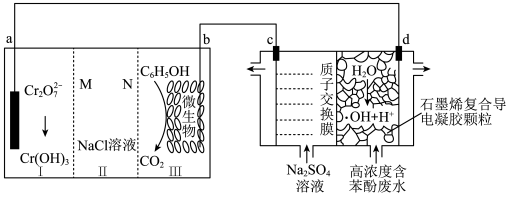
| A.该装置工作时左侧原电池内电路电流通过电解质溶液从电极b流向电极a |
| B.温度过高时该装置处理废水中苯酚的能力会下降 |
C.当电极a上有2mol  生成时,c极区溶液仍为中性 生成时,c极区溶液仍为中性 |
D.当电极b上有0.6mol  生成时,处理苯酚的量为0.1mol 生成时,处理苯酚的量为0.1mol |
您最近一年使用:0次
解题方法
10 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确 的是
实验目的 | 方案设计 | 现象 | 结论 | |
| A | 验证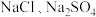 混合溶液中的 混合溶液中的 | 取少量混合溶液于试管中,加入过量 溶液,静置,向上层清液中滴加 溶液,静置,向上层清液中滴加 溶液 溶液 | 若上层清液变浑浊 | 则混合溶液中含有 |
| B | 探究 分子的极性或非极性 分子的极性或非极性 | 用毛皮摩擦过的带电橡胶棒靠近 液流 液流 | 液流方向改变 |  是极性分子 是极性分子 |
| C | 比较 和 和 的酸性 的酸性 | 分别测等物质的量浓度的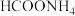 和 和 溶液的pH 溶液的pH | 前者的pH小 | 酸性: > > |
| D | 探究 和 和 的反应{已知 的反应{已知 呈红棕色} 呈红棕色} | 将 气体通入 气体通入 溶液中 溶液中 | 溶液先变为红棕色,过一段时间又变成浅绿色 |  与 与 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



