解题方法
1 . 高铁酸钾( ,
,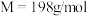 )是一种高效多功能的绿色消毒、净水剂,用途广泛。具体工艺流程如下:
)是一种高效多功能的绿色消毒、净水剂,用途广泛。具体工艺流程如下:
i. 固体易溶于水,微溶于KOH溶液,难溶于乙醚等有机溶剂;
固体易溶于水,微溶于KOH溶液,难溶于乙醚等有机溶剂;
ii. 水溶液稳定性较差,发生反应:
水溶液稳定性较差,发生反应: ;在酸性溶液中快速产生
;在酸性溶液中快速产生 ,在低温、强碱性溶液中相当稳定。
,在低温、强碱性溶液中相当稳定。
(1)检验 溶液中
溶液中 所需试剂名称及相应的实验现象
所需试剂名称及相应的实验现象___________ 。
(2)步骤④的操作名称是___________ 。
(3)步骤①中的离子方程式为___________ 。
(4)下列说法不正确 的是___________(填字母)。
(5) 可用于生活废水的脱氮(将含氮物质如
可用于生活废水的脱氮(将含氮物质如 ,转化为
,转化为 )处理。
)处理。 对生活废水的脱氮效果随水体pH的变化结果如图,试分析pH较小时脱氮效果不好的可能原因
对生活废水的脱氮效果随水体pH的变化结果如图,试分析pH较小时脱氮效果不好的可能原因___________ 。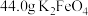 精品与水完全反应,生成标准状况下
精品与水完全反应,生成标准状况下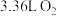 ,该高铁酸钾样品的纯度为
,该高铁酸钾样品的纯度为___________ (用质量分数表示)。
 ,
,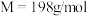 )是一种高效多功能的绿色消毒、净水剂,用途广泛。具体工艺流程如下:
)是一种高效多功能的绿色消毒、净水剂,用途广泛。具体工艺流程如下: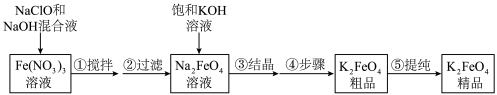
i.
 固体易溶于水,微溶于KOH溶液,难溶于乙醚等有机溶剂;
固体易溶于水,微溶于KOH溶液,难溶于乙醚等有机溶剂;ii.
 水溶液稳定性较差,发生反应:
水溶液稳定性较差,发生反应: ;在酸性溶液中快速产生
;在酸性溶液中快速产生 ,在低温、强碱性溶液中相当稳定。
,在低温、强碱性溶液中相当稳定。(1)检验
 溶液中
溶液中 所需试剂名称及相应的实验现象
所需试剂名称及相应的实验现象(2)步骤④的操作名称是
(3)步骤①中的离子方程式为
(4)下列说法
A.利用上述流程制备 ,可采用将 ,可采用将 通入到NaOH和 通入到NaOH和 的混合体系中实现 的混合体系中实现 |
B. 具有强氧化性可以杀菌消毒,生成的 具有强氧化性可以杀菌消毒,生成的 胶体具有吸附性可以净水 胶体具有吸附性可以净水 |
C.步骤③中反应说明 溶解度小于 溶解度小于 |
D.步骤⑤可用水洗涤 粗品来除去固体表面的杂质,提高产品纯度 粗品来除去固体表面的杂质,提高产品纯度 |
(5)
 可用于生活废水的脱氮(将含氮物质如
可用于生活废水的脱氮(将含氮物质如 ,转化为
,转化为 )处理。
)处理。 对生活废水的脱氮效果随水体pH的变化结果如图,试分析pH较小时脱氮效果不好的可能原因
对生活废水的脱氮效果随水体pH的变化结果如图,试分析pH较小时脱氮效果不好的可能原因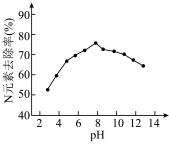
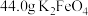 精品与水完全反应,生成标准状况下
精品与水完全反应,生成标准状况下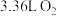 ,该高铁酸钾样品的纯度为
,该高铁酸钾样品的纯度为
您最近一年使用:0次
解题方法
2 . 下列说法正确的是
| A.多电子原子中,离原子核由近到远,电子的能量由高到低 |
| B.汤姆孙原子模型提出原子的中心有个带正电荷的核 |
C. 的酸性强于 的酸性强于 ,所以非金属性:硫>氯 ,所以非金属性:硫>氯 |
| D.元素周期表中副族共有8个 |
您最近一年使用:0次
3 . 25℃时,有关物质平衡常数的数值如表所示:
(1)三种酸由强到弱的顺序是_______ 。
(2)同浓度的CH3COO-、SO 、S2-结合H+能力由大到小的顺序为
、S2-结合H+能力由大到小的顺序为_______ 。
(3)初始浓度为0.1mol/L的CH3COOH溶液pH为_______ 。(已知lg1.3=0.11)
(4)物质的量浓度均为0.1mol/L的CH3COOH和CH3COONa溶液等体积混合(体积变化忽略不计),则下列关于混合溶液的说法中不正确 的是_______ 。
(5)反应H2S(aq)+Cu2+(aq) CuS(s)+2H+(aq)的平衡常数为
CuS(s)+2H+(aq)的平衡常数为_______ (保留小数点后一位)。
| CH3COOH | H2SO3 | H2S | CuS |
| Ka=1.69×10-5 | Ka1=1.54×10-2 Ka2=1.02×10-7 | Ka1=1.1×10-7 Ka2=1.0×10-13 | Ksp=6.0×10-36 |
(2)同浓度的CH3COO-、SO
 、S2-结合H+能力由大到小的顺序为
、S2-结合H+能力由大到小的顺序为(3)初始浓度为0.1mol/L的CH3COOH溶液pH为
(4)物质的量浓度均为0.1mol/L的CH3COOH和CH3COONa溶液等体积混合(体积变化忽略不计),则下列关于混合溶液的说法中
| A.c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-) |
| B.c(Na+)-c(OH-)=c(CH3COO-)-c(H+) |
| C.c(CH3COOH)+c(CH3COO-)=0.2mol/L |
| D.c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
 CuS(s)+2H+(aq)的平衡常数为
CuS(s)+2H+(aq)的平衡常数为
您最近一年使用:0次
4 . 常温时,碳酸钙和硫酸钙的沉淀溶解平衡关系如图所示,已知 ,
, (酸根离子)=
(酸根离子)=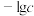 (酸根离子)。[已知:
(酸根离子)。[已知: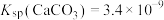 ,
,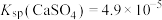 ]下列说法不正确的是
]下列说法不正确的是
 ,
, (酸根离子)=
(酸根离子)=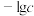 (酸根离子)。[已知:
(酸根离子)。[已知: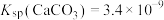 ,
,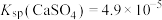 ]下列说法不正确的是
]下列说法不正确的是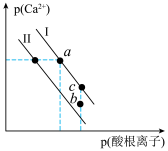
A.曲线Ⅱ为 沉淀溶解曲线 沉淀溶解曲线 |
| B.加入适量的氯化钙固体,可使溶液由c点变到a点 |
| C.b点对应的硫酸钙溶液不饱和 |
D.向碳酸钙饱和溶液中通入 气体,溶液中 气体,溶液中 不变 不变 |
您最近一年使用:0次
5 . 下列说法不正确 的是
| A.碘单质受热变成气体,冷却后又成晶体,此过程中化学键没有发生变化 |
B. 、 、 、 、 的状态由气态到固态变化的主要原因是分子间作用力逐渐增大 的状态由气态到固态变化的主要原因是分子间作用力逐渐增大 |
C. 在水中电离只破坏离子键 在水中电离只破坏离子键 |
| D.DNA的结构和生理活性都与氢键的作用有关 |
您最近一年使用:0次
7日内更新
|
30次组卷
|
2卷引用:浙江省衢州市2023-2024学年高一上学期教学质量检测 化学试题
6 . 一定条件下,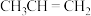 与
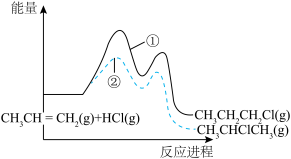
与 发生加成反应有①、②两种可能,反应进程中能量变化如图所示。下列说法正确的是
发生加成反应有①、②两种可能,反应进程中能量变化如图所示。下列说法正确的是
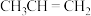 与
与 发生加成反应有①、②两种可能,反应进程中能量变化如图所示。下列说法正确的是
发生加成反应有①、②两种可能,反应进程中能量变化如图所示。下列说法正确的是
A.生成等物质的量  比 比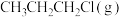 吸收的热量更多 吸收的热量更多 |
B.反应刚开始时,产物中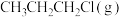 的比例更大 的比例更大 |
C.适当提高反应温度,可以提高产物中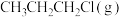 的比例 的比例 |
| D.反应①、反应②对应生成物的总键能相同 |
您最近一年使用:0次
名校
7 . 自由能大小可以反映物质氧化能力的相对强弱。锰元素的自由能-氧化态图如图所示,下列说法不正确 的是

A.碱性条件下 易被还原为 易被还原为 |
B.碱性条件下 ;的氧化能力明显降低 ;的氧化能力明显降低 |
C. 中Mn为+7价 中Mn为+7价 |
D.酸性条件下1mol ,被充分还原,则转移5mol电子 ,被充分还原,则转移5mol电子 |
您最近一年使用:0次
2024-09-16更新
|
328次组卷
|
2卷引用:浙江省衢州市2023-2024学年高一上学期教学质量检测 化学试题
解题方法
8 . 常温下,用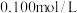 NaOH溶液滴定20mL
NaOH溶液滴定20mL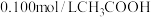 溶液所得滴定曲线如图所示。下列说法正确的是
溶液所得滴定曲线如图所示。下列说法正确的是
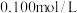 NaOH溶液滴定20mL
NaOH溶液滴定20mL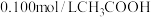 溶液所得滴定曲线如图所示。下列说法正确的是
溶液所得滴定曲线如图所示。下列说法正确的是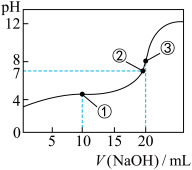
A.点①所示溶液溶质为 和 和 ,且 ,且 |
B.点②所示溶液中: |
| C.点①、②、③所示溶液中,水的电离程度最大的是③ |
D.滴定过程中可能出现: |
您最近一年使用:0次
9 . 某纳米材料 仅由两种元素组成,其摩尔质量为
仅由两种元素组成,其摩尔质量为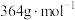 ,气体
,气体 能使湿润的红色石蕊试纸变蓝。可以发生如图转化(X、A、B、C均为化合物):
能使湿润的红色石蕊试纸变蓝。可以发生如图转化(X、A、B、C均为化合物):
(1)固体 的组成元素为
的组成元素为___________ (用元素符号表示),沉淀 的化学式为
的化学式为___________ 。
(2)气体C与氧气通入水中生成溶液D的离子方程式为___________ 。
(3)固体 在潮湿空气加热发生反应的化学方程式为
在潮湿空气加热发生反应的化学方程式为___________ 。
(4)设计实验检验溶液 中的阳离子
中的阳离子___________ 。
 仅由两种元素组成,其摩尔质量为
仅由两种元素组成,其摩尔质量为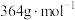 ,气体
,气体 能使湿润的红色石蕊试纸变蓝。可以发生如图转化(X、A、B、C均为化合物):
能使湿润的红色石蕊试纸变蓝。可以发生如图转化(X、A、B、C均为化合物):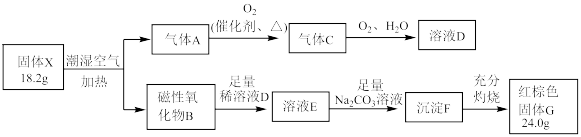
(1)固体
 的组成元素为
的组成元素为 的化学式为
的化学式为(2)气体C与氧气通入水中生成溶液D的离子方程式为
(3)固体
 在潮湿空气加热发生反应的化学方程式为
在潮湿空气加热发生反应的化学方程式为(4)设计实验检验溶液
 中的阳离子
中的阳离子
您最近一年使用:0次
2024-09-11更新
|
38次组卷
|
2卷引用:浙江省温州市2023-2024学年高一上学期期末教学质量统一检测化学试题A
解题方法
10 . 把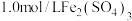 溶液与
溶液与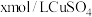 溶液各取
溶液各取 混合(假设混合溶液的体积等于混合前两种溶液的体积之和)。
混合(假设混合溶液的体积等于混合前两种溶液的体积之和)。
(1)此混合溶液中 的浓度为
的浓度为_____________ 。
(2)向混合溶液中加入足量铁粉,充分反应后(忽略溶液体积的变化),测得溶液中 的浓度为
的浓度为 ,则
,则
____________ 。
(3)若向混合溶液中加入一定量的铁粉,充分反应后,过滤出不溶物,溶液质量增重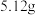 ,则反应后的溶液中
,则反应后的溶液中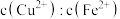 为
为____________ 。
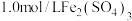 溶液与
溶液与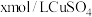 溶液各取
溶液各取 混合(假设混合溶液的体积等于混合前两种溶液的体积之和)。
混合(假设混合溶液的体积等于混合前两种溶液的体积之和)。(1)此混合溶液中
 的浓度为
的浓度为(2)向混合溶液中加入足量铁粉,充分反应后(忽略溶液体积的变化),测得溶液中
 的浓度为
的浓度为 ,则
,则
(3)若向混合溶液中加入一定量的铁粉,充分反应后,过滤出不溶物,溶液质量增重
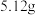 ,则反应后的溶液中
,则反应后的溶液中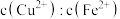 为
为
您最近一年使用:0次



