解题方法
1 . 水溶液中的离子反应与平衡在生产和生活中有着广泛的用途。
(1)相同条件下,pH=10的氨水和pH=10的氢氧化钠溶液,水的电离程度_______ (填“前者大”、“后者大”或“相同”)。向氨水中滴加同浓度的CH3COOH溶液,滴加过程中
_______ (填“增大”、“减小”或“不变”)。
(2)Na2S又称臭碱、硫化碱,用离子方程式说明Na2S溶液呈碱性的原因_______ 。Na2S溶液中,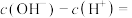
_______ (写出表达式,不含Na+)。
(3)常温下,向5mL浓度为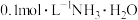 溶液中加入0.1molNH4NO3晶体(假设溶液体积不变),溶液呈中性,则NH3⋅H2O的电离平衡常数
溶液中加入0.1molNH4NO3晶体(假设溶液体积不变),溶液呈中性,则NH3⋅H2O的电离平衡常数
_______ 。
(4)烟气中的SO2可以用钠碱循环法加以处理,用Na2SO3溶液作为吸收液。25℃, 、
、 、
、 的物质的量分数
的物质的量分数 与pH的关系如图1所示。当吸收液pH降低为一定数值时,又可将吸收液通入如图2所示的电解槽(电极为惰性电极)进行再生。
与pH的关系如图1所示。当吸收液pH降低为一定数值时,又可将吸收液通入如图2所示的电解槽(电极为惰性电极)进行再生。_______ ;
②当吸收液pH=5.9时,可进行再生至pH≥8.9,其中 放电的电极反应式为
放电的电极反应式为_______ ,再生后的吸收液中 的最小值为
的最小值为_______ ,此时若有1molNa+通过离子交换膜,则再生后溶液中的 的物质的量为
的物质的量为_______ (保留一位小数,假设左室中溶液体积为1L,忽略体积变化)。
(1)相同条件下,pH=10的氨水和pH=10的氢氧化钠溶液,水的电离程度

(2)Na2S又称臭碱、硫化碱,用离子方程式说明Na2S溶液呈碱性的原因
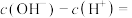
(3)常温下,向5mL浓度为
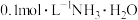 溶液中加入0.1molNH4NO3晶体(假设溶液体积不变),溶液呈中性,则NH3⋅H2O的电离平衡常数
溶液中加入0.1molNH4NO3晶体(假设溶液体积不变),溶液呈中性,则NH3⋅H2O的电离平衡常数
(4)烟气中的SO2可以用钠碱循环法加以处理,用Na2SO3溶液作为吸收液。25℃,
 、
、 、
、 的物质的量分数
的物质的量分数 与pH的关系如图1所示。当吸收液pH降低为一定数值时,又可将吸收液通入如图2所示的电解槽(电极为惰性电极)进行再生。
与pH的关系如图1所示。当吸收液pH降低为一定数值时,又可将吸收液通入如图2所示的电解槽(电极为惰性电极)进行再生。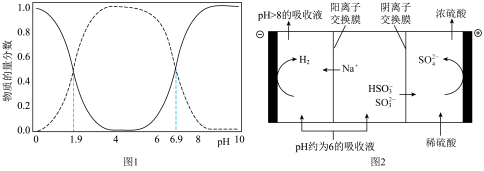
②当吸收液pH=5.9时,可进行再生至pH≥8.9,其中
 放电的电极反应式为
放电的电极反应式为 的最小值为
的最小值为 的物质的量为
的物质的量为
您最近一年使用:0次
2 . 药物贝诺酯由乙酰水杨酸和对乙酰氨基酚制备,其原理为
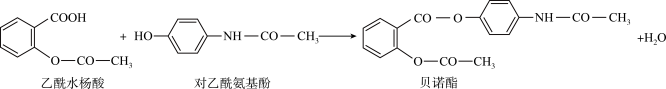
| A.乙酰水杨酸分子中所有碳原子可共平面 |
| B.对乙酰氨基酚的核磁共振碳谱有5组峰 |
| C.对乙酰氨基酚在一定条件下可与甲醛反应 |
| D.贝诺酯在酸性条件下充分水解可得到3种产物 |
您最近一年使用:0次
3 . 测定平衡常数对定量认识化学反应具有重要意义。已知: 能与
能与 反应生成
反应生成 ,在水溶液中建立平衡:
,在水溶液中建立平衡: 。通过测定平衡体系中的
。通过测定平衡体系中的 、
、 和
和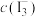 ,就可求得该反应的平衡常数。回答下列问题:
,就可求得该反应的平衡常数。回答下列问题:
I.同学甲为测定上述平衡体系中 ,采取如下方法:取
,采取如下方法:取 上述平衡体系的混合溶液,用
上述平衡体系的混合溶液,用 的
的 溶液进行滴定(反应为
溶液进行滴定(反应为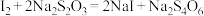 ),消耗
),消耗 溶液
溶液 。根据
。根据 、
、 和c可求得
和c可求得 。
。
(1)上述滴定时,可采用___________ 作指示剂,滴定终点的现象为___________ 。
(2)同学乙认为该甲设计方案不合理,原因是甲测得的 实际为平衡体系中
实际为平衡体系中___________ 的物质的量浓度之和(填化学式)。
Ⅱ.乙对上述方案进行改进,室温下测定水溶液中该反应平衡常数的过程如下(溶液体积变化忽略不计): 和
和 不溶于
不溶于 ;室温下,碘单质在四氯化碳和水混合液体中的浓度比值即
;室温下,碘单质在四氯化碳和水混合液体中的浓度比值即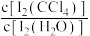 是常数(用Kd表示,称为分配系数),室温条件下Kd=85。
是常数(用Kd表示,称为分配系数),室温条件下Kd=85。
(3)操作I的名称为___________ 。
(4)若分别用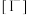 、
、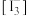 、
、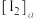 表示
表示上层 液体中 、
、 和
和 的物质的量浓度,用
的物质的量浓度,用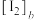 表示
表示下层 液体中 的物质的量浓度,则反应
的物质的量浓度,则反应 的平衡常数K的表达式为
的平衡常数K的表达式为___________ ,上层液体中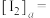
___________  。
。
(5)实验测得上层溶液 的c( )=0.0045 mol·L-1,结合上述有关数据,计算出该反应的平衡常数K=
)=0.0045 mol·L-1,结合上述有关数据,计算出该反应的平衡常数K=___________ (保留三位有效数字)。
 能与
能与 反应生成
反应生成 ,在水溶液中建立平衡:
,在水溶液中建立平衡: 。通过测定平衡体系中的
。通过测定平衡体系中的 、
、 和
和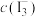 ,就可求得该反应的平衡常数。回答下列问题:
,就可求得该反应的平衡常数。回答下列问题:I.同学甲为测定上述平衡体系中
 ,采取如下方法:取
,采取如下方法:取 上述平衡体系的混合溶液,用
上述平衡体系的混合溶液,用 的
的 溶液进行滴定(反应为
溶液进行滴定(反应为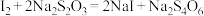 ),消耗
),消耗 溶液
溶液 。根据
。根据 、
、 和c可求得
和c可求得 。
。(1)上述滴定时,可采用
(2)同学乙认为该甲设计方案不合理,原因是甲测得的
 实际为平衡体系中
实际为平衡体系中Ⅱ.乙对上述方案进行改进,室温下测定水溶液中该反应平衡常数的过程如下(溶液体积变化忽略不计):
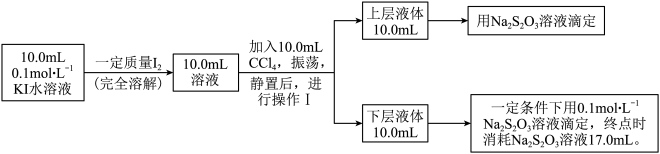
 和
和 不溶于
不溶于 ;室温下,碘单质在四氯化碳和水混合液体中的浓度比值即
;室温下,碘单质在四氯化碳和水混合液体中的浓度比值即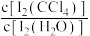 是常数(用Kd表示,称为分配系数),室温条件下Kd=85。
是常数(用Kd表示,称为分配系数),室温条件下Kd=85。(3)操作I的名称为
(4)若分别用
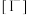 、
、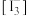 、
、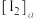 表示
表示 、
、 和
和 的物质的量浓度,用
的物质的量浓度,用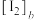 表示
表示 的物质的量浓度,则反应
的物质的量浓度,则反应 的平衡常数K的表达式为
的平衡常数K的表达式为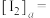
 。
。(5)实验测得
 )=0.0045 mol·L-1,结合上述有关数据,计算出该反应的平衡常数K=
)=0.0045 mol·L-1,结合上述有关数据,计算出该反应的平衡常数K=
您最近一年使用:0次
解题方法
4 . 燃煤废气中的 转化为二甲醚的反应原理为:
转化为二甲醚的反应原理为: ,一定条件下,现有两个体积均为2.0L恒容密闭容器甲和乙,在容器甲中充入1mol
,一定条件下,现有两个体积均为2.0L恒容密闭容器甲和乙,在容器甲中充入1mol 和3mol
和3mol ,在容器乙中充入2mol
,在容器乙中充入2mol 和6mol
和6mol ,发生上述反应并达到平衡。该反应中
,发生上述反应并达到平衡。该反应中 的平衡转化率随温度的变化曲线如图1所示;容器甲中,在不同催化剂作用下,相同时间内
的平衡转化率随温度的变化曲线如图1所示;容器甲中,在不同催化剂作用下,相同时间内 的转化率随温度变化如图2所示。下列说法正确的是
的转化率随温度变化如图2所示。下列说法正确的是
 转化为二甲醚的反应原理为:
转化为二甲醚的反应原理为: ,一定条件下,现有两个体积均为2.0L恒容密闭容器甲和乙,在容器甲中充入1mol
,一定条件下,现有两个体积均为2.0L恒容密闭容器甲和乙,在容器甲中充入1mol 和3mol
和3mol ,在容器乙中充入2mol
,在容器乙中充入2mol 和6mol
和6mol ,发生上述反应并达到平衡。该反应中
,发生上述反应并达到平衡。该反应中 的平衡转化率随温度的变化曲线如图1所示;容器甲中,在不同催化剂作用下,相同时间内
的平衡转化率随温度的变化曲线如图1所示;容器甲中,在不同催化剂作用下,相同时间内 的转化率随温度变化如图2所示。下列说法正确的是
的转化率随温度变化如图2所示。下列说法正确的是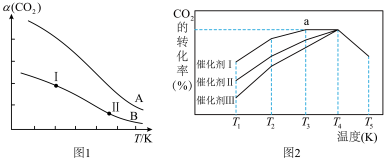
A.图1中,表示乙容器 的平衡转化率随温度变化的是曲线B 的平衡转化率随温度变化的是曲线B |
B.图1中,逆反应速率 :状态I<状态Ⅱ :状态I<状态Ⅱ |
| C.图2中,a点达到化学平衡状态 |
D.图2中, 对应的平衡常数小于 对应的平衡常数小于 对应的平衡常数 对应的平衡常数 |
您最近一年使用:0次
5 . 二氯异氰尿酸钠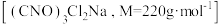 是一种高效广谱杀菌消毒剂,常温下为白色固体,难溶于冷水。实验室中,先向NaOH溶液通入
是一种高效广谱杀菌消毒剂,常温下为白色固体,难溶于冷水。实验室中,先向NaOH溶液通入 产生高浓度NaClO溶液,再与氰尿酸
产生高浓度NaClO溶液,再与氰尿酸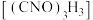 吡啶溶液反应制备二氯异氰尿酸钠并测其纯度。
吡啶溶液反应制备二氯异氰尿酸钠并测其纯度。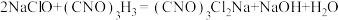 ,该反应为放热反应。
,该反应为放热反应。
回答下列问题:
(1)装置A中a的作用为_______ ,装置C中试剂可选用_______ 。
(2)装置存在一处缺陷,会导致装置B中NaOH的利用率降低,改进方法是_______ 。
(3)三颈烧瓶液面上方出现黄绿色气体时,由上口加入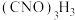 的吡啶溶液,反应过程中仍需不断通入
的吡啶溶液,反应过程中仍需不断通入 ,原因是
,原因是_______ 。
(4)反应结束后,B中浊液经过滤、_______ 、干燥得到粗产品。
(5)利用碘量法测定粗产品中二氯异氰尿酸钠的纯度,原理为:
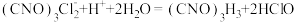 ;
;
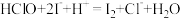 ;
;
 。
。
准确称取 粗产品,溶于无氧蒸馏水配成100mL溶液;取25.00mL溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入淀粉溶液作指示剂,用
粗产品,溶于无氧蒸馏水配成100mL溶液;取25.00mL溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入淀粉溶液作指示剂,用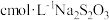 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 。
。
①滴定终点的现象是:当滴入最后半滴标准溶液时,_______ 。
②粗产品中二氯异氰尿酸钠的纯度为_______ %(用含m、c、V的代数式表示)。
③若碘量瓶中加入稀硫酸的量过少,将导致粗产品中二氯异氰尿酸钠的纯度_______ (填“偏低”“偏高”或“无影响”)。
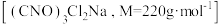 是一种高效广谱杀菌消毒剂,常温下为白色固体,难溶于冷水。实验室中,先向NaOH溶液通入
是一种高效广谱杀菌消毒剂,常温下为白色固体,难溶于冷水。实验室中,先向NaOH溶液通入 产生高浓度NaClO溶液,再与氰尿酸
产生高浓度NaClO溶液,再与氰尿酸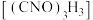 吡啶溶液反应制备二氯异氰尿酸钠并测其纯度。
吡啶溶液反应制备二氯异氰尿酸钠并测其纯度。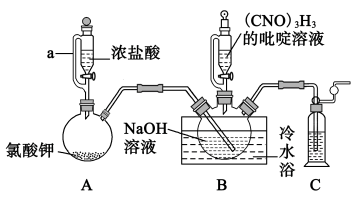
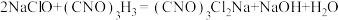 ,该反应为放热反应。
,该反应为放热反应。回答下列问题:
(1)装置A中a的作用为
(2)装置存在一处缺陷,会导致装置B中NaOH的利用率降低,改进方法是
(3)三颈烧瓶液面上方出现黄绿色气体时,由上口加入
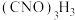 的吡啶溶液,反应过程中仍需不断通入
的吡啶溶液,反应过程中仍需不断通入 ,原因是
,原因是(4)反应结束后,B中浊液经过滤、
(5)利用碘量法测定粗产品中二氯异氰尿酸钠的纯度,原理为:
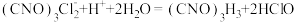 ;
;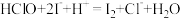 ;
; 。
。准确称取
 粗产品,溶于无氧蒸馏水配成100mL溶液;取25.00mL溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入淀粉溶液作指示剂,用
粗产品,溶于无氧蒸馏水配成100mL溶液;取25.00mL溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入淀粉溶液作指示剂,用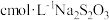 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 。
。①滴定终点的现象是:当滴入最后半滴标准溶液时,
②粗产品中二氯异氰尿酸钠的纯度为
③若碘量瓶中加入稀硫酸的量过少,将导致粗产品中二氯异氰尿酸钠的纯度
您最近一年使用:0次
解题方法
6 . 含氮物质种类繁多,实验小组对不同含氮物质做了相关研究。
(1) 能与
能与 形成具有对称空间结构的
形成具有对称空间结构的 。若
。若 中两个
中两个 分别被
分别被 取代,能得到a、b两种不同结构的
取代,能得到a、b两种不同结构的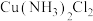 :
:_______ b(填“>”“<”或“=”)。
② 的空间结构为
的空间结构为_______ ,1mol 中含有配位键的数目为
中含有配位键的数目为_______ (用 表示)。
表示)。
(2)乙二胺 是二元弱碱,分步电离,在水中的电离类似于氨。25℃时,乙二胺溶液中各含氮微粒的物质的量分数
是二元弱碱,分步电离,在水中的电离类似于氨。25℃时,乙二胺溶液中各含氮微粒的物质的量分数 与溶液
与溶液 的关系如图。
的关系如图。 在水中的第二步电离方程式为
在水中的第二步电离方程式为_______ ;乙二胺一级电离平衡常数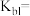
_______ 。
②C点的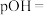
_______ 。
③将盐酸滴入乙二胺溶液中,pOH由4.9增大到7.9的过程中,水的电离程度_______ (填“增大”“减小”“先增大后减小”或“先减小后增大”);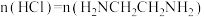 时,溶液中
时,溶液中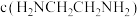
_______ 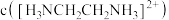 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)
 能与
能与 形成具有对称空间结构的
形成具有对称空间结构的 。若
。若 中两个
中两个 分别被
分别被 取代,能得到a、b两种不同结构的
取代,能得到a、b两种不同结构的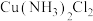 :
:
②
 的空间结构为
的空间结构为 中含有配位键的数目为
中含有配位键的数目为 表示)。
表示)。(2)乙二胺
 是二元弱碱,分步电离,在水中的电离类似于氨。25℃时,乙二胺溶液中各含氮微粒的物质的量分数
是二元弱碱,分步电离,在水中的电离类似于氨。25℃时,乙二胺溶液中各含氮微粒的物质的量分数 与溶液
与溶液 的关系如图。
的关系如图。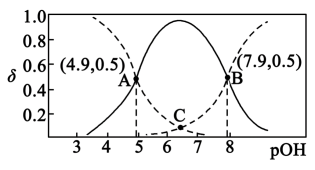
 在水中的第二步电离方程式为
在水中的第二步电离方程式为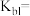
②C点的
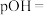
③将盐酸滴入乙二胺溶液中,pOH由4.9增大到7.9的过程中,水的电离程度
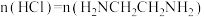 时,溶液中
时,溶液中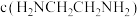
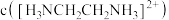 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
解题方法
7 . 含碳化合物对环境、生产和人类生命活动有很大影响。回答下列有关问题:
(1)在催化剂作用下, 可实现如下转化:
可实现如下转化:_______ ,其在周期表中的位置为_______ ,乙中碳原子的杂化方式有_______ 种。
(2)工业上以 为碳源可以合成乙醇和二甲醚
为碳源可以合成乙醇和二甲醚 ,乙醇的沸点高于二甲醚,试解释原因
,乙醇的沸点高于二甲醚,试解释原因_______ 。
(3)光气 是一种有毒气体,其组成元素的电负性由大到小的顺序为
是一种有毒气体,其组成元素的电负性由大到小的顺序为_______ ;若把光气分子中的氯原子换成氟原子,推测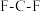 键角
键角_______ 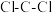 键角(填“>”“<”或“=”)。
键角(填“>”“<”或“=”)。
(4) 甲基咪唑(
甲基咪唑( )的离子液体有利于
)的离子液体有利于 水合物生成,该物质中大
水合物生成,该物质中大 键可表示为
键可表示为_______ (大 键可用
键可用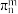 表示,m、n分别代表参与形成大
表示,m、n分别代表参与形成大 键的电子数和原子数);
键的电子数和原子数);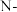 甲基咪唑(
甲基咪唑(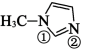 )中
)中_______ (填“①”或“②”)号N原子更容易形成配位键。
(1)在催化剂作用下,
 可实现如下转化:
可实现如下转化: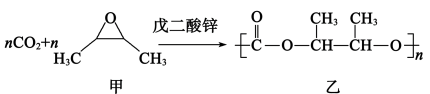
(2)工业上以
 为碳源可以合成乙醇和二甲醚
为碳源可以合成乙醇和二甲醚 ,乙醇的沸点高于二甲醚,试解释原因
,乙醇的沸点高于二甲醚,试解释原因(3)光气
 是一种有毒气体,其组成元素的电负性由大到小的顺序为
是一种有毒气体,其组成元素的电负性由大到小的顺序为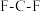 键角
键角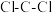 键角(填“>”“<”或“=”)。
键角(填“>”“<”或“=”)。(4)
 甲基咪唑(
甲基咪唑( )的离子液体有利于
)的离子液体有利于 水合物生成,该物质中大
水合物生成,该物质中大 键可表示为
键可表示为 键可用
键可用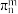 表示,m、n分别代表参与形成大
表示,m、n分别代表参与形成大 键的电子数和原子数);
键的电子数和原子数);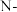 甲基咪唑(
甲基咪唑( )中
)中
您最近一年使用:0次
解题方法
8 . 已知 是难溶于水、可溶于酸的盐。常温下用HCl调节
是难溶于水、可溶于酸的盐。常温下用HCl调节 浊液的pH,测得体系中
浊液的pH,测得体系中 (X为
(X为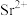 或
或 )与
)与 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是
 是难溶于水、可溶于酸的盐。常温下用HCl调节
是难溶于水、可溶于酸的盐。常温下用HCl调节 浊液的pH,测得体系中
浊液的pH,测得体系中 (X为
(X为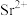 或
或 )与
)与 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是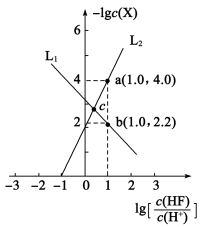
A. 代表 代表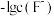 与 与 的变化曲线 的变化曲线 |
B. 的数量级为 的数量级为 |
C.a点, |
D.c点,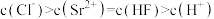 |
您最近一年使用:0次
解题方法
9 . 室温下,用含少量 的
的 溶液制备
溶液制备 的过程如图。下列说法正确的是
的过程如图。下列说法正确的是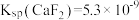 ,
,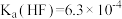 ;
;
②当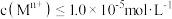 ,可认为
,可认为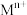 离子沉淀完全。
离子沉淀完全。
 的
的 溶液制备
溶液制备 的过程如图。下列说法正确的是
的过程如图。下列说法正确的是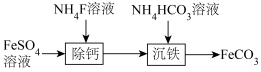
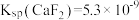 ,
,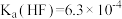 ;
;②当
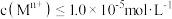 ,可认为
,可认为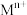 离子沉淀完全。
离子沉淀完全。A.配制 溶液时需加盐酸抑制 溶液时需加盐酸抑制 水解 水解 |
B. 溶液中: 溶液中: |
C.为确保 沉淀完全,除钙后的溶液中氟离子浓度至少为 沉淀完全,除钙后的溶液中氟离子浓度至少为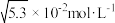 |
D.“沉铁”时发生反应的离子方程式: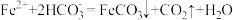 |
您最近一年使用:0次
解题方法
10 . 下列离子方程式书写正确的是
A. 除去废水中的 除去废水中的 : :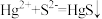 |
B. 溶液与少量 溶液与少量 溶液反应: 溶液反应: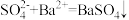 |
C.向 溶液中滴加 溶液中滴加 溶液: 溶液: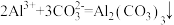 |
D.向 溶液中加入过量浓氨水: 溶液中加入过量浓氨水: |
您最近一年使用:0次



