1 . 已知相同温度下,Ksp(BaSO4)<Ksp(BaCO3)。某温度下,饱和溶液中-lg[c( )]、-lg[c(
)]、-lg[c( )]与-lg[c(Ba2+)]的关系如图所示。
)]与-lg[c(Ba2+)]的关系如图所示。
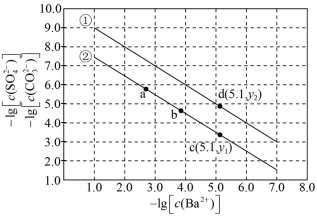
下列说法正确的是
 )]、-lg[c(
)]、-lg[c( )]与-lg[c(Ba2+)]的关系如图所示。
)]与-lg[c(Ba2+)]的关系如图所示。
下列说法正确的是
| A.曲线①代表BaCO3的沉淀溶解曲线 |
| B.该温度下BaSO4的Ksp(BaSO4)值为1.0×10-10 |
| C.加适量BaCl2固体可使溶液由a点变到b点 |
D.c(Ba2+)=10-5.1 mol/L时,两溶液中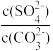 =10 =10 |
您最近一年使用:0次
名校
解题方法
2 . 一种从阳极泥(主要成分为Cu、Ag、Pt、Au、 、
、 等)中回收Se和贵重金属的工艺流程如图所示:
等)中回收Se和贵重金属的工艺流程如图所示:
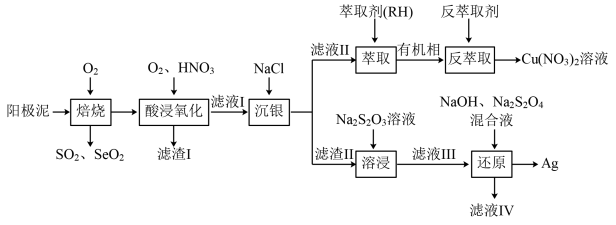
已知:①该工艺中萃取与反萃取的原理为: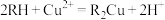 。
。
② 易与
易与 形成配离子:
形成配离子: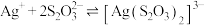 ,上述工艺条件下该反应的平衡常数为
,上述工艺条件下该反应的平衡常数为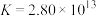 。
。
③上述工艺条件下,AgCl的溶度积常数: 。
。
(1)“焙烧”产生的; 与
与 的混合烟气可用水吸收制得单质Se,该反应的化学方程式为
的混合烟气可用水吸收制得单质Se,该反应的化学方程式为____________ 。
(2)“滤渣Ⅰ”的主要成分是______ (填化学式);“酸浸氧化”中通入氧气,体现了绿色化学的思想,其目的是____________ 。
(3)“反萃取剂”最好选用______ (填化学式)溶液。
(4)“溶浸”过程中滤渣Ⅱ被 溶液溶解,发生反应的平衡常数为
溶液溶解,发生反应的平衡常数为______ 。
(5)“还原”过程中; 没有参与氧化还原过程,“滤液Ⅳ”中还主要含有
没有参与氧化还原过程,“滤液Ⅳ”中还主要含有 。“还原”过程中氧化剂与还原剂的物质的量之比为
。“还原”过程中氧化剂与还原剂的物质的量之比为______ 。
(6)为减少工艺中试剂用量,“滤液Ⅳ”可返回______ (填工序名称)工序循环使用。
 、
、 等)中回收Se和贵重金属的工艺流程如图所示:
等)中回收Se和贵重金属的工艺流程如图所示:
已知:①该工艺中萃取与反萃取的原理为:
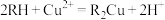 。
。②
 易与
易与 形成配离子:
形成配离子: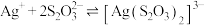 ,上述工艺条件下该反应的平衡常数为
,上述工艺条件下该反应的平衡常数为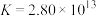 。
。③上述工艺条件下,AgCl的溶度积常数:
 。
。(1)“焙烧”产生的;
 与
与 的混合烟气可用水吸收制得单质Se,该反应的化学方程式为
的混合烟气可用水吸收制得单质Se,该反应的化学方程式为(2)“滤渣Ⅰ”的主要成分是
(3)“反萃取剂”最好选用
(4)“溶浸”过程中滤渣Ⅱ被
 溶液溶解,发生反应的平衡常数为
溶液溶解,发生反应的平衡常数为(5)“还原”过程中;
 没有参与氧化还原过程,“滤液Ⅳ”中还主要含有
没有参与氧化还原过程,“滤液Ⅳ”中还主要含有 。“还原”过程中氧化剂与还原剂的物质的量之比为
。“还原”过程中氧化剂与还原剂的物质的量之比为(6)为减少工艺中试剂用量,“滤液Ⅳ”可返回
您最近一年使用:0次
名校
3 .  时,某混合溶液中
时,某混合溶液中 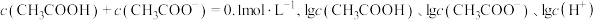 和
和 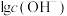 随
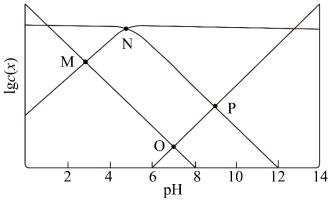
随 变化的关系如下图所示。
变化的关系如下图所示。  为
为 的电离常数,下列说法正确的是
的电离常数,下列说法正确的是
 时,某混合溶液中
时,某混合溶液中 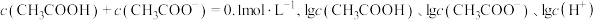 和
和 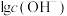 随
随 变化的关系如下图所示。
变化的关系如下图所示。  为
为 的电离常数,下列说法正确的是
的电离常数,下列说法正确的是
A. 时, 时, |
B. 点时, 点时, |
C.该体系中,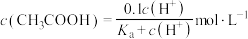 |
D. 由7到 由7到  的变化过程中, 的变化过程中, 的水解程度始终增大 的水解程度始终增大 |
您最近一年使用:0次
解题方法
4 . 聚丙烯是生产医用无纺布口罩及防护服的材料。丙烯是制造聚丙烯的单体。工业上制备丙烯的方法有多种,回答下列问题:
Ⅰ.以异丙醇为原料制备丙烯。已知:
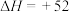 kJ⋅mol
kJ⋅mol 。
。
已知几种共价键键能如表所示:
(1)该反应在______ (填“较高”“较低”或“任意”)温度下能自发进行。
(2)C=C键键能为______ kJ⋅mol 。
。
Ⅱ.中国某课题组开发富含硼氧活性位点的热稳定层柱状框架类材料助力丙烷氧化脱氢。
有关反应如下:
反应1: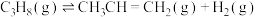

反应2: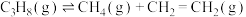

(3)向密闭容器中充入1 mol ,同时发生反应1和反应2,升高温度,氢气的体积分数增大。
,同时发生反应1和反应2,升高温度,氢气的体积分数增大。
当达到平衡时,测得丙烯的体积分数与温度、压强的关系如图1所示。
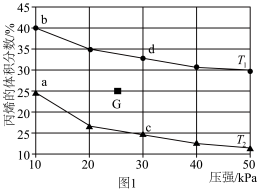
①其他条件相同,增大压强,丙烯体积分数减小的原因是____________ 。
②b点时丙烯与乙烯的体积之比为10∶1,丙烷的平衡转化率为______ (保留3位有效数字)。
③下列物理量中,图中c点大于d点的是______ (填标号)。
A.正反应速率 B.对应温度下反应1的平衡常数
C.逆反应速率 D.平均摩尔质量
④当降温的同时,缩小容器的体积,G点对应的平衡体系达到新平衡时丙烯的体积分数可能对应图中的______ (填“a”“b”“c”或“d”)点。
(4)一定温度下,总压保持为p时,向反应器中充入 和
和 ,发生反应1和反应2,测得丙烷的平衡转化率与投料比
,发生反应1和反应2,测得丙烷的平衡转化率与投料比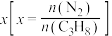 的关系如图2所示。
的关系如图2所示。
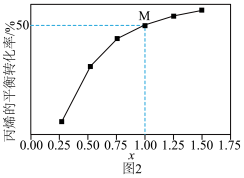
①向反应器中充入 的目的是
的目的是____________ 。
②该温度下,M点丙烯的选择性为66.7%,此时反应1的平衡常数 为
为______ 。
提示:(ⅰ)用分压计算的平衡常数为 ,分压=总压×物质的量分数。
,分压=总压×物质的量分数。
(ⅱ)丙烯的选择性 。
。
Ⅰ.以异丙醇为原料制备丙烯。已知:

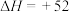 kJ⋅mol
kJ⋅mol 。
。已知几种共价键键能如表所示:
| 共价键 | H-C | C-C | C-C | C-O | H-O |
键能/(kJ⋅mol ) ) | 413 | 347 | E | 326 | 467 |
(1)该反应在
(2)C=C键键能为
 。
。Ⅱ.中国某课题组开发富含硼氧活性位点的热稳定层柱状框架类材料助力丙烷氧化脱氢。
有关反应如下:
反应1:
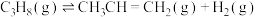

反应2:
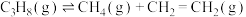

(3)向密闭容器中充入1 mol
 ,同时发生反应1和反应2,升高温度,氢气的体积分数增大。
,同时发生反应1和反应2,升高温度,氢气的体积分数增大。当达到平衡时,测得丙烯的体积分数与温度、压强的关系如图1所示。

①其他条件相同,增大压强,丙烯体积分数减小的原因是
②b点时丙烯与乙烯的体积之比为10∶1,丙烷的平衡转化率为
③下列物理量中,图中c点大于d点的是
A.正反应速率 B.对应温度下反应1的平衡常数
C.逆反应速率 D.平均摩尔质量
④当降温的同时,缩小容器的体积,G点对应的平衡体系达到新平衡时丙烯的体积分数可能对应图中的
(4)一定温度下,总压保持为p时,向反应器中充入
 和
和 ,发生反应1和反应2,测得丙烷的平衡转化率与投料比
,发生反应1和反应2,测得丙烷的平衡转化率与投料比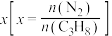 的关系如图2所示。
的关系如图2所示。
①向反应器中充入
 的目的是
的目的是②该温度下,M点丙烯的选择性为66.7%,此时反应1的平衡常数
 为
为提示:(ⅰ)用分压计算的平衡常数为
 ,分压=总压×物质的量分数。
,分压=总压×物质的量分数。(ⅱ)丙烯的选择性
 。
。
您最近一年使用:0次
2024-02-25更新
|
146次组卷
|
2卷引用:陕西省西安市鄠邑区2023-2024学年高三上学期期末考试理科综合试题-高中化学
名校
解题方法
5 . 某蓝色液中含下列离子中的若干种:Cu2+、Na+、Ba2+、Cl-、 、
、 ,各种离子的数目相等。取适量该溶液加入硝酸银溶液,有白色沉淀生成,滴加硝酸后仍存有沉淀。根据上述实验,以下推测不正确的是(已知:硫酸银会溶于硝酸)
,各种离子的数目相等。取适量该溶液加入硝酸银溶液,有白色沉淀生成,滴加硝酸后仍存有沉淀。根据上述实验,以下推测不正确的是(已知:硫酸银会溶于硝酸)
 、
、 ,各种离子的数目相等。取适量该溶液加入硝酸银溶液,有白色沉淀生成,滴加硝酸后仍存有沉淀。根据上述实验,以下推测不正确的是(已知:硫酸银会溶于硝酸)
,各种离子的数目相等。取适量该溶液加入硝酸银溶液,有白色沉淀生成,滴加硝酸后仍存有沉淀。根据上述实验,以下推测不正确的是(已知:硫酸银会溶于硝酸)| A.溶液中可能有Na+ | B.溶液中可能有Ba2+ |
C.溶液中可能有 | D.溶液中可能有 |
您最近一年使用:0次
解题方法
6 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
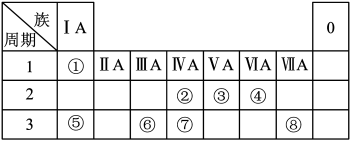
(1)地壳中含量居于第二位的元素在周期表中的位置是___________ 。
(2)②的最高价氧化物的分子式为___________ ;⑦的最高价氧化物对应水化物的分子式为___________ 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:___________ 、___________ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
(5)半径大小比较:③___________ ④;金属性强弱比较:⑤___________ ⑥(填“>”、“<”或“=”)。
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为___________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②的最高价氧化物的分子式为
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
| A.最高正化合价为+6 | B.气态氢化物比 稳定 稳定 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
(5)半径大小比较:③
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
名校
解题方法
7 . 化合物(YW4)2X2Z4·W2Z为无色柱状晶体,受热易分解,已知W、X、Y、Z的原子序数依次增大,其和为22,X、Y、Z为同一周期相邻元素。可利用下图装置检验该化合物分解出的相同元素组成的不同产物。
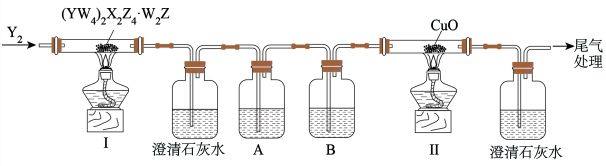
| A.(YW4)2X2Z4的物质类别为正盐 |
| B.装置B中盛装的试剂是氢氧化钠溶液 |
| C.反应开始前通入Y2,可以避免装置中的空气干扰产物的检验 |
| D.装置中两处澄清石灰水都变浑浊,证明分解产物中含有两种由X、Z组成的物质 |
您最近一年使用:0次
2024-02-19更新
|
288次组卷
|
2卷引用:陕西省西安交通大学附属中学2023-2024学年高一上学期期末考试化学试卷
名校
解题方法
8 . 卤素在高分子材料及电子电气等领域都有广泛应用。
(1)卤族元素位于元素周期表的___________ 区,基态溴原子的价层电子排布式为___________ 。
(2)比较键角大小:NH3___________ NF3(填“>”“<”或“=”)。
(3)已知下列5种羧酸:①CF3COOH②CH3COOH③CH2FCOOH④CH2ClCOOH⑤CH3CH2COOH,其酸性由强到弱的顺序为①___________ (填序号)。
(4)已知:由于 中甲基的推电子诱导效应,π电子离1号碳更近,H+倾向于与电子密度更高的1号碳结合,丙烯与HCl加成的主产物为CH3CHClCH3.,CF3CH=CH2与HCl加成反应主产物的结构简式为
中甲基的推电子诱导效应,π电子离1号碳更近,H+倾向于与电子密度更高的1号碳结合,丙烯与HCl加成的主产物为CH3CHClCH3.,CF3CH=CH2与HCl加成反应主产物的结构简式为___________ 。
(5)图1为气态氯化铍,图2为固态氯化铍。
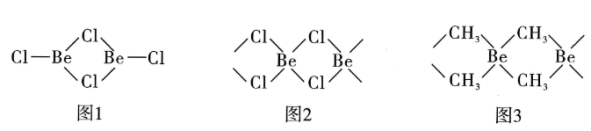
①气态氯化铍为___________ (填“极性”或“非极性”)分子。氯化铍由气态转化为固态,Be的杂化方式由___________ 转化为___________ 。
②若将固态氯化铍中的Cl原子替换为甲基,可形成如图3化合物。1个甲基与2个Be原子形成共价键时所提供的电子数为___________ 。
(1)卤族元素位于元素周期表的
(2)比较键角大小:NH3
(3)已知下列5种羧酸:①CF3COOH②CH3COOH③CH2FCOOH④CH2ClCOOH⑤CH3CH2COOH,其酸性由强到弱的顺序为①
(4)已知:由于
 中甲基的推电子诱导效应,π电子离1号碳更近,H+倾向于与电子密度更高的1号碳结合,丙烯与HCl加成的主产物为CH3CHClCH3.,CF3CH=CH2与HCl加成反应主产物的结构简式为
中甲基的推电子诱导效应,π电子离1号碳更近,H+倾向于与电子密度更高的1号碳结合,丙烯与HCl加成的主产物为CH3CHClCH3.,CF3CH=CH2与HCl加成反应主产物的结构简式为(5)图1为气态氯化铍,图2为固态氯化铍。

①气态氯化铍为
②若将固态氯化铍中的Cl原子替换为甲基,可形成如图3化合物。1个甲基与2个Be原子形成共价键时所提供的电子数为
您最近一年使用:0次
9 . 锰酸锂离子蓄电池是第二代锂离子动力电池。一种以软锰矿浆(主要成分为 ,含少量
,含少量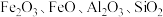 等杂质)为原料制备锰酸锂的流程如图所示。
等杂质)为原料制备锰酸锂的流程如图所示。
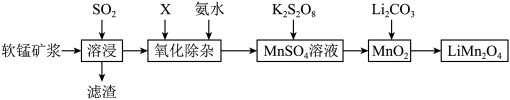
(1)溶浸生产中为提高 吸收率可采取的措施有___________(填序号)。
吸收率可采取的措施有___________(填序号)。
(2)X可选择的最佳试剂是___________ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
(3)由硫酸锰与 (过硫酸钾,结构为
(过硫酸钾,结构为 )溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。
)溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。 中
中 原子的化合价为
原子的化合价为___________ ,S原子的杂化方式为___________ 。
(4)将 和
和 按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品
按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品 并生两种气体。该反应的化学方程式为
并生两种气体。该反应的化学方程式为___________ 。
(5)锰酸锂可充电电池的总反应为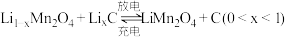
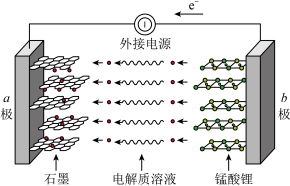
①放电时,电池正极的电极反应式为___________ 。
②充电时, 向
向___________ 极移动(填“a”或“b”)。
 ,含少量
,含少量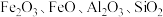 等杂质)为原料制备锰酸锂的流程如图所示。
等杂质)为原料制备锰酸锂的流程如图所示。
(1)溶浸生产中为提高
 吸收率可采取的措施有___________(填序号)。
吸收率可采取的措施有___________(填序号)。A.不断搅拌,使 和软锰矿浆充分接触 和软锰矿浆充分接触 | B.减小通入 的流速 的流速 |
| C.减少软锰矿浆的进入量 | D.增大通入 的流速 的流速 |
(2)X可选择的最佳试剂是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液(3)由硫酸锰与
 (过硫酸钾,结构为
(过硫酸钾,结构为 )溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。
)溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。 中
中 原子的化合价为
原子的化合价为(4)将
 和
和 按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品
按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品 并生两种气体。该反应的化学方程式为
并生两种气体。该反应的化学方程式为(5)锰酸锂可充电电池的总反应为
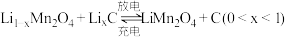

①放电时,电池正极的电极反应式为
②充电时,
 向
向
您最近一年使用:0次
解题方法
10 . PbO主要用作颜料,冶金助熔剂、油漆催干剂,橡胶硫化促进剂、杀虫剂等。一种以方铅矿(含PbS及少量Fe2O3、MgO、SiO2等)为原料制备PbO的工艺流程如图:
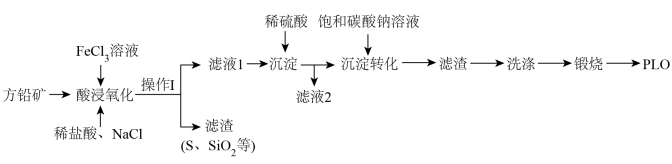
回答下列问题:
(1)Pb的价电子轨道表示式为__________ ,Pb在元素周期表中属于______ 区元素。
(2)“酸浸氧化”过程中FeCl3与PbS发生反应生成[PbCl4]2-,反应的离子方程式为_____________ 。
(3)验证滤液1中存在Fe2+,可取样后滴加少量________ (填化学式)溶液,观察到有蓝色沉淀析出。
(4)已知:Ksp(PbCO3)=7.4×10-14、Ksp(PbSO4)=1.6×10-8。要实现PbSO4将化明PbCO3, 的最小值为
的最小值为___________ (保留两位有效数字)。“洗涤”时,检验PbCO3固体是否洗涤干净的操作是________ 。
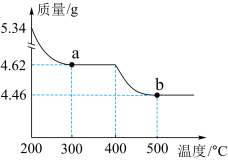
(5)已知焙烧PbCO3可制得铅的氧化物,为了研究其产物成分,取5.34gPbCO3进行焙烧,其热重曲线如图所示,请写出350℃时所得铅的氧化物的化学式:_________ 。

回答下列问题:
(1)Pb的价电子轨道表示式为
(2)“酸浸氧化”过程中FeCl3与PbS发生反应生成[PbCl4]2-,反应的离子方程式为
(3)验证滤液1中存在Fe2+,可取样后滴加少量
(4)已知:Ksp(PbCO3)=7.4×10-14、Ksp(PbSO4)=1.6×10-8。要实现PbSO4将化明PbCO3,
 的最小值为
的最小值为(5)已知焙烧PbCO3可制得铅的氧化物,为了研究其产物成分,取5.34gPbCO3进行焙烧,其热重曲线如图所示,请写出350℃时所得铅的氧化物的化学式:

您最近一年使用:0次



