名校
解题方法
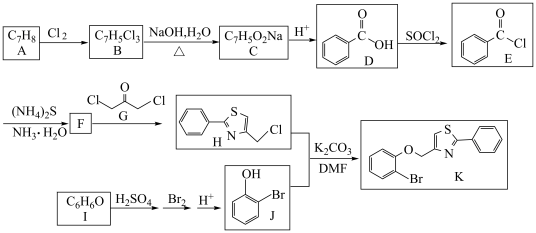
1 . 有机物K是重要的药物中间体,一种K的合成路线如下:
(1)A→B的反应条件是___________ 。D→E的反应类型为___________ 。
(2)F的结构简式为___________ 。
(3)I的化学名称是___________ 。J中官能团的名称是___________ 。
(4)反应B→C的化学方程式为___________ 。
(5)鉴别D的水溶液与I的水溶液的化学试剂为___________ 。
(6)L是D与乙醇酯化后的产物,同时满足下列条件的L的同分异构体有___________ 种;
①含有苯环;
②能发生水解反应且1molL需要2molNaOH发生反应。
其中,核磁共振氢谱有4组峰,且峰面积比为6:2:1:1的物质的结构简式为___________ (任写一种)。
已知:①
②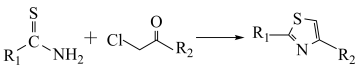
(1)A→B的反应条件是
(2)F的结构简式为
(3)I的化学名称是
(4)反应B→C的化学方程式为
(5)鉴别D的水溶液与I的水溶液的化学试剂为
(6)L是D与乙醇酯化后的产物,同时满足下列条件的L的同分异构体有
①含有苯环;
②能发生水解反应且1molL需要2molNaOH发生反应。
其中,核磁共振氢谱有4组峰,且峰面积比为6:2:1:1的物质的结构简式为
您最近一年使用:0次
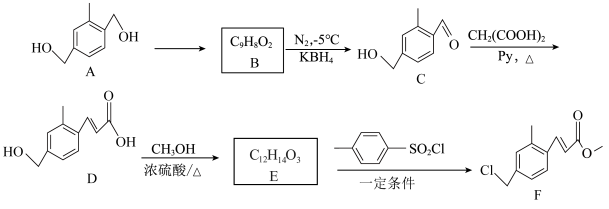
2 . F是合成某药物的中间体,一种制备F的合成路线如图所示。
(1)A→B的试剂和条件为___________ ,其反应类型是___________ 。
(2) 的名称为
的名称为___________ 。
(3)D中含氧官能团的名称为___________ 。
(4)D→E的化学方程式为___________ 。
(5)D→E和E→F的顺序___________ (填“能”或“不能”)颠倒,原因是___________ 。
(6)G是D的芳香族同分异构体,同时具备下列条件的G的结构有___________ 种(不考虑立体异构)。
①能发生银镜反应
②能与碳酸氢钠溶液反应生成 气体
气体
③只有2个取代基与苯环直接相连,且分子结构中有2个甲基
其中核磁共振氢谱有五组峰,且峰面积之比为 的结构简式为
的结构简式为___________ 。
已知:
(1)A→B的试剂和条件为
(2)
 的名称为
的名称为(3)D中含氧官能团的名称为
(4)D→E的化学方程式为
(5)D→E和E→F的顺序
(6)G是D的芳香族同分异构体,同时具备下列条件的G的结构有
①能发生银镜反应
②能与碳酸氢钠溶液反应生成
 气体
气体③只有2个取代基与苯环直接相连,且分子结构中有2个甲基
其中核磁共振氢谱有五组峰,且峰面积之比为
 的结构简式为
的结构简式为
您最近一年使用:0次
解题方法
3 . 烯烃的加氢甲酰化反应是醛合成中重要的均相催化工业反应之一。我国科学家利用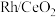 催化剂实现烯烃甲酰化。回答下列问题:
催化剂实现烯烃甲酰化。回答下列问题: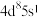 ,位于周期表第五周期第
,位于周期表第五周期第_____ 族,位于_____ 区。
(2)基态O原子核外电子有_____ 种不同的空间运动状态。
(3)乙中C原子的杂化类型是_____ 。
(4)丙分子中所含元素电负性由大到小顺序为_____ 。丙分子有_____ 个手性碳原子。
(5)已知: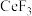 、
、 的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是
的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是_____ 。
(6) 的立方晶胞结构如图所示。已知
的立方晶胞结构如图所示。已知 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为 。
。_____ 。该晶体密度为_____  。
。
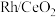 催化剂实现烯烃甲酰化。回答下列问题:
催化剂实现烯烃甲酰化。回答下列问题: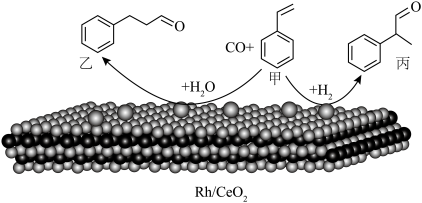
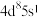 ,位于周期表第五周期第
,位于周期表第五周期第(2)基态O原子核外电子有
(3)乙中C原子的杂化类型是
(4)丙分子中所含元素电负性由大到小顺序为
(5)已知:
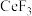 、
、 的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是
的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是(6)
 的立方晶胞结构如图所示。已知
的立方晶胞结构如图所示。已知 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为 。
。
 。
。
您最近一年使用:0次
4 . 铬酸铅[常温下,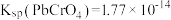 ]又称铬黄,常用于染料或颜料,某同学在实验室以
]又称铬黄,常用于染料或颜料,某同学在实验室以 为原料制备
为原料制备 ,实验步骤如下:
,实验步骤如下:
步骤1:称取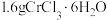 于
于 的烧杯中,加入
的烧杯中,加入 蒸馏水,搅拌使其溶解,逐滴滴入稍微过量的
蒸馏水,搅拌使其溶解,逐滴滴入稍微过量的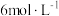 的
的 溶液;
溶液;
步骤2:向上述溶液中逐滴滴入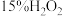 溶液,溶液由绿色变为黄色。加热煮沸
溶液,溶液由绿色变为黄色。加热煮沸 ,将多余的
,将多余的 赶尽,此时溶液变为亮黄色。再逐滴滴入
赶尽,此时溶液变为亮黄色。再逐滴滴入 的硝酸溶液,亮黄色溶液又变为橙红色,此时溶液的
的硝酸溶液,亮黄色溶液又变为橙红色,此时溶液的 为4.6;
为4.6;
步骤3:在煮沸条件下逐滴滴入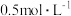 的
的 溶液,加入第一滴后先搅拌
溶液,加入第一滴后先搅拌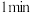 再加第2滴,每滴加一滴可以看到有黄色沉淀产生,滴加到不再有新的黄色沉淀产生时停止加入
再加第2滴,每滴加一滴可以看到有黄色沉淀产生,滴加到不再有新的黄色沉淀产生时停止加入 溶液。继续煮沸
溶液。继续煮沸 ,取下静置片刻,检验是否沉淀完全,过滤,产品用蒸馏水洗涤2~3次;
,取下静置片刻,检验是否沉淀完全,过滤,产品用蒸馏水洗涤2~3次;
步骤4:将沉淀放入烘箱中干燥、称重、计算产率。
已知:元素铬( )在溶液中主要以
)在溶液中主要以 (蓝紫色)、
(蓝紫色)、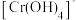 (绿色)、
(绿色)、 (橙红色)、
(橙红色)、 (黄色)等形式存在,
(黄色)等形式存在, 为难溶于水的灰蓝色固体。回答下列问题:
为难溶于水的灰蓝色固体。回答下列问题:
(1)实验室在配制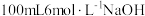 溶液时,下列仪器一定不需要的是___________(填字母)。
溶液时,下列仪器一定不需要的是___________(填字母)。
(2)步骤1中加入稍微过量的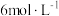 的
的 溶液过程中的现象是
溶液过程中的现象是___________ , 溶液不能过量太多,其原因是
溶液不能过量太多,其原因是___________ 。
(3)步骤2溶液中逐滴滴入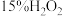 溶液,溶液由绿色变为黄色。发生反应的离子方程式为
溶液,溶液由绿色变为黄色。发生反应的离子方程式为___________ 。
(4)步骤2用硝酸调节 ,存在如下平衡:
,存在如下平衡: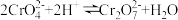 。已知
。已知 随
随 的变化如图所示。
的变化如图所示。 的平衡转化率
的平衡转化率___________ (填“增大”“减小”或“不变”)。
②升高温度,溶液中 的平衡转化率减小,则该反应的
的平衡转化率减小,则该反应的
___________ (填“>”或“<”)0。
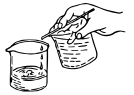
(5)步骤3采用倾析法过滤,如图所示。下列关于该过滤方法的说法不正确的是___________(填字母)。
(6)对于步骤3,甲同学提出可用 代替
代替 作为原料,乙同学认为
作为原料,乙同学认为 难溶于水
难溶于水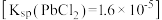 ,故设想不可能。甲同学进行实验,发现可以得到产品,但产量很低,其原因是
,故设想不可能。甲同学进行实验,发现可以得到产品,但产量很低,其原因是___________ 。
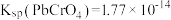 ]又称铬黄,常用于染料或颜料,某同学在实验室以
]又称铬黄,常用于染料或颜料,某同学在实验室以 为原料制备
为原料制备 ,实验步骤如下:
,实验步骤如下:步骤1:称取
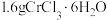 于
于 的烧杯中,加入
的烧杯中,加入 蒸馏水,搅拌使其溶解,逐滴滴入稍微过量的
蒸馏水,搅拌使其溶解,逐滴滴入稍微过量的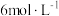 的
的 溶液;
溶液;步骤2:向上述溶液中逐滴滴入
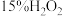 溶液,溶液由绿色变为黄色。加热煮沸
溶液,溶液由绿色变为黄色。加热煮沸 ,将多余的
,将多余的 赶尽,此时溶液变为亮黄色。再逐滴滴入
赶尽,此时溶液变为亮黄色。再逐滴滴入 的硝酸溶液,亮黄色溶液又变为橙红色,此时溶液的
的硝酸溶液,亮黄色溶液又变为橙红色,此时溶液的 为4.6;
为4.6;步骤3:在煮沸条件下逐滴滴入
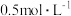 的
的 溶液,加入第一滴后先搅拌
溶液,加入第一滴后先搅拌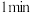 再加第2滴,每滴加一滴可以看到有黄色沉淀产生,滴加到不再有新的黄色沉淀产生时停止加入
再加第2滴,每滴加一滴可以看到有黄色沉淀产生,滴加到不再有新的黄色沉淀产生时停止加入 溶液。继续煮沸
溶液。继续煮沸 ,取下静置片刻,检验是否沉淀完全,过滤,产品用蒸馏水洗涤2~3次;
,取下静置片刻,检验是否沉淀完全,过滤,产品用蒸馏水洗涤2~3次;步骤4:将沉淀放入烘箱中干燥、称重、计算产率。
已知:元素铬(
 )在溶液中主要以
)在溶液中主要以 (蓝紫色)、
(蓝紫色)、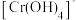 (绿色)、
(绿色)、 (橙红色)、
(橙红色)、 (黄色)等形式存在,
(黄色)等形式存在, 为难溶于水的灰蓝色固体。回答下列问题:
为难溶于水的灰蓝色固体。回答下列问题:(1)实验室在配制
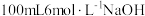 溶液时,下列仪器一定不需要的是___________(填字母)。
溶液时,下列仪器一定不需要的是___________(填字母)。A. | B. | C. | D. |
(2)步骤1中加入稍微过量的
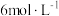 的
的 溶液过程中的现象是
溶液过程中的现象是 溶液不能过量太多,其原因是
溶液不能过量太多,其原因是(3)步骤2溶液中逐滴滴入
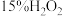 溶液,溶液由绿色变为黄色。发生反应的离子方程式为
溶液,溶液由绿色变为黄色。发生反应的离子方程式为(4)步骤2用硝酸调节
 ,存在如下平衡:
,存在如下平衡: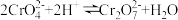 。已知
。已知 随
随 的变化如图所示。
的变化如图所示。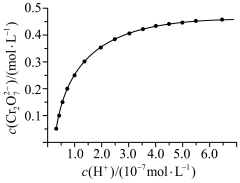
 的平衡转化率
的平衡转化率②升高温度,溶液中
 的平衡转化率减小,则该反应的
的平衡转化率减小,则该反应的
(5)步骤3采用倾析法过滤,如图所示。下列关于该过滤方法的说法不正确的是___________(填字母)。
| A.该方法适用于过滤胶状沉淀或颗粒较小的沉淀 |
| B.使用该方法过滤后,若沉淀物要洗涤,可注入水(或其他洗涤液),充分搅拌后使沉淀沉降,再进行过滤 |
| C.这种过滤方法可以避免沉淀堵塞滤纸小孔而影响过滤速度 |
| D.该操作中玻璃棒的作用为引流 |
(6)对于步骤3,甲同学提出可用
 代替
代替 作为原料,乙同学认为
作为原料,乙同学认为 难溶于水
难溶于水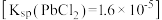 ,故设想不可能。甲同学进行实验,发现可以得到产品,但产量很低,其原因是
,故设想不可能。甲同学进行实验,发现可以得到产品,但产量很低,其原因是
您最近一年使用:0次
5 . 铁及其化合物在化工生产中发挥着重要作用。回答下列问题:
(1)一定温度下,在某密闭无氧环境中热分解 ,反应的热化学方程式为
,反应的热化学方程式为 。反应生成的混合气体中
。反应生成的混合气体中 的物质的量分数为
的物质的量分数为___________ 。反应达平衡后,缩小容器体积,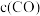
___________ (填“增大”“减小”或“不变”)。
(2)将 置入抽空的刚性容器中,升高温度,发生分解反应:
置入抽空的刚性容器中,升高温度,发生分解反应: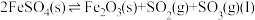 。平衡时
。平衡时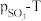 的关系如图所示。
的关系如图所示。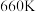 时,该反应的平衡总压
时,该反应的平衡总压
___________  ,压强平衡常数
,压强平衡常数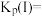
___________ 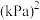 (压强平衡常数是用分压代表平衡浓度,分压=总压×物质的量分数)。
(压强平衡常数是用分压代表平衡浓度,分压=总压×物质的量分数)。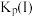 随反应温度升高而
随反应温度升高而___________ (填“增大”“减小”或“不变”)。 可用作脱除
可用作脱除 气体的脱硫剂。
气体的脱硫剂。 首先与表面的
首先与表面的 产生疏松多孔的产物
产生疏松多孔的产物 ,随着反应的进行,Fe2O3不断减少,产物层不断加厚,如图所示。失效的脱硫剂可在氧气中加热重新转化为Fe2O3实现“再生”。
,随着反应的进行,Fe2O3不断减少,产物层不断加厚,如图所示。失效的脱硫剂可在氧气中加热重新转化为Fe2O3实现“再生”。 “再生”时转化为Fe2O3的化学方程式:
“再生”时转化为Fe2O3的化学方程式:___________ 。
②“再生”时若 浓度过大、反应温度过高,“再生”后的脱硫剂脱硫效果明显变差的原因可能是
浓度过大、反应温度过高,“再生”后的脱硫剂脱硫效果明显变差的原因可能是___________ 。
(1)一定温度下,在某密闭无氧环境中热分解
 ,反应的热化学方程式为
,反应的热化学方程式为 。反应生成的混合气体中
。反应生成的混合气体中 的物质的量分数为
的物质的量分数为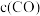
(2)将
 置入抽空的刚性容器中,升高温度,发生分解反应:
置入抽空的刚性容器中,升高温度,发生分解反应: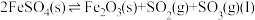 。平衡时
。平衡时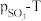 的关系如图所示。
的关系如图所示。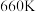 时,该反应的平衡总压
时,该反应的平衡总压
 ,压强平衡常数
,压强平衡常数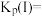
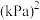 (压强平衡常数是用分压代表平衡浓度,分压=总压×物质的量分数)。
(压强平衡常数是用分压代表平衡浓度,分压=总压×物质的量分数)。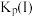 随反应温度升高而
随反应温度升高而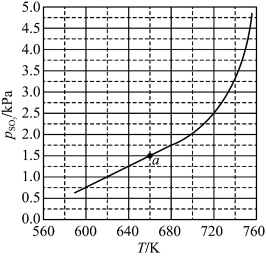
 可用作脱除
可用作脱除 气体的脱硫剂。
气体的脱硫剂。 首先与表面的
首先与表面的 产生疏松多孔的产物
产生疏松多孔的产物 ,随着反应的进行,Fe2O3不断减少,产物层不断加厚,如图所示。失效的脱硫剂可在氧气中加热重新转化为Fe2O3实现“再生”。
,随着反应的进行,Fe2O3不断减少,产物层不断加厚,如图所示。失效的脱硫剂可在氧气中加热重新转化为Fe2O3实现“再生”。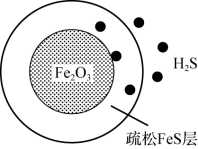
 “再生”时转化为Fe2O3的化学方程式:
“再生”时转化为Fe2O3的化学方程式:②“再生”时若
 浓度过大、反应温度过高,“再生”后的脱硫剂脱硫效果明显变差的原因可能是
浓度过大、反应温度过高,“再生”后的脱硫剂脱硫效果明显变差的原因可能是
您最近一年使用:0次
6 . 钴基变形高温合金是指含钴40%~70%的铸造合金,具有较好的抗氧化和抗热腐蚀性。制备某钴基变形高温合金的废料中主要含有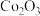 ,还含有少量
,还含有少量 、
、 及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收
及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收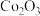 的工业流程如图所示。
的工业流程如图所示。 、
、 、
、 、
、 、
、 、
、 等。
等。
②部分阳离子以氢氧化物形式开始沉淀和沉淀完全(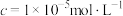 )时的pH见下表。
)时的pH见下表。
(1)“溶浸”前,通常需要将合金废料粉碎,这样做的目的是___________ 。“溶浸”时加入 的作用是
的作用是___________ 。
(2)“滤液1”中加入 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。得到“滤渣2”时需要加 溶液调节溶液的
溶液调节溶液的 范围是
范围是___________ 。
(3)已知:25℃时, 、
、 。向“滤液2”中加入
。向“滤液2”中加入 溶液的目的是将溶液中的
溶液的目的是将溶液中的 与
与 转化为氮化物沉淀。如果“滤液2”中的
转化为氮化物沉淀。如果“滤液2”中的 ,则开始滴加
,则开始滴加 溶液时,首先析出的沉淀是
溶液时,首先析出的沉淀是___________ (填化学式),已知当加入过量 溶液后,所得滤液中
溶液后,所得滤液中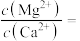
___________ 。
(4) 在空气中充分煅烧,除得到产品外,还生成了
在空气中充分煅烧,除得到产品外,还生成了 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
(5)若将草酸铵溶液换为碳酸氢钠溶液,可将 转化为
转化为 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为___________ 。
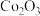 ,还含有少量
,还含有少量 、
、 及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收
及铝、镁、钙等金属元素的氧化物。用该废料采用酸溶法回收 的工业流程如图所示。
的工业流程如图所示。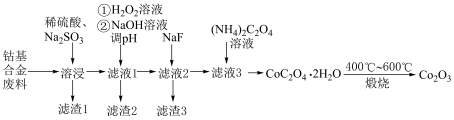
 、
、 、
、 、
、 、
、 、
、 等。
等。②部分阳离子以氢氧化物形式开始沉淀和沉淀完全(
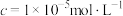 )时的pH见下表。
)时的pH见下表。| 沉淀物 |  |  |  |  |  |
| 开始沉淀时的pH | 6.6 | 7.6 | 2.7 | 3.4 | 9.2 |
| 沉淀完全时的pH | 9.2 | 9.6 | 3.2 | 4.7 | 11.1 |
(1)“溶浸”前,通常需要将合金废料粉碎,这样做的目的是
 的作用是
的作用是(2)“滤液1”中加入
 溶液的作用是
溶液的作用是 溶液调节溶液的
溶液调节溶液的 范围是
范围是(3)已知:25℃时,
 、
、 。向“滤液2”中加入
。向“滤液2”中加入 溶液的目的是将溶液中的
溶液的目的是将溶液中的 与
与 转化为氮化物沉淀。如果“滤液2”中的
转化为氮化物沉淀。如果“滤液2”中的 ,则开始滴加
,则开始滴加 溶液时,首先析出的沉淀是
溶液时,首先析出的沉淀是 溶液后,所得滤液中
溶液后,所得滤液中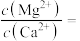
(4)
 在空气中充分煅烧,除得到产品外,还生成了
在空气中充分煅烧,除得到产品外,还生成了 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(5)若将草酸铵溶液换为碳酸氢钠溶液,可将
 转化为
转化为 沉淀,反应的离子方程式为
沉淀,反应的离子方程式为
您最近一年使用:0次
7 . 甲苯是重要的化工原料,可合成许多重要的化工产品,其中用于合成M与高分子化合物E的流程如下图所示。
(1)M的名称为___________ ,甲苯→A的反应类型为___________ 。
(2)D中官能团的名称为___________ ,B的结构简式为___________ 。
(3)甲苯→G有两种途径:①先与 加成后在
加成后在 、光照条件下取代;②
、光照条件下取代;②___________ (答出反应类型与相应试剂),两种方案中所得产物纯度较高的是___________ ;G→M的反应条件为___________ 。
(4)C→D的化学方程式为___________ 。
(5)A有许多芳香族同分异构体,其中符合下列条件的同分异构体共有___________ 种,写出核磁共振氢谱有5组峰的物质的结构简式:___________ 。
①遇 溶液能发生显色反应;
溶液能发生显色反应;
②分子中只有一个环状结构。

(1)M的名称为
(2)D中官能团的名称为
(3)甲苯→G有两种途径:①先与
 加成后在
加成后在 、光照条件下取代;②
、光照条件下取代;②(4)C→D的化学方程式为
(5)A有许多芳香族同分异构体,其中符合下列条件的同分异构体共有
①遇
 溶液能发生显色反应;
溶液能发生显色反应;②分子中只有一个环状结构。
您最近一年使用:0次
8 . 常温下,向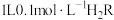 溶液中滴加
溶液中滴加 溶液,混合溶液中
溶液,混合溶液中 [X表示
[X表示 或
或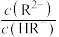 随溶液
随溶液 的变化如图所示[可能用到的数据:
的变化如图所示[可能用到的数据: ,
,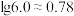 ]。下列说法错误的是
]。下列说法错误的是
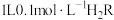 溶液中滴加
溶液中滴加 溶液,混合溶液中
溶液,混合溶液中 [X表示
[X表示 或
或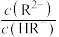 随溶液
随溶液 的变化如图所示[可能用到的数据:
的变化如图所示[可能用到的数据: ,
,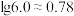 ]。下列说法错误的是
]。下列说法错误的是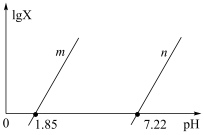
A.曲线 代表 代表 与溶液 与溶液 的关系 的关系 |
B.常温下, 的 的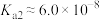 |
C.常温下, 溶液中: 溶液中: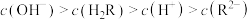 |
D.从开始滴加至 溶液过量的过程中,水的电离程度是先增大后减小 溶液过量的过程中,水的电离程度是先增大后减小 |
您最近一年使用:0次
解题方法
9 .  常用作有机合成中的还原剂,其合成反应为
常用作有机合成中的还原剂,其合成反应为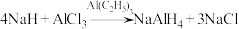 。回答下列问题:
。回答下列问题:
(1)基态氧原子中价层电子排布图为___________ ,O、H、Al电负性由大到小的顺序为___________ ,钠的焰色是黄色,产生此焰色时属于___________ (填“发射”或“吸收”)光谱。
(2)已知 熔点为194℃、NaCl熔点为801℃,其原因是
熔点为194℃、NaCl熔点为801℃,其原因是___________ ,又知铝的第一电离能比镁的第一电离能小,原因是___________ 。
(3)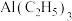 中碳原子的杂化方式为
中碳原子的杂化方式为___________ , 的空间构型为
的空间构型为___________ , 中不存在的化学键是
中不存在的化学键是___________ (填字母)。
A.σ键 B.配位键 C.离子键 D.非极性键
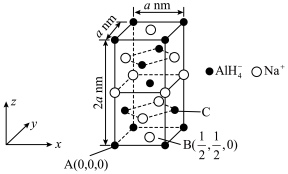
(4) 晶体密度为
晶体密度为 ,其晶胞图及部分微粒分数坐标如图所示,则C的分数坐标为
,其晶胞图及部分微粒分数坐标如图所示,则C的分数坐标为___________ ,阿伏加德罗常数
___________  。
。
 常用作有机合成中的还原剂,其合成反应为
常用作有机合成中的还原剂,其合成反应为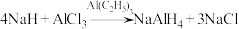 。回答下列问题:
。回答下列问题:(1)基态氧原子中价层电子排布图为
(2)已知
 熔点为194℃、NaCl熔点为801℃,其原因是
熔点为194℃、NaCl熔点为801℃,其原因是(3)
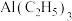 中碳原子的杂化方式为
中碳原子的杂化方式为 的空间构型为
的空间构型为 中不存在的化学键是
中不存在的化学键是A.σ键 B.配位键 C.离子键 D.非极性键
(4)
 晶体密度为
晶体密度为 ,其晶胞图及部分微粒分数坐标如图所示,则C的分数坐标为
,其晶胞图及部分微粒分数坐标如图所示,则C的分数坐标为
 。
。
您最近一年使用:0次
解题方法
10 . 利用下图所示的电化学装置可消除污水中的氮污染,下列叙述正确的是

| A.电极电势:A>B |
B.负极上电极反应式: |
C.好氧反应器中反应式为 |
D.X离子为 ,交换膜Y是阴离子交换膜 ,交换膜Y是阴离子交换膜 |
您最近一年使用:0次



