解题方法
1 . 为探究铜的化合物有关性质,现进行如下实验。
回答下列问题:
(1)由 配制实验I中的
配制实验I中的 溶液,下列仪器中不需要的是
溶液,下列仪器中不需要的是_______ (填仪器名称),定容后还需要进行的操作为_______ 。_______ 。
(3)实验Ⅱ未观察到蓝色絮状沉淀,猜想原因是实验Ⅱ取用的 溶液浓度太低。查阅资料得:
溶液浓度太低。查阅资料得: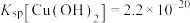 ,通过计算否定该猜想
,通过计算否定该猜想_______ 。
(4)实验Ⅲ生成蓝色絮状沉淀的离子方程式为_______ 。
(5)查阅资料:烯醛类物质易形成亮黄色树脂状化合物,微溶于水。实验Ⅳ中产生烯醛类物质的结构简式为_______ 。
(6)实验Ⅴ的现象为_______ 。
序号 | 实验操作 | 实验现象 |
Ⅰ | 将绿豆大的钠放入装有100mL 0.2  溶液的烧杯中 溶液的烧杯中 | |固体溶解,有气泡冒出,有蓝色絮状沉淀 |
Ⅱ | 取实验I等量的钠放入装有100mL 0.002  溶液的烧杯中 溶液的烧杯中 | 固体溶解,有气泡冒出,无蓝色絮状沉淀,测得溶液pH=9 |
Ⅲ | 取实验Ⅱ反应后的溶液于试管中,逐滴加入0.1 HCl溶液 HCl溶液 | 先出现蓝色絮状沉淀,后沉淀溶解 |
Ⅳ | 取实验Ⅰ反应后的溶液于试管中,振荡,加入0.5mL乙醛溶液,加热 | 试管底部出现砖红色沉淀,上层悬浊液呈现亮黄色 |
Ⅴ | 取实验I反应后的溶液于试管中,振荡,加入0.5mL甲醛溶液,加热 |
(1)由
 配制实验I中的
配制实验I中的 溶液,下列仪器中不需要的是
溶液,下列仪器中不需要的是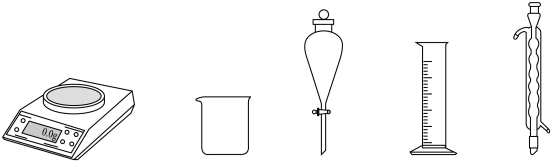
(3)实验Ⅱ未观察到蓝色絮状沉淀,猜想原因是实验Ⅱ取用的
 溶液浓度太低。查阅资料得:
溶液浓度太低。查阅资料得: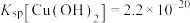 ,通过计算否定该猜想
,通过计算否定该猜想(4)实验Ⅲ生成蓝色絮状沉淀的离子方程式为
(5)查阅资料:烯醛类物质易形成亮黄色树脂状化合物,微溶于水。实验Ⅳ中产生烯醛类物质的结构简式为
(6)实验Ⅴ的现象为
您最近一年使用:0次
7日内更新
|
429次组卷
|
4卷引用:2025届广东省广州市高三上学期8月第一次调研考试化学试卷
2 . 在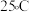 时,向三羟甲基甲胺(简写为
时,向三羟甲基甲胺(简写为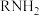 )与其盐酸盐
)与其盐酸盐 组成的
组成的 混合溶液中,分别逐滴滴入
混合溶液中,分别逐滴滴入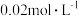 盐酸和
盐酸和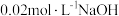 溶液,测得
溶液,测得 与滴入溶液体积的关系如图所示。已知:起始时,
与滴入溶液体积的关系如图所示。已知:起始时, ,图中Ⅰ、Ⅱ、Ⅲ分别表示起始时,
,图中Ⅰ、Ⅱ、Ⅲ分别表示起始时,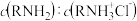 为
为 、
、 、
、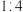 的曲线。
的曲线。
下列说法正确的是
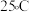 时,向三羟甲基甲胺(简写为
时,向三羟甲基甲胺(简写为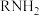 )与其盐酸盐
)与其盐酸盐 组成的
组成的 混合溶液中,分别逐滴滴入
混合溶液中,分别逐滴滴入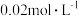 盐酸和
盐酸和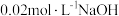 溶液,测得
溶液,测得 与滴入溶液体积的关系如图所示。已知:起始时,
与滴入溶液体积的关系如图所示。已知:起始时, ,图中Ⅰ、Ⅱ、Ⅲ分别表示起始时,
,图中Ⅰ、Ⅱ、Ⅲ分别表示起始时,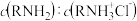 为
为 、
、 、
、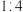 的曲线。
的曲线。下列说法正确的是
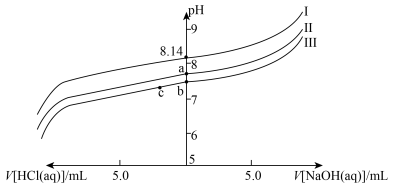
A. 数量级为 数量级为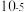 |
B.溶液中水的电离程度: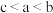 |
C.当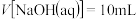 时,混合溶液都有 时,混合溶液都有 |
| D.三羟甲基甲胺与其盐酸盐可组成缓冲体系 |
您最近一年使用:0次
2024-09-18更新
|
424次组卷
|
5卷引用:2025届广东省广州市高三上学期8月第一次调研考试化学试卷
3 . 某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。
【 的制备】
的制备】
(1)用下图装置制备 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是_______ 。
(2)写出装置C中生成 的离子方程式:
的离子方程式:_______ 。 的性质探究】
的性质探究】
资料:ⅰ. 在强酸性条件下被还原成
在强酸性条件下被还原成 ,在近中性条件下被还原成
,在近中性条件下被还原成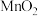 。
。
ⅱ.单质硫可溶于 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。
该小组研究 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。
(3)实验Ⅰ和Ⅱ的现象与资料均不相符,比如按资料ⅰ,应该生成黑色的 沉淀,请用离子方程式解释
沉淀,请用离子方程式解释 消失的原因:
消失的原因:_______ 。
(4)反思:反应物相同而现象不同,表明物质变化不仅与自身性质有关,还与_______ (填2条)等因素有关。
(5)该小组为了证明实验Ⅱ中 被氧化成
被氧化成 ,探究如下:
,探究如下:
①甲同学取Ⅱ中少量溶液进行实验,检测有 ,得出结论,乙同学否定了该结论,理由是
,得出结论,乙同学否定了该结论,理由是____ 。
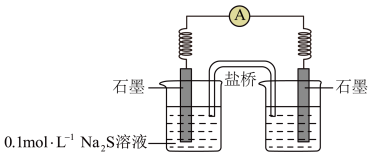
②该小组同学讨论后,设计了如图装置进行实验,_______ 。
b.连通后电流计指针偏转,一段时间后,_______ (填操作和现象),证实该条件下 可以将
可以将 氧化成
氧化成 。
。
 制备
制备 并对其性质进行探究。
并对其性质进行探究。【
 的制备】
的制备】(1)用下图装置制备
 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是(2)写出装置C中生成
 的离子方程式:
的离子方程式: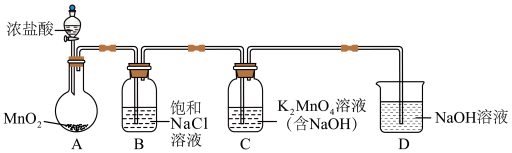
 的性质探究】
的性质探究】资料:ⅰ.
 在强酸性条件下被还原成
在强酸性条件下被还原成 ,在近中性条件下被还原成
,在近中性条件下被还原成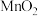 。
。ⅱ.单质硫可溶于
 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。该小组研究
 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。| 实验序号 | 实验过程 | 实验现象 |
| Ⅰ |
| 溶液呈淡黄色(pH≈8),生成浅粉色沉淀(MnS) |
| Ⅱ |
| 紫色变浅(pH<1),生成棕褐色沉淀( ) ) |
(3)实验Ⅰ和Ⅱ的现象与资料均不相符,比如按资料ⅰ,应该生成黑色的
 沉淀,请用离子方程式解释
沉淀,请用离子方程式解释 消失的原因:
消失的原因:(4)反思:反应物相同而现象不同,表明物质变化不仅与自身性质有关,还与
(5)该小组为了证明实验Ⅱ中
 被氧化成
被氧化成 ,探究如下:
,探究如下:①甲同学取Ⅱ中少量溶液进行实验,检测有
 ,得出结论,乙同学否定了该结论,理由是
,得出结论,乙同学否定了该结论,理由是②该小组同学讨论后,设计了如图装置进行实验,
b.连通后电流计指针偏转,一段时间后,
 可以将
可以将 氧化成
氧化成 。
。
您最近一年使用:0次
4 . 微格列汀是一种抗糖尿病药物,其结构简式如图所示。下列说法正确的是
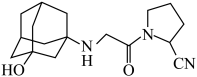
| A.有3种官能团 | B.有5个手性碳原子 |
| C.碳原子有2种杂化方式 | D.在碱性溶液中加热能稳定存在 |
您最近一年使用:0次
2024-09-13更新
|
658次组卷
|
5卷引用:2025届广东省广州市高三上学期8月第一次调研考试化学试卷
5 . 下图为某药物合成线路的一部分:_______ 。
(2)化合物Ⅴ中不含氧的官能团名称为_______ ;化合物Ⅱ的某种同分异构体含有苯环,在核磁共振氢谱图上只有3组峰,既能发生银镜反应,又能发生水解反应,其结构简式为_______ 。
(3)根据化合物Ⅱ的结构特征,分析预测其可能的化学性质,完成下表。
(4)已知反应②的原子利用率为100%,反应③为消去反应,则物质Ⅲ的结构简式为_____ 。反应④需要的另外一种有机反应物为____ 。
(5)下列说法正确的是_______(填标号)。
(6)以甲苯为主要原料,无机试剂任选,制备化合物Ⅰ,基于你设计的合成路线,回答下列问题(均要注明反应条件):
ⅰ.第一步反应的化学方程式为_______ 。
ⅱ.最后一步为把溶液酸化,则酸化之前反应的化学方程式为_______ 。
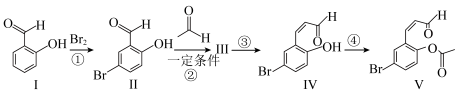
(2)化合物Ⅴ中不含氧的官能团名称为
(3)根据化合物Ⅱ的结构特征,分析预测其可能的化学性质,完成下表。
| 序号 | 反应试剂、条件 | 反应形成的新结构 | 反应类型 |
| a |  | ||
| b | 银镜反应 |
(4)已知反应②的原子利用率为100%,反应③为消去反应,则物质Ⅲ的结构简式为
(5)下列说法正确的是_______(填标号)。
| A.化合物Ⅰ可溶于水,是因为它可以和水分子形成氢键 |
B.反应②中有 键的断裂与形成 键的断裂与形成 |
C.化合物Ⅳ分别与足量的 和 和 反应,消耗 反应,消耗 和 和 的物质的量之比为5:1 的物质的量之比为5:1 |
| D.相同物质的量的化合物Ⅳ和Ⅴ在一定条件下分别与足量的热NaOH溶液反应,两者消耗NaOH的物质的量之比为3:4 |
(6)以甲苯为主要原料,无机试剂任选,制备化合物Ⅰ,基于你设计的合成路线,回答下列问题(均要注明反应条件):
ⅰ.第一步反应的化学方程式为
ⅱ.最后一步为把溶液酸化,则酸化之前反应的化学方程式为
您最近一年使用:0次
名校
6 . 其他条件相同时,不同pH条件下,用浓度传感器测得反应2A(aq)+B(aq)=3C(aq)+D(aq)中产物D的浓度随时间变化的关系如图。则下列有关叙述正确的是
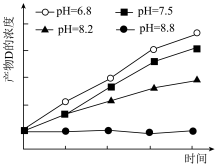
| A.pH=8.8时,升高温度,反应速率不变 |
| B.保持条件不变,c(H+)越低,c(D)越高 |
| C.为了实验取样,可以采用调节pH的方法迅速停止反应 |
| D.减小外界压强,反应速率一定减小 |
您最近一年使用:0次
2024-09-07更新
|
242次组卷
|
2卷引用:广东省东莞中学松山湖学校2025届高三上学期8月模拟考试化学试题
7 . 某离子液体结构如图所示。已知X、Y、Z、W是原子序数依次增大的短周期元素,其中Y和Z位于同一周期,W的最高价氧化物的水化物为强酸。下列说法正确的是
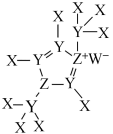
| A.第一电离能:Y>Z>X |
| B.阳离子中的五元环为平面结构 |
| C.最简单氢化物的键角:Z>Y |
| D.W的单质和某种氧化物可用于自来水的消毒 |
您最近一年使用:0次
8 .  能与
能与 生成
生成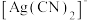 ,常用于自然界中提取银或废液中回收银。
,常用于自然界中提取银或废液中回收银。
(1)已知Ag在第五周期,与Cu同族, 的价层电子排布式为
的价层电子排布式为_______ 。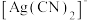 中
中_______ 原子提供孤电子对。
(2)向AgCl悬浊液中加入少量NaCN粉末,沉淀会逐渐溶解。此过程也可以表示为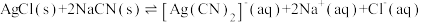 ,则此反应的
,则此反应的
_______ 。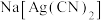 溶液中加入
溶液中加入 ,生成黑色沉淀,存在以下平衡:
,生成黑色沉淀,存在以下平衡:
ⅰ.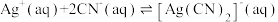
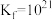 ;
;
ⅱ.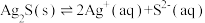
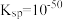 。
。
①下列说法正确的是_______ (填标号)。
A.加入 时,反应ⅰ的平衡逆向移动,其平衡常数
时,反应ⅰ的平衡逆向移动,其平衡常数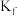 减小
减小
B.随着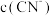 增大,
增大,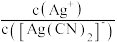 减小
减小
C.溶液中存在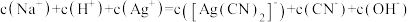
D.加水稀释,反应ⅱ的平衡正向移动, 增大
增大
②反应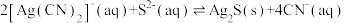

_______ (用 、
、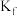 表示)。
表示)。
(4)由于 有剧毒,生产中常改用
有剧毒,生产中常改用 提取
提取 。
。
已知: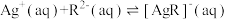
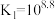 ;
;
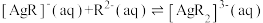
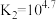 。
。
向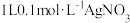 溶液中加入
溶液中加入 固体,得到澄清溶液(溶液体积不变),溶液中
固体,得到澄清溶液(溶液体积不变),溶液中 、
、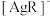 、
、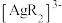 的物质的量分数
的物质的量分数 随
随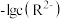 的变化如图所示。
的变化如图所示。 。
。
①曲线_______ (填标号)表示 的变化。
的变化。
②m点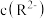 约为
约为_______  。
。
 能与
能与 生成
生成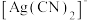 ,常用于自然界中提取银或废液中回收银。
,常用于自然界中提取银或废液中回收银。(1)已知Ag在第五周期,与Cu同族,
 的价层电子排布式为
的价层电子排布式为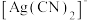 中
中(2)向AgCl悬浊液中加入少量NaCN粉末,沉淀会逐渐溶解。此过程也可以表示为
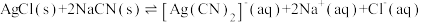 ,则此反应的
,则此反应的
已知: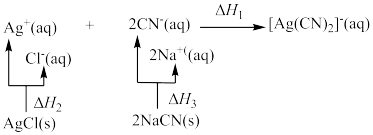
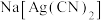 溶液中加入
溶液中加入 ,生成黑色沉淀,存在以下平衡:
,生成黑色沉淀,存在以下平衡:ⅰ.
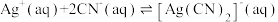
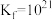 ;
;ⅱ.
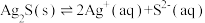
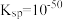 。
。①下列说法正确的是
A.加入
 时,反应ⅰ的平衡逆向移动,其平衡常数
时,反应ⅰ的平衡逆向移动,其平衡常数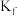 减小
减小B.随着
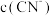 增大,
增大,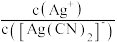 减小
减小C.溶液中存在
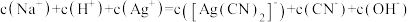
D.加水稀释,反应ⅱ的平衡正向移动,
 增大
增大②反应
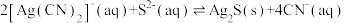

 、
、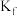 表示)。
表示)。(4)由于
 有剧毒,生产中常改用
有剧毒,生产中常改用 提取
提取 。
。已知:
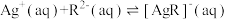
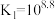 ;
;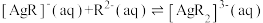
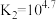 。
。向
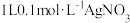 溶液中加入
溶液中加入 固体,得到澄清溶液(溶液体积不变),溶液中
固体,得到澄清溶液(溶液体积不变),溶液中 、
、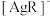 、
、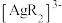 的物质的量分数
的物质的量分数 随
随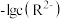 的变化如图所示。
的变化如图所示。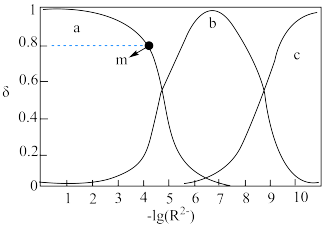
 。
。①曲线
 的变化。
的变化。②m点
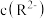 约为
约为 。
。
您最近一年使用:0次
解题方法
9 . 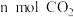 与
与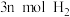 在恒容容器的不同温度下发生反应:
在恒容容器的不同温度下发生反应: ,达到平衡时各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
,达到平衡时各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
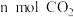 与
与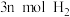 在恒容容器的不同温度下发生反应:
在恒容容器的不同温度下发生反应: ,达到平衡时各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
,达到平衡时各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是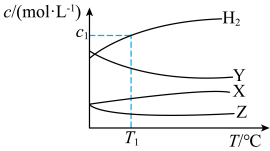
A.该反应的 |
B.曲线Y表示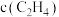 随温度的变化关系 随温度的变化关系 |
C.升高温度,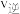 加快, 加快,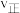 减慢, 减慢,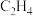 平衡产率减小 平衡产率减小 |
D.其他条件不变,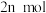  与 与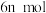  在 在 ℃下反应,达到平衡时 ℃下反应,达到平衡时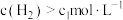 |
您最近一年使用:0次
2024-09-04更新
|
602次组卷
|
3卷引用:广东省2025届高三一调模拟卷化学试题
解题方法
10 . 某学习小组按下图流程,在实验室模拟处理含苯酚的工业废水,并进行相关实验探究。回答下列问题:___________ 。操作Ⅰ、Ⅱ、Ⅲ共同用到的玻璃仪器除烧杯外还有___________ (填名称),流程中可循环使用的物质是___________ 。
(2)“水层2”中主要溶质为___________ (填化学式),其在生活中主要用途是___________ (填一个即可)。
(3)将所得苯酚配制成一定浓度的苯酚溶液,探究铁盐种类和pH对苯酚与 显色反应的影响。
显色反应的影响。
【查阅资料】 ⅰ.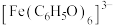 为紫色:
为紫色:
ⅱ. 对苯酚与
对苯酚与 的显色反应无影响;
的显色反应无影响;
ⅲ.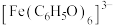 对特定波长光的吸收程度(用吸光度A表示)与
对特定波长光的吸收程度(用吸光度A表示)与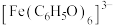 的浓度在一定范围内成正比。
的浓度在一定范围内成正比。
【提出猜想】猜想1: 对苯酚与
对苯酚与 的显色反应有影响。
的显色反应有影响。
猜想2: 对苯酚与
对苯酚与 的显色反应有影响。
的显色反应有影响。
猜想3: 对苯酚与
对苯酚与 的显色反应有影响。
的显色反应有影响。
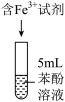
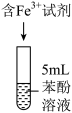
【进行实验】常温下,用盐酸调节pH配制得到pH分别为a和b的
 溶液(
溶液( ),用硫酸调节pH配制得到pH分别为a和b的
),用硫酸调节pH配制得到pH分别为a和b的
 溶液。取5mL苯酚溶液于试管中,按实验1~4分别再加入0.1mL含
溶液。取5mL苯酚溶液于试管中,按实验1~4分别再加入0.1mL含 的试剂,显色10min后用紫外-可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对
的试剂,显色10min后用紫外-可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对 水解程度的影响可忽略)。
水解程度的影响可忽略)。
结果讨论实验结果为 。
。
①小组同学认为根据结果“ ”不足以证明猜想3成立的理由是
”不足以证明猜想3成立的理由是___________ 。
②为进一步验证猜想,小组同学设计了实验5和6,补充下表中相关内容。
(限选试剂: 溶液、
溶液、 溶液、
溶液、 固体、
固体、 固体)
固体)
③根据实验1~6的结果,小组同学得出猜想1不成立,猜想2成立,且 对苯酚与
对苯酚与 的显色反应起抑制作用,得出此结论的依据是
的显色反应起抑制作用,得出此结论的依据是___________ 。
④根据实验1~6的结果,小组同学得出猜想3成立,且 对苯酚与
对苯酚与 的显色反应有抑制作用,从化学平衡角度解释其原因是
的显色反应有抑制作用,从化学平衡角度解释其原因是___________ 。
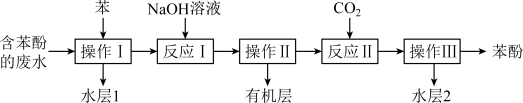
(2)“水层2”中主要溶质为
(3)将所得苯酚配制成一定浓度的苯酚溶液,探究铁盐种类和pH对苯酚与
 显色反应的影响。
显色反应的影响。【查阅资料】 ⅰ.
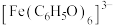 为紫色:
为紫色:ⅱ.
 对苯酚与
对苯酚与 的显色反应无影响;
的显色反应无影响;ⅲ.
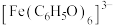 对特定波长光的吸收程度(用吸光度A表示)与
对特定波长光的吸收程度(用吸光度A表示)与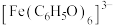 的浓度在一定范围内成正比。
的浓度在一定范围内成正比。【提出猜想】猜想1:
 对苯酚与
对苯酚与 的显色反应有影响。
的显色反应有影响。猜想2:
 对苯酚与
对苯酚与 的显色反应有影响。
的显色反应有影响。猜想3:
 对苯酚与
对苯酚与 的显色反应有影响。
的显色反应有影响。【进行实验】常温下,用盐酸调节pH配制得到pH分别为a和b的

 溶液(
溶液( ),用硫酸调节pH配制得到pH分别为a和b的
),用硫酸调节pH配制得到pH分别为a和b的
 溶液。取5mL苯酚溶液于试管中,按实验1~4分别再加入0.1mL含
溶液。取5mL苯酚溶液于试管中,按实验1~4分别再加入0.1mL含 的试剂,显色10min后用紫外-可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对
的试剂,显色10min后用紫外-可见分光光度计测定该溶液的吸光度(本实验条件下,pH改变对 水解程度的影响可忽略)。
水解程度的影响可忽略)。
| 序号 | 含 的试剂 的试剂 | 吸光度 | |
  溶液 溶液 |   溶液 溶液 | |||
| 1 |  | / |  | |
| 2 |  | / |  | |
| 3 | / |  |  | |
| 4 | / |  |  | |
 。
。①小组同学认为根据结果“
 ”不足以证明猜想3成立的理由是
”不足以证明猜想3成立的理由是②为进一步验证猜想,小组同学设计了实验5和6,补充下表中相关内容。
(限选试剂:
 溶液、
溶液、 溶液、
溶液、 固体、
固体、 固体)
固体)
| 序号 | 含 的试剂 的试剂 | 再加入的试剂 | 吸光度 | |
  溶液 溶液 |   溶液 溶液 | ||||
| 5 | / |  |  固体 固体 | 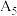 | |
| 6 |  | / | 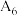 | ||
 对苯酚与
对苯酚与 的显色反应起抑制作用,得出此结论的依据是
的显色反应起抑制作用,得出此结论的依据是④根据实验1~6的结果,小组同学得出猜想3成立,且
 对苯酚与
对苯酚与 的显色反应有抑制作用,从化学平衡角度解释其原因是
的显色反应有抑制作用,从化学平衡角度解释其原因是
您最近一年使用:0次