解题方法
1 . 甲醇是一种重要的化工原料和燃料。利用 和
和 生成甲醇的反应如下:
生成甲醇的反应如下:
反应Ⅰ:

反应Ⅱ:
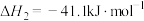
已知:几种化学键的键能数据如下表所示。
(1)结合上表数据,
_______  。反应Ⅱ能自发进行的条件是
。反应Ⅱ能自发进行的条件是_______ (填“低温”“高温”或“任意温度”)。
(2)在120℃,体积恒定的密闭容器中发生反应Ⅰ和Ⅱ。
①若达到平衡后,增大体系的压强,则CO的物质的量_______ (填“增大”“减小”或“不变”),原因是_______ 。
②若通入1mol 和2.5mol
和2.5mol  混合气体,起始压强为0.35MPa,发生反应Ⅰ和Ⅱ.平衡时,总压为0.25MPa,
混合气体,起始压强为0.35MPa,发生反应Ⅰ和Ⅱ.平衡时,总压为0.25MPa, 的转化率为60%,则反应Ⅱ的压强平衡常数
的转化率为60%,则反应Ⅱ的压强平衡常数
_______ 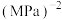 (分压=总压×物质的量分数,列出计算式即可)。
(分压=总压×物质的量分数,列出计算式即可)。
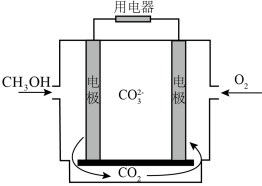
(3)某研究小组自制熔融碳酸盐甲醇燃料电池,工作原理如图所示:_______ 。
②该电池以恒定电流I A工作t min,测得化学能转化为电能的转化率为 ,则消耗甲醇
,则消耗甲醇_______ kg(已知:一个电子的电量为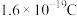 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 )。
)。
 和
和 生成甲醇的反应如下:
生成甲醇的反应如下:反应Ⅰ:


反应Ⅱ:

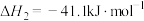
已知:几种化学键的键能数据如下表所示。
化学键 |
|
|
|
|
键能/ | 436 | 803 | 1071 | 463 |
(1)结合上表数据,

 。反应Ⅱ能自发进行的条件是
。反应Ⅱ能自发进行的条件是(2)在120℃,体积恒定的密闭容器中发生反应Ⅰ和Ⅱ。
①若达到平衡后,增大体系的压强,则CO的物质的量
②若通入1mol
 和2.5mol
和2.5mol  混合气体,起始压强为0.35MPa,发生反应Ⅰ和Ⅱ.平衡时,总压为0.25MPa,
混合气体,起始压强为0.35MPa,发生反应Ⅰ和Ⅱ.平衡时,总压为0.25MPa, 的转化率为60%,则反应Ⅱ的压强平衡常数
的转化率为60%,则反应Ⅱ的压强平衡常数
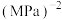 (分压=总压×物质的量分数,列出计算式即可)。
(分压=总压×物质的量分数,列出计算式即可)。(3)某研究小组自制熔融碳酸盐甲醇燃料电池,工作原理如图所示:
②该电池以恒定电流I A工作t min,测得化学能转化为电能的转化率为
 ,则消耗甲醇
,则消耗甲醇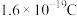 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
7日内更新
|
529次组卷
|
4卷引用:2025届广东省广州市高三上学期8月第一次调研考试化学试卷
名校
2 . 美沙拉嗪是治疗溃疡性结肠炎的活性成分,对肠壁的炎症有显著的抑制作用。该有机物的结构如图所示,下列说法错误的是
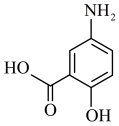
| A.该物质有三种官能团 |
| B.该物质既可以与酸反应也可以与碱反应 |
C.1mol该物质最多可以与 反应 反应 |
| D.该物质可以发生酯化反应 |
您最近一年使用:0次
2024-09-14更新
|
177次组卷
|
2卷引用:广东省2025届高三上学期8月部分学校摸底测试 化学试题
名校
解题方法
3 . 草酸亚铁晶体( )呈黄色,难溶于水,具有强还原性。用下列装置制备草酸亚铁晶体。
)呈黄色,难溶于水,具有强还原性。用下列装置制备草酸亚铁晶体。
 )呈黄色,难溶于水,具有强还原性。用下列装置制备草酸亚铁晶体。
)呈黄色,难溶于水,具有强还原性。用下列装置制备草酸亚铁晶体。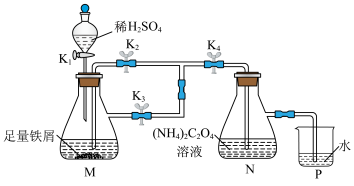
| A.配制溶液的蒸馏水需经煮沸后迅速冷却 |
B.检查气密性后,打开 、 、 、 、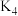 ,关闭 ,关闭 |
C.P中不再冒出气泡时,打开 ,关闭 ,关闭 、 、 |
| D.反应结束将N中混合物过滤、洗涤、干燥得草酸亚铁晶体 |
您最近一年使用:0次
2024-09-13更新
|
732次组卷
|
5卷引用:2025届广东省广州市高三上学期8月第一次调研考试化学试卷
名校
解题方法
4 . 二氧化碳加氢是对温室气体的有效转化,也是合成再生能源与化工原料的重要途径。
(1)已知在25℃和101kPa时,H2和CH4的燃烧热分别为285.8kJ•mol-1和890.3kJ•mol-1。由CO2加氢反应制备CH4的反应为:CO2(g)+4H2(g) CH4(g)+2H2O(l),该反应的反应热△H=
CH4(g)+2H2O(l),该反应的反应热△H=______ 。
(2)①CO2催化加氢可以制低碳烯烃:2CO2(g)+6H2(g) C2H4(g)+4H2O(g),该反应在恒压条件下,反应温度、投料比[
C2H4(g)+4H2O(g),该反应在恒压条件下,反应温度、投料比[ =m]对CO2平衡转化率的影响如图所示,该反应为
=m]对CO2平衡转化率的影响如图所示,该反应为______ 反应(填“吸热”或“放热”),m1、m2、m3的相对大小为______ 。
理论上反应历程中消耗的H*与生成的甲醇的物质的量之比为______ 。
(3)二氧化碳可催化加氢制甲醇。在一定条件下,向某恒容密闭容器中充入CO2和H2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。测得在相同时间内,不同温度下H2的转化率如图所示。
CH3OH(g)+H2O(g)。测得在相同时间内,不同温度下H2的转化率如图所示。______ v(c)逆(填“>”“<”或“=”)。
②下列说法正确的有______ 。
A.b点时达到平衡状态
B.a点时容器内气体密度大于b点
C.平均相对分子质量不再改变时,该反应达到平衡状态
D.温度高于T2后H2转化率下降,原因可能是该反应△H<0
(4)一定条件下CO2可与H2反应制备甲酸。T℃时,将2molCO2与2molH2混合气体充入体积为2L恒容密闭容器发生反应:CO2(g)+H2(g) HCOOH(g)。已知反应速率:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆分别为正、逆反应的速率常数;平衡常数:K=2。当CO2的转化率为20%时,
HCOOH(g)。已知反应速率:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆分别为正、逆反应的速率常数;平衡常数:K=2。当CO2的转化率为20%时, =
=______ (写出计算过程)。
(1)已知在25℃和101kPa时,H2和CH4的燃烧热分别为285.8kJ•mol-1和890.3kJ•mol-1。由CO2加氢反应制备CH4的反应为:CO2(g)+4H2(g)
 CH4(g)+2H2O(l),该反应的反应热△H=
CH4(g)+2H2O(l),该反应的反应热△H=(2)①CO2催化加氢可以制低碳烯烃:2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g),该反应在恒压条件下,反应温度、投料比[
C2H4(g)+4H2O(g),该反应在恒压条件下,反应温度、投料比[ =m]对CO2平衡转化率的影响如图所示,该反应为
=m]对CO2平衡转化率的影响如图所示,该反应为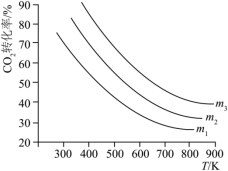
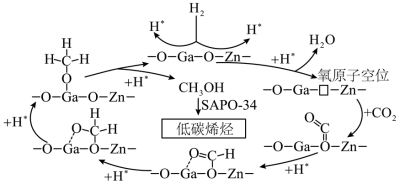
理论上反应历程中消耗的H*与生成的甲醇的物质的量之比为
(3)二氧化碳可催化加氢制甲醇。在一定条件下,向某恒容密闭容器中充入CO2和H2,发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。测得在相同时间内,不同温度下H2的转化率如图所示。
CH3OH(g)+H2O(g)。测得在相同时间内,不同温度下H2的转化率如图所示。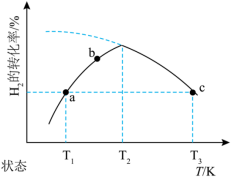
②下列说法正确的有
A.b点时达到平衡状态
B.a点时容器内气体密度大于b点
C.平均相对分子质量不再改变时,该反应达到平衡状态
D.温度高于T2后H2转化率下降,原因可能是该反应△H<0
(4)一定条件下CO2可与H2反应制备甲酸。T℃时,将2molCO2与2molH2混合气体充入体积为2L恒容密闭容器发生反应:CO2(g)+H2(g)
 HCOOH(g)。已知反应速率:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆分别为正、逆反应的速率常数;平衡常数:K=2。当CO2的转化率为20%时,
HCOOH(g)。已知反应速率:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆分别为正、逆反应的速率常数;平衡常数:K=2。当CO2的转化率为20%时, =
=
您最近一年使用:0次
名校
5 . 有机物的世界缤纷多彩,回答下列问题:
苯乙烯在一定条件下有如图转化关系 反应生成B的实验现象为
反应生成B的实验现象为___________ ,1mol苯乙烯最多能和___________ mol的 的溶液反应。
的溶液反应。
(2)苯乙烯生成高聚物D的的化学方程式为___________ ,该反应类型是___________ 。
(3)苯乙烯与水反应生成C的可能生成物有___________ 、___________ 。
(4)苯乙烯与足量 一定条件下充分反应的生成物A的分子式为
一定条件下充分反应的生成物A的分子式为___________ ,A的一氯代物有___________ 种,有机物 (正二十烷)存在于烤烟烟叶中,正二十烷与A的关系是
(正二十烷)存在于烤烟烟叶中,正二十烷与A的关系是___________ 。
A.同分异构体 B.同系物 C.同素异形体 D.都不是
苯乙烯在一定条件下有如图转化关系

 反应生成B的实验现象为
反应生成B的实验现象为 的溶液反应。
的溶液反应。(2)苯乙烯生成高聚物D的的化学方程式为
(3)苯乙烯与水反应生成C的可能生成物有
(4)苯乙烯与足量
 一定条件下充分反应的生成物A的分子式为
一定条件下充分反应的生成物A的分子式为 (正二十烷)存在于烤烟烟叶中,正二十烷与A的关系是
(正二十烷)存在于烤烟烟叶中,正二十烷与A的关系是A.同分异构体 B.同系物 C.同素异形体 D.都不是
您最近一年使用:0次
6 . 铁(Fe)、钴(Co)、镍(Ni)是第四周期第Ⅷ族的元素,称为铁系元素,相关化合物在生产生活中应用广泛。
(1)铁在元素周期表中位置(周期、族)为___________ ,属于___________ 区,基态 的价电子排布式为
的价电子排布式为___________ 。
(2)铁系元素能与CO形成 、
、 等金属羰基化合物。金属羰基化合物的配位原子为(填元素名称),其更容易进行配位的原因是
等金属羰基化合物。金属羰基化合物的配位原子为(填元素名称),其更容易进行配位的原因是___________ 。CO与 结构相似,其中CO分子内
结构相似,其中CO分子内 键和
键和 键的个数比为
键的个数比为___________ 。
(3)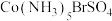 可形成两种钴的配合物。已知
可形成两种钴的配合物。已知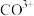 的配位数是6,为确定钴的配合物的结构,对两种配合物进行了如下实验:在第一种配合物的溶液中加
的配位数是6,为确定钴的配合物的结构,对两种配合物进行了如下实验:在第一种配合物的溶液中加 溶液时,产生白色沉淀,在第二种配合物的溶液中加
溶液时,产生白色沉淀,在第二种配合物的溶液中加 溶液时,则无明显现象。则第一种配合物的结构式可表示为
溶液时,则无明显现象。则第一种配合物的结构式可表示为___________ ,第二种配合物的结构式可表示为___________ 。若在第二种配合物的溶液中滴加 溶液,则产生的现象是
溶液,则产生的现象是___________ 。(提示: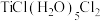 这种配合物的结构式可表示为
这种配合物的结构式可表示为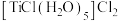 )
)
(4)NiO晶胞与NaCl晶胞相似,如图所示:___________ 个。晶胞参数为apm, 代表阿伏伽德罗常数的值。则NiO晶体的密度为
代表阿伏伽德罗常数的值。则NiO晶体的密度为___________  (只列出计算式)。
(只列出计算式)。
(1)铁在元素周期表中位置(周期、族)为
 的价电子排布式为
的价电子排布式为(2)铁系元素能与CO形成
 、
、 等金属羰基化合物。金属羰基化合物的配位原子为(填元素名称),其更容易进行配位的原因是
等金属羰基化合物。金属羰基化合物的配位原子为(填元素名称),其更容易进行配位的原因是 结构相似,其中CO分子内
结构相似,其中CO分子内 键和
键和 键的个数比为
键的个数比为(3)
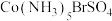 可形成两种钴的配合物。已知
可形成两种钴的配合物。已知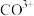 的配位数是6,为确定钴的配合物的结构,对两种配合物进行了如下实验:在第一种配合物的溶液中加
的配位数是6,为确定钴的配合物的结构,对两种配合物进行了如下实验:在第一种配合物的溶液中加 溶液时,产生白色沉淀,在第二种配合物的溶液中加
溶液时,产生白色沉淀,在第二种配合物的溶液中加 溶液时,则无明显现象。则第一种配合物的结构式可表示为
溶液时,则无明显现象。则第一种配合物的结构式可表示为 溶液,则产生的现象是
溶液,则产生的现象是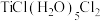 这种配合物的结构式可表示为
这种配合物的结构式可表示为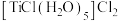 )
)(4)NiO晶胞与NaCl晶胞相似,如图所示:
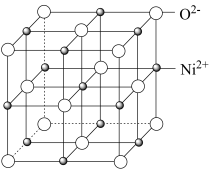
 代表阿伏伽德罗常数的值。则NiO晶体的密度为
代表阿伏伽德罗常数的值。则NiO晶体的密度为 (只列出计算式)。
(只列出计算式)。
您最近一年使用:0次
名校
7 .  、
、 、
、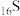 、
、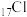 是周期表中的短周期主族元素。下列有关说法正确的是
是周期表中的短周期主族元素。下列有关说法正确的是
 、
、 、
、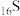 、
、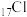 是周期表中的短周期主族元素。下列有关说法正确的是
是周期表中的短周期主族元素。下列有关说法正确的是A.键角: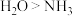 | B.第一电离能: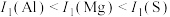 |
C.碱性: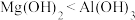 | D.半径: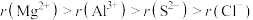 |
您最近一年使用:0次
名校
8 . 下列化学实验中的操作、现象及解释有正确对应关系的是
| 选项 | 操作 | 现象 | 解释 |
| A | 向酸性 溶液中加入甲苯 溶液中加入甲苯 | 溶液褪色 | 苯环对甲基有影响 |
| B | 将含有稀硫酸的蔗糖溶液水浴加热后,加入新制氢氧化铜悬浊液并加热 | 没有产生红色沉淀 | 蔗糖未水解 |
| C | 将乙醇与浓硫酸共热至170℃所得气体直接通入酸性KMnO溶液中 | 溶液褪色 | 气体中含有乙烯 |
| D | 向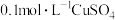 溶液里逐滴加入 溶液里逐滴加入 氨水至过量 氨水至过量 | 先形成蓝色沉淀,后溶解得到深蓝色溶液 | 沉淀溶解时主要反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 电致变色材料在飞机的舷窗上广泛应用,一种新一代集电致变色功能和储能功能于一体的电子器件的工作原理如图所示,接通电源后,该器件的透光率逐渐降低,可以有效阻碍强光射入。下列说法正确的是
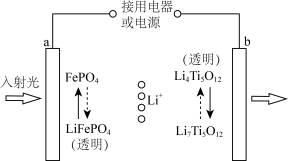
| A.接通电源后,电子从电源流入a极 |
| B.接通电源后,当电路中转移1mol电子,a极质量增加7g |
C.以此为电源电解精炼铜,则此装置中有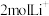 移动时,精炼池的阳极减轻64g 移动时,精炼池的阳极减轻64g |
D.接用电器时,b极发生反应: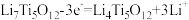 |
您最近一年使用:0次
名校
解题方法
10 . 乙烯在硫酸催化下制取乙醇的反应机理,能量与反应进程的关系如图所示。下列叙述正确的是
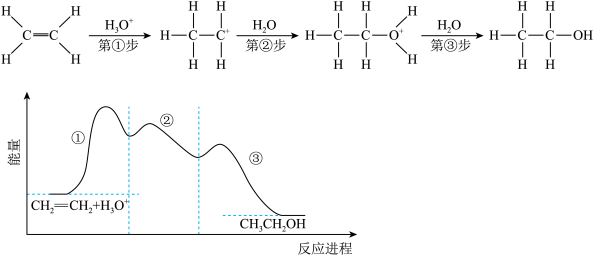
| A.第②步反应过渡态物质比第③步反应过渡态物质稳定 |
| B.总反应在任何条件下都能自发进行 |
| C.总反应速率由第①步反应决定 |
| D.第①、②、③步反应都是放热反应 |
您最近一年使用:0次
2024-09-07更新
|
275次组卷
|
2卷引用:广东省东莞中学松山湖学校2025届高三上学期8月模拟考试化学试题







