1 . 某废水处理过程中始终保持 饱和,即
饱和,即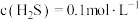 ,通过调节
,通过调节 使
使 和
和 形成硫化物而分离,体系中
形成硫化物而分离,体系中 与
与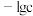 关系如图所示,c为
关系如图所示,c为 、
、 、
、 和
和 的浓度,单位为
的浓度,单位为 。已知
。已知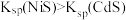 ,下列说法正确的是
,下列说法正确的是
 饱和,即
饱和,即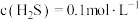 ,通过调节
,通过调节 使
使 和
和 形成硫化物而分离,体系中
形成硫化物而分离,体系中 与
与 关系如图所示,c为
关系如图所示,c为 、
、 、
、 和
和 的浓度,单位为
的浓度,单位为 。已知
。已知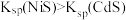 ,下列说法正确的是
,下列说法正确的是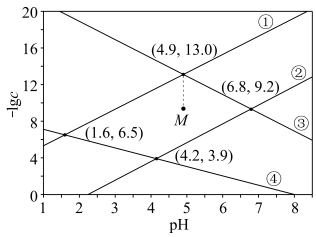
A.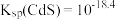 |
B.M点条件下能生成 沉淀,不能生成 沉淀,不能生成 沉淀 沉淀 |
C.③为 与 与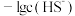 的关系曲线 的关系曲线 |
D.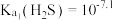 |
您最近一年使用:0次
2 . 三盐基硫酸铅简称“三盐”,是一种重要的工业原料,其化学式为 (相对分子质量为990)。以
(相对分子质量为990)。以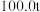 铅泥(主要成分为
铅泥(主要成分为 、
、 及
及 等,
等, 、
、 不与
不与 溶液反应)为原料制备三盐的工艺流程如图所示。
溶液反应)为原料制备三盐的工艺流程如图所示。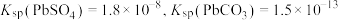 。
。
回答下列问题:
(1)“转化”时 发生反应的离子方程式为
发生反应的离子方程式为_______ ,反应达到平衡时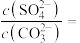
_______ 。
(2)“酸溶”时若有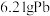 发生反应,则生成
发生反应,则生成 的体积(标准状况)为
的体积(标准状况)为_______  ,为提高“酸溶”速率,可采取的措施是
,为提高“酸溶”速率,可采取的措施是_______ (任意写出一条)。
(3)“滤液2”中溶质的主要成分的化学式为_______ 。
(4)“合成”时主要反应的化学方程式为_______ 。
(5)若得到纯净干燥的三盐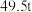 ,假设铅泥中的铅元素有
,假设铅泥中的铅元素有 转化为三盐,则铅泥中央铅元素的质量分数为
转化为三盐,则铅泥中央铅元素的质量分数为_______  。
。
 (相对分子质量为990)。以
(相对分子质量为990)。以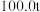 铅泥(主要成分为
铅泥(主要成分为 、
、 及
及 等,
等, 、
、 不与
不与 溶液反应)为原料制备三盐的工艺流程如图所示。
溶液反应)为原料制备三盐的工艺流程如图所示。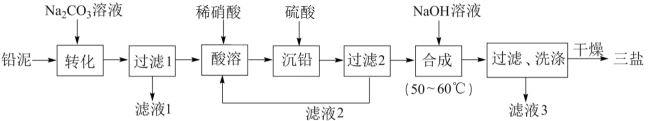
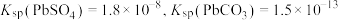 。
。回答下列问题:
(1)“转化”时
 发生反应的离子方程式为
发生反应的离子方程式为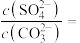
(2)“酸溶”时若有
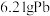 发生反应,则生成
发生反应,则生成 的体积(标准状况)为
的体积(标准状况)为 ,为提高“酸溶”速率,可采取的措施是
,为提高“酸溶”速率,可采取的措施是(3)“滤液2”中溶质的主要成分的化学式为
(4)“合成”时主要反应的化学方程式为
(5)若得到纯净干燥的三盐
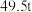 ,假设铅泥中的铅元素有
,假设铅泥中的铅元素有 转化为三盐,则铅泥中央铅元素的质量分数为
转化为三盐,则铅泥中央铅元素的质量分数为 。
。
您最近一年使用:0次
3 . 常温下,在烧杯中将0.025 mol  粉末加水配成1 L悬浊液,然后向烧杯中加入
粉末加水配成1 L悬浊液,然后向烧杯中加入 固体并充分搅拌(忽略溶液体积的变化)。加入
固体并充分搅拌(忽略溶液体积的变化)。加入 固体的过程中溶液中几种离子的浓度变化曲线如图。下列说法正确的是
固体的过程中溶液中几种离子的浓度变化曲线如图。下列说法正确的是
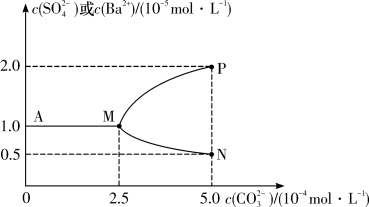
 粉末加水配成1 L悬浊液,然后向烧杯中加入
粉末加水配成1 L悬浊液,然后向烧杯中加入 固体并充分搅拌(忽略溶液体积的变化)。加入
固体并充分搅拌(忽略溶液体积的变化)。加入 固体的过程中溶液中几种离子的浓度变化曲线如图。下列说法正确的是
固体的过程中溶液中几种离子的浓度变化曲线如图。下列说法正确的是
A.常温下,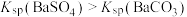 |
B. 在水中的溶解度、 在水中的溶解度、 均比在 均比在 溶液中的大 溶液中的大 |
C.MP曲线表示的是溶液中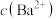 的变化 的变化 |
D. 恰好全部转化为 恰好全部转化为 时,离子浓度大小关系为 时,离子浓度大小关系为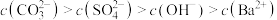 |
您最近一年使用:0次
解题方法
4 . 镍是一种性能优良的金属,在许多领域应用广泛。Ni-NTA-Nangold可用于检测或定位6x组氨酸(His)或Poly-His标记的重组蛋白,Ni(Ⅱ)-NTA的结构简式如图1所示。
(1)基态Ni原子核外电子空间运动状态有_______ 种,其价层电子的轨道表示式为_______ 。
(2)Ni(Ⅱ)-NTA的配体之一为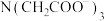 。
。
①Ni(Ⅱ)-NTA中与 配位的原子形成的空间构型为
配位的原子形成的空间构型为_______ 形。
②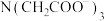 中第二周期元素的第一电离能(
中第二周期元素的第一电离能( )从大到小的顺序为
)从大到小的顺序为_______ (用元素符号表示),其中N原子的杂化方式为_______ 。
(3)Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点Ni明显高于Ca,其原因是_______ 。
(4)某笼形包合物 的晶胞结构如图2所示,其中
的晶胞结构如图2所示,其中 位于面心。
位于面心。_______ 。
②该包合物中氨与苯分子数目之比为_______ , 极易溶于水,而
极易溶于水,而 微溶于水,其原因是
微溶于水,其原因是_______ 。
③若此晶胞体积为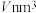 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该晶体密度为
,该晶体密度为_______  。
。
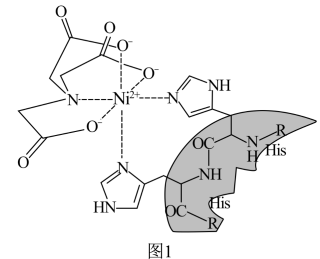
(1)基态Ni原子核外电子空间运动状态有
(2)Ni(Ⅱ)-NTA的配体之一为
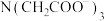 。
。①Ni(Ⅱ)-NTA中与
 配位的原子形成的空间构型为
配位的原子形成的空间构型为②
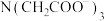 中第二周期元素的第一电离能(
中第二周期元素的第一电离能( )从大到小的顺序为
)从大到小的顺序为(3)Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点Ni明显高于Ca,其原因是
(4)某笼形包合物
 的晶胞结构如图2所示,其中
的晶胞结构如图2所示,其中 位于面心。
位于面心。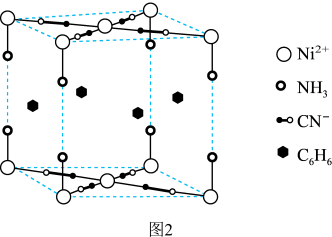
②该包合物中氨与苯分子数目之比为
 极易溶于水,而
极易溶于水,而 微溶于水,其原因是
微溶于水,其原因是③若此晶胞体积为
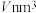 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该晶体密度为
,该晶体密度为 。
。
您最近一年使用:0次
5 .  的资源化途径有多种,其中包括甲烷化、碳酸二甲酯化等。回答下列问题:
的资源化途径有多种,其中包括甲烷化、碳酸二甲酯化等。回答下列问题:
(1) 甲烷化:利用
甲烷化:利用 与
与 合成
合成 ,主要涉及以下反应:
,主要涉及以下反应:
ⅰ.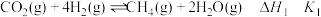 ;
;
ⅱ.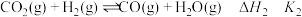 ;
;
ⅲ.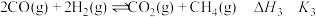 。
。
①上述反应的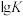 (
( 为平衡常数)随温度
为平衡常数)随温度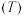 的变化如图1所示,其中属于吸热反应的有
的变化如图1所示,其中属于吸热反应的有_______ (填序号),
_______ (用 、
、 表示)。
表示)。 、
、 ,仅发生反应ⅰ。下列说法正确的是
,仅发生反应ⅰ。下列说法正确的是_______ (填字母)。
A升高温度,反应速率加快,活化能降低
B.使用高效的催化剂能提高单位时间内 的产率
的产率
C.当混合气体的压强保持不变时,反应达到平衡状态
D.反应达到平衡后,其他条件不变,向该容器通入Ar,平衡正向移动
(2)向恒压(pMPa)、密闭容器中通入1mol 和4mol
和4mol ,在催化剂的作用下仅发生反应ⅰ、ⅱ,平衡时
,在催化剂的作用下仅发生反应ⅰ、ⅱ,平衡时 、CO、
、CO、 的物质的量随温度的变化如图2所示。
的物质的量随温度的变化如图2所示。_______ (填化学式);当温度高于 ℃,B物质的量随温度升高而减少的主要原因是
℃,B物质的量随温度升高而减少的主要原因是_______ 。
②在 ℃时,平衡体系中
℃时,平衡体系中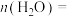
_______ mol,反应ⅱ的压强平衡常数
_______ (保留分数形式,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)碳酸二甲酯化:由 催化
催化 合成碳酸二甲酯(DMC)的反应过程如图3所示。
合成碳酸二甲酯(DMC)的反应过程如图3所示。_______ (填“a”“b”或“c”),合成DMC的总反应的化学方程式为_______ (标注同位素原子)。
 的资源化途径有多种,其中包括甲烷化、碳酸二甲酯化等。回答下列问题:
的资源化途径有多种,其中包括甲烷化、碳酸二甲酯化等。回答下列问题:(1)
 甲烷化:利用
甲烷化:利用 与
与 合成
合成 ,主要涉及以下反应:
,主要涉及以下反应:ⅰ.
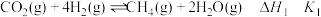 ;
;ⅱ.
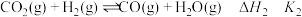 ;
;ⅲ.
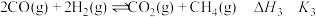 。
。①上述反应的
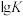 (
( 为平衡常数)随温度
为平衡常数)随温度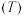 的变化如图1所示,其中属于吸热反应的有
的变化如图1所示,其中属于吸热反应的有
 、
、 表示)。
表示)。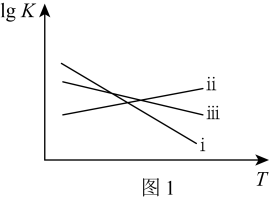
 、
、 ,仅发生反应ⅰ。下列说法正确的是
,仅发生反应ⅰ。下列说法正确的是A升高温度,反应速率加快,活化能降低
B.使用高效的催化剂能提高单位时间内
 的产率
的产率C.当混合气体的压强保持不变时,反应达到平衡状态
D.反应达到平衡后,其他条件不变,向该容器通入Ar,平衡正向移动
(2)向恒压(pMPa)、密闭容器中通入1mol
 和4mol
和4mol ,在催化剂的作用下仅发生反应ⅰ、ⅱ,平衡时
,在催化剂的作用下仅发生反应ⅰ、ⅱ,平衡时 、CO、
、CO、 的物质的量随温度的变化如图2所示。
的物质的量随温度的变化如图2所示。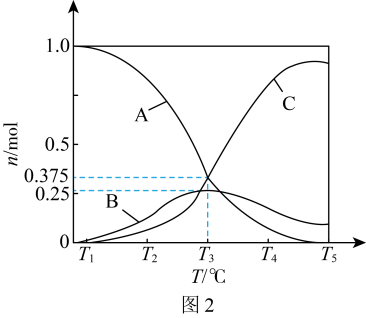
 ℃,B物质的量随温度升高而减少的主要原因是
℃,B物质的量随温度升高而减少的主要原因是②在
 ℃时,平衡体系中
℃时,平衡体系中

(3)碳酸二甲酯化:由
 催化
催化 合成碳酸二甲酯(DMC)的反应过程如图3所示。
合成碳酸二甲酯(DMC)的反应过程如图3所示。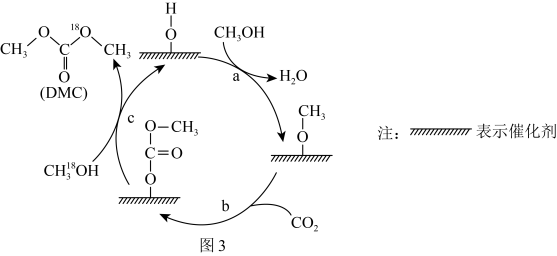
您最近一年使用:0次
解题方法
6 . 某工厂通过如下装置处理两个车间的废气(电极均为惰性电极),既处理了污染物,又变废为宝。下列说法正确的是
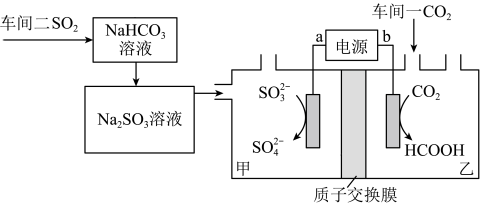
A.电极电势: |
B.工作时 由乙池移向甲池 由乙池移向甲池 |
C.通电一段时间后甲区域的 增大 增大 |
D.阴极反应式: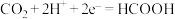 |
您最近一年使用:0次
解题方法
7 . 实验室利用以下装置配制2 的稀硝酸并制取NO,其中装置及操作均正确且能达到实验目的的是
的稀硝酸并制取NO,其中装置及操作均正确且能达到实验目的的是
 的稀硝酸并制取NO,其中装置及操作均正确且能达到实验目的的是
的稀硝酸并制取NO,其中装置及操作均正确且能达到实验目的的是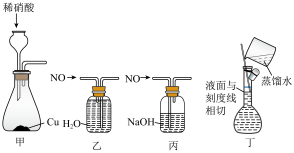
| A.用装置甲制备NO气体 | B.用装置乙收集NO气体 |
| C.用装置丙进行NO的尾气吸收 | D.用装置丁配制100mL2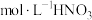 溶液 溶液 |
您最近一年使用:0次
解题方法
8 . 麻沸散的有效成分之一东莨菪碱(M)的结构简式如图所示。下列有关M的说法正确的是
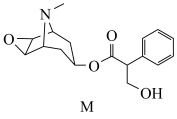
| A.属于苯的同系物 | B.分子中所有原子共面 |
| C.不能在较强碱性环境中稳定存在 | D.苯环上的一氯代物有4种(不考虑立体异构) |
您最近一年使用:0次
解题方法
9 . 神舟五号的发射标志着我国成为世界上第三个独立自主完整掌握载人航天技术的国家。下列说法正确的是
| A.特种陶瓷碳化硅属于硅酸盐 |
| B.铝合金材料强度高、密度大、耐腐蚀 |
| C.聚甲基丙烯酰亚胺属于天然有机高分子材料 |
| D.用于制造精密计时原子钟的铷(Rb)是第ⅠA族元素 |
您最近一年使用:0次
解题方法
10 . 连二亚硫酸钠( )在空气中极易被氧化,不溶于乙醇,在碱性介质中较稳定,低于52℃时
)在空气中极易被氧化,不溶于乙醇,在碱性介质中较稳定,低于52℃时 在水溶液中以
在水溶液中以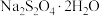 形态结晶,高于52℃时
形态结晶,高于52℃时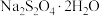 在碱性溶液中脱水成无水盐。实验室制备
在碱性溶液中脱水成无水盐。实验室制备 的原理为
的原理为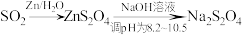 (
( 易溶于水),实验装置如图1所示(夹持仪器已省略),实验步骤如下:
易溶于水),实验装置如图1所示(夹持仪器已省略),实验步骤如下:
ⅱ.向三颈烧瓶中依次加入Zn粉和水,电磁搅拌形成悬浊液;
ⅲ.打开仪器a的活塞,向装置C中通入一段时间 ;
;
ⅳ.打开仪器c的活塞,滴加稍过量NaOH溶液,控制pH在8.2~10.5之间[ 呈现两性,pH>10.5时其开始溶解];
呈现两性,pH>10.5时其开始溶解];
ⅴ.过滤,滤液经一系列操作可获得 。
。
回答下列问题:
(1)仪器b的名称是_______ ,该仪器中发生反应的化学方程式为_______ 。
(2)装置B单向阀的作用是_______ ;步骤ⅲ中装置C的水浴温度应控制为35~45℃之间,其原因是_______ 。
(3)下列关于步骤ⅳ的说法错误的是_______(填字母)。
(4)“一系列操作”包括:a.趁热过滤;b.用乙醇洗涤;c.搅拌下用水蒸气加热至60℃左右;d.分批加入细食盐粉,搅拌使其结晶,用倾析法除去上层溶液,余少量母液。上述操作的合理顺序为_______ →干燥(填字母)。
(5)电解法制备 的原理如图2所示,M、N均为惰性电极,充分电解后左池的溶质主要为
的原理如图2所示,M、N均为惰性电极,充分电解后左池的溶质主要为 、NaOH。M极电极反应式为
、NaOH。M极电极反应式为_______ 。 样品纯度的测定(假设杂质不参与反应,实验过程需在氮气氛围中进行):称取0.2500g样品加入三颈烧瓶中,加入适量NaOH溶液,打开电磁搅拌器,通过滴定仪控制滴定管向三颈烧瓶中快速滴加0.1000
样品纯度的测定(假设杂质不参与反应,实验过程需在氮气氛围中进行):称取0.2500g样品加入三颈烧瓶中,加入适量NaOH溶液,打开电磁搅拌器,通过滴定仪控制滴定管向三颈烧瓶中快速滴加0.1000 的
的 标准溶液,达到滴定终点时消耗25.00mL标准溶液{
标准溶液,达到滴定终点时消耗25.00mL标准溶液{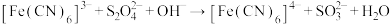 (未配平)}。
(未配平)}。
①该样品的纯度为_______ %。
②若实验过程中未通入 ,则所测
,则所测 的纯度
的纯度_______ (填“偏低”“偏高”或“无影响”)。
 )在空气中极易被氧化,不溶于乙醇,在碱性介质中较稳定,低于52℃时
)在空气中极易被氧化,不溶于乙醇,在碱性介质中较稳定,低于52℃时 在水溶液中以
在水溶液中以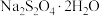 形态结晶,高于52℃时
形态结晶,高于52℃时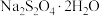 在碱性溶液中脱水成无水盐。实验室制备
在碱性溶液中脱水成无水盐。实验室制备 的原理为
的原理为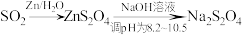 (
( 易溶于水),实验装置如图1所示(夹持仪器已省略),实验步骤如下:
易溶于水),实验装置如图1所示(夹持仪器已省略),实验步骤如下: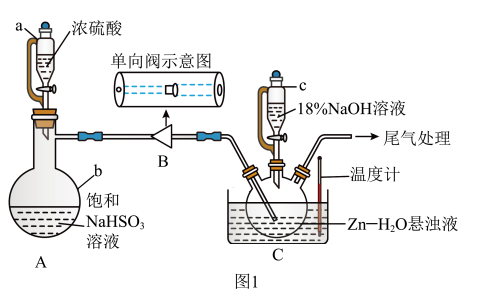
ⅱ.向三颈烧瓶中依次加入Zn粉和水,电磁搅拌形成悬浊液;
ⅲ.打开仪器a的活塞,向装置C中通入一段时间
 ;
;ⅳ.打开仪器c的活塞,滴加稍过量NaOH溶液,控制pH在8.2~10.5之间[
 呈现两性,pH>10.5时其开始溶解];
呈现两性,pH>10.5时其开始溶解];ⅴ.过滤,滤液经一系列操作可获得
 。
。回答下列问题:
(1)仪器b的名称是
(2)装置B单向阀的作用是
(3)下列关于步骤ⅳ的说法错误的是_______(填字母)。
A.pH过大 沉淀完全,且 沉淀完全,且 能稳定存在 能稳定存在 |
B.pH过小 会沉淀不完全,产品中会产生含锌杂质 会沉淀不完全,产品中会产生含锌杂质 |
| C.装置C中18%NaOH溶液应用无氧水配制 |
| D.不可以用碳酸钠溶液代替氢氧化钠溶液 |
(4)“一系列操作”包括:a.趁热过滤;b.用乙醇洗涤;c.搅拌下用水蒸气加热至60℃左右;d.分批加入细食盐粉,搅拌使其结晶,用倾析法除去上层溶液,余少量母液。上述操作的合理顺序为
(5)电解法制备
 的原理如图2所示,M、N均为惰性电极,充分电解后左池的溶质主要为
的原理如图2所示,M、N均为惰性电极,充分电解后左池的溶质主要为 、NaOH。M极电极反应式为
、NaOH。M极电极反应式为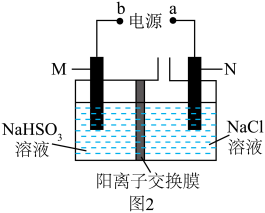
 样品纯度的测定(假设杂质不参与反应,实验过程需在氮气氛围中进行):称取0.2500g样品加入三颈烧瓶中,加入适量NaOH溶液,打开电磁搅拌器,通过滴定仪控制滴定管向三颈烧瓶中快速滴加0.1000
样品纯度的测定(假设杂质不参与反应,实验过程需在氮气氛围中进行):称取0.2500g样品加入三颈烧瓶中,加入适量NaOH溶液,打开电磁搅拌器,通过滴定仪控制滴定管向三颈烧瓶中快速滴加0.1000 的
的 标准溶液,达到滴定终点时消耗25.00mL标准溶液{
标准溶液,达到滴定终点时消耗25.00mL标准溶液{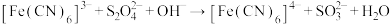 (未配平)}。
(未配平)}。①该样品的纯度为
②若实验过程中未通入
 ,则所测
,则所测 的纯度
的纯度
您最近一年使用:0次



