解题方法
1 . 化学与生活密切相关,下列说法正确的是
| A.苯甲酸钠可作为食品防腐剂是由于其具有酸性 |
| B.含磷污水是很好的肥料,可灌溉庄稼,可直接排放到自然界水体中 |
| C.硅酸钠的水溶液俗称水玻璃,可用作木材防火剂 |
| D.化妆品中的甘油难溶于水 |
您最近一年使用:0次
2 . 丙烯是三大合成材料的基本原料之一,可用于生产多种重要有机化工原料。由丙烷制丙烯的两种方法如下:
I.丙烷无氧脱氢法:
II.丙烷氧化脱氢法:
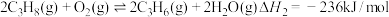
(1)已知 ,由此计算
,由此计算
___________  ,该反应的正反应活化能
,该反应的正反应活化能 (正)
(正)___________ 逆反应活化能 (逆)(填“>”或“<”)。
(逆)(填“>”或“<”)。
(2)一定温度下,在恒容密闭容器中充入 发生反应I,下列能说明该反应达到平衡状态的是
发生反应I,下列能说明该反应达到平衡状态的是___________ (填字母)。
A.容器内混合气体的平均相对分子质量不再变化
B. 的值保持不变
的值保持不变
C.
D.容器内混合气体的密度不再变化
E. 和
和 的物质的量之比不变
的物质的量之比不变
(3)某温度下,在刚性密闭容器中充入 发生反应I,起始压强为
发生反应I,起始压强为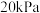 ,平衡时总压强为
,平衡时总压强为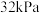 ,
, 平衡转化率为
平衡转化率为___________ ,该反应的平衡常数
___________  。
。
(4)一定压强下,向密闭容器中充入一定量的 和
和 ,发生反应
,发生反应
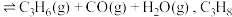 的平衡转化率在不同投料比
的平衡转化率在不同投料比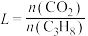 下与温度的关系如图1所示,该反应为反应
下与温度的关系如图1所示,该反应为反应___________ (填“吸热”或“放热”),投料比 由小到大的顺序为
由小到大的顺序为___________ 。

(5)反应II制备丙烯时还会生成 、
、 等副产物,在催化剂的作用下,
等副产物,在催化剂的作用下, 的转化率和
的转化率和 的产率随温度的变化关系如图2所示,在
的产率随温度的变化关系如图2所示,在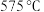 时,
时, 的选择性为
的选择性为___________ 。
( 的选择性
的选择性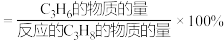 )。
)。
I.丙烷无氧脱氢法:

II.丙烷氧化脱氢法:
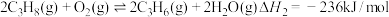
(1)已知
 ,由此计算
,由此计算
 ,该反应的正反应活化能
,该反应的正反应活化能 (正)
(正) (逆)(填“>”或“<”)。
(逆)(填“>”或“<”)。(2)一定温度下,在恒容密闭容器中充入
 发生反应I,下列能说明该反应达到平衡状态的是
发生反应I,下列能说明该反应达到平衡状态的是A.容器内混合气体的平均相对分子质量不再变化
B.
 的值保持不变
的值保持不变C.

D.容器内混合气体的密度不再变化
E.
 和
和 的物质的量之比不变
的物质的量之比不变(3)某温度下,在刚性密闭容器中充入
 发生反应I,起始压强为
发生反应I,起始压强为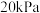 ,平衡时总压强为
,平衡时总压强为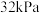 ,
, 平衡转化率为
平衡转化率为
 。
。(4)一定压强下,向密闭容器中充入一定量的
 和
和 ,发生反应
,发生反应
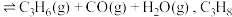 的平衡转化率在不同投料比
的平衡转化率在不同投料比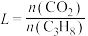 下与温度的关系如图1所示,该反应为反应
下与温度的关系如图1所示,该反应为反应 由小到大的顺序为
由小到大的顺序为
(5)反应II制备丙烯时还会生成
 、
、 等副产物,在催化剂的作用下,
等副产物,在催化剂的作用下, 的转化率和
的转化率和 的产率随温度的变化关系如图2所示,在
的产率随温度的变化关系如图2所示,在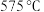 时,
时, 的选择性为
的选择性为(
 的选择性
的选择性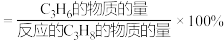 )。
)。
您最近一年使用:0次
3 . 常温下,在含有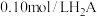 的溶液中,含
的溶液中,含 元素的微粒
元素的微粒 随
随 的变化关系如图所示。已知:
的变化关系如图所示。已知: ,下列说法错误的是
,下列说法错误的是

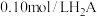 的溶液中,含
的溶液中,含 元素的微粒
元素的微粒 随
随 的变化关系如图所示。已知:
的变化关系如图所示。已知: ,下列说法错误的是
,下列说法错误的是
A.曲线③表示 |
B. 的 的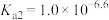 |
| C.NaHA溶液显碱性 |
D. 点对应的溶液中: 点对应的溶液中: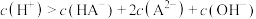 |
您最近一年使用:0次
解题方法
4 . 导电聚合物可用于军事上伪装隐身,还可以用于电磁屏蔽,由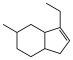 合成某导电高分子
合成某导电高分子 的路线如下:
的路线如下:

(1)写出A中所含官能团的名称
(2)比物质
 少2个
少2个 原子的一种化合物
原子的一种化合物
 ,其化学名称为
,其化学名称为 的反应类型是
的反应类型是(3)写出
 的化学反应方程式
的化学反应方程式(4)
 有多种同分异构体,其中属于芳香族化合物,苯环上有三个支链且支链中不含
有多种同分异构体,其中属于芳香族化合物,苯环上有三个支链且支链中不含 结构的同分异构体有
结构的同分异构体有(5)以
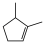 、乙醇为原料合成
、乙醇为原料合成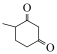 (其它试剂任选),设计其合成路线
(其它试剂任选),设计其合成路线
您最近一年使用:0次
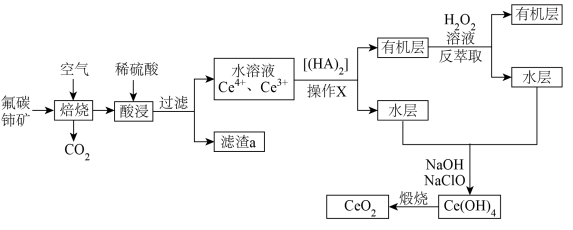
5 . 以氟碳铈矿(含 、
、 、
、 等)制备氧化铈
等)制备氧化铈 的流程如下:
的流程如下:
已知:在硫酸体系中, 在
在 中的溶解度大于其在水中的溶解度,
中的溶解度大于其在水中的溶解度, 与之相反。
与之相反。
(1)为提高酸浸效率通常采取的措施可以是将氟碳铈矿粉碎,还可以是___________ (任写一条)。
(2) 中
中 元素的化合价为
元素的化合价为___________ ;滤渣 的主要成分是
的主要成分是___________ 、___________ (填写化学式)。
(3)操作X需要的玻璃仪器有___________ 、___________ 。
(4)写出反萃取过程的离子方程式___________ 。
(5)常温下,向反萃取后的水层中先加入 调节
调节 使
使 完全沉淀,则调节
完全沉淀,则调节 应大于
应大于___________ (已知离子浓度小于 时,认为沉淀完全,
时,认为沉淀完全,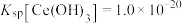 );再向产生的
);再向产生的 中加入
中加入 溶液,写出该反应的化学方程式
溶液,写出该反应的化学方程式___________ 。
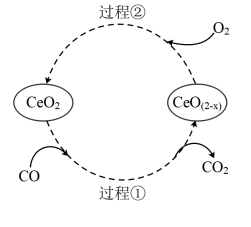
(6) 是汽车尾气净化催化剂中最重要的助剂,工作原理如图所示。写出过程①发生反应的化学方程式:
是汽车尾气净化催化剂中最重要的助剂,工作原理如图所示。写出过程①发生反应的化学方程式:___________ 。
 、
、 、
、 等)制备氧化铈
等)制备氧化铈 的流程如下:
的流程如下:
已知:在硫酸体系中,
 在
在 中的溶解度大于其在水中的溶解度,
中的溶解度大于其在水中的溶解度, 与之相反。
与之相反。(1)为提高酸浸效率通常采取的措施可以是将氟碳铈矿粉碎,还可以是
(2)
 中
中 元素的化合价为
元素的化合价为 的主要成分是
的主要成分是(3)操作X需要的玻璃仪器有
(4)写出反萃取过程的离子方程式
(5)常温下,向反萃取后的水层中先加入
 调节
调节 使
使 完全沉淀,则调节
完全沉淀,则调节 应大于
应大于 时,认为沉淀完全,
时,认为沉淀完全,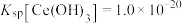 );再向产生的
);再向产生的 中加入
中加入 溶液,写出该反应的化学方程式
溶液,写出该反应的化学方程式(6)
 是汽车尾气净化催化剂中最重要的助剂,工作原理如图所示。写出过程①发生反应的化学方程式:
是汽车尾气净化催化剂中最重要的助剂,工作原理如图所示。写出过程①发生反应的化学方程式:
您最近一年使用:0次
6 . 碱式碳酸铜 俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:
俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:
Ⅰ.配制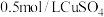 溶液和
溶液和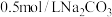 溶液各
溶液各 。
。
Ⅱ.取 所配
所配 溶液,按照
溶液,按照 和
和 的物质的量之比
的物质的量之比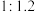 进行混合,在
进行混合,在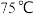 下搅拌反应产生蓝绿色沉淀。
下搅拌反应产生蓝绿色沉淀。
Ⅲ.待沉淀完全后减压过滤,用乙醇淋洗,干燥。
回答下列问题:
(1)步骤Ⅰ中,配制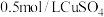 溶液时,不需要使用下列仪器中的
溶液时,不需要使用下列仪器中的___________ (填仪器名称)。___________ ,步骤Ⅲ中检验沉淀是否洗净的操作为___________ 。
(3)步骤Ⅲ中用乙醇淋洗的原因是___________ 。
Ⅳ.碱式碳酸铜纯度的测定:同学们设计了如图装置对制得的 蓝绿色固体进行实验。
蓝绿色固体进行实验。 装置加热前,需要首先打开活塞
装置加热前,需要首先打开活塞 ,用
,用 装置制取适量
装置制取适量 ,然后关闭
,然后关闭 ,点燃
,点燃 处酒精灯。装置A中发生反应的离子程式为
处酒精灯。装置A中发生反应的离子程式为___________ ,C中盛装的试剂应是___________ 。
(5)装置 的作用为
的作用为___________ 。
(6)待固体完全分解后,测得装置E增重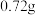 ,则该碱式碳酸铜的纯度为
,则该碱式碳酸铜的纯度为___________  (保留1位小数)。
(保留1位小数)。
 俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:
俗称铜绿,是一种不溶于水和乙醇的绿色固体,能用于催化剂、杀菌剂和电镀等行业。实验室制备碱式碳酸铜的步骤如下:Ⅰ.配制
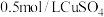 溶液和
溶液和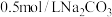 溶液各
溶液各 。
。Ⅱ.取
 所配
所配 溶液,按照
溶液,按照 和
和 的物质的量之比
的物质的量之比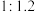 进行混合,在
进行混合,在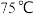 下搅拌反应产生蓝绿色沉淀。
下搅拌反应产生蓝绿色沉淀。Ⅲ.待沉淀完全后减压过滤,用乙醇淋洗,干燥。
回答下列问题:
(1)步骤Ⅰ中,配制
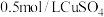 溶液时,不需要使用下列仪器中的
溶液时,不需要使用下列仪器中的
(3)步骤Ⅲ中用乙醇淋洗的原因是
Ⅳ.碱式碳酸铜纯度的测定:同学们设计了如图装置对制得的
 蓝绿色固体进行实验。
蓝绿色固体进行实验。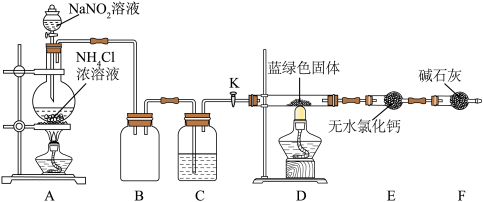
 装置加热前,需要首先打开活塞
装置加热前,需要首先打开活塞 ,用
,用 装置制取适量
装置制取适量 ,然后关闭
,然后关闭 ,点燃
,点燃 处酒精灯。装置A中发生反应的离子程式为
处酒精灯。装置A中发生反应的离子程式为(5)装置
 的作用为
的作用为(6)待固体完全分解后,测得装置E增重
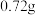 ,则该碱式碳酸铜的纯度为
,则该碱式碳酸铜的纯度为 (保留1位小数)。
(保留1位小数)。
您最近一年使用:0次
7 .  、
、 及其化合物在工业生产中起着重要的作用。回答下列问题:
及其化合物在工业生产中起着重要的作用。回答下列问题:
(1)基态氮原子的价电子排布式为___________ ,其最高能级的轨道形状为___________ (用文字描述)。
(2)比较键角大小:
___________  (填“>”或“<”);第一电离能用
(填“>”或“<”);第一电离能用 表示,已知
表示,已知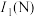 大于
大于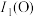 ,其原因是
,其原因是___________
(3)镍能形成多种配合物,其中常温下 是无色液体,
是无色液体,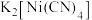 是红黄色晶体,熔融态下可以导电。
是红黄色晶体,熔融态下可以导电。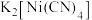 的熔点高于
的熔点高于 的原因是
的原因是___________ 。
(4)某有机物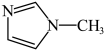 ,其环上所有原子共平面,则分子中
,其环上所有原子共平面,则分子中 原子的杂化方式为
原子的杂化方式为___________
(5) 的空间构型为
的空间构型为___________ (用文字描述)。
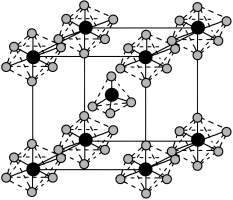
(6) 是一种离子化合物,为白色晶体,其晶胞如图所示。晶胞中含有由
是一种离子化合物,为白色晶体,其晶胞如图所示。晶胞中含有由 和
和 原子构成的一种正四面体形阳离子和一种正八面体形阴离子(黑色球:P,灰色球:Cl)。阳离子和阴离子中
原子构成的一种正四面体形阳离子和一种正八面体形阴离子(黑色球:P,灰色球:Cl)。阳离子和阴离子中 原子的配位数之比为
原子的配位数之比为___________ ,若晶胞参数为 ,则晶体的密度为
,则晶体的密度为___________  (列出计算式)。
(列出计算式)。
 、
、 及其化合物在工业生产中起着重要的作用。回答下列问题:
及其化合物在工业生产中起着重要的作用。回答下列问题:(1)基态氮原子的价电子排布式为
(2)比较键角大小:

 (填“>”或“<”);第一电离能用
(填“>”或“<”);第一电离能用 表示,已知
表示,已知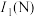 大于
大于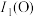 ,其原因是
,其原因是(3)镍能形成多种配合物,其中常温下
 是无色液体,
是无色液体,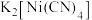 是红黄色晶体,熔融态下可以导电。
是红黄色晶体,熔融态下可以导电。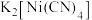 的熔点高于
的熔点高于 的原因是
的原因是(4)某有机物
 ,其环上所有原子共平面,则分子中
,其环上所有原子共平面,则分子中 原子的杂化方式为
原子的杂化方式为(5)
 的空间构型为
的空间构型为(6)
 是一种离子化合物,为白色晶体,其晶胞如图所示。晶胞中含有由
是一种离子化合物,为白色晶体,其晶胞如图所示。晶胞中含有由 和
和 原子构成的一种正四面体形阳离子和一种正八面体形阴离子(黑色球:P,灰色球:Cl)。阳离子和阴离子中
原子构成的一种正四面体形阳离子和一种正八面体形阴离子(黑色球:P,灰色球:Cl)。阳离子和阴离子中 原子的配位数之比为
原子的配位数之比为 ,则晶体的密度为
,则晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解题方法
8 . 某电化学装置如图所示,该装置能将 转化为燃料
转化为燃料 ,从而实现“碳中和”。下列说法正确的是
,从而实现“碳中和”。下列说法正确的是
 转化为燃料
转化为燃料 ,从而实现“碳中和”。下列说法正确的是
,从而实现“碳中和”。下列说法正确的是
A. 极接电源的负极 极接电源的负极 |
B. 极发生反应为: 极发生反应为: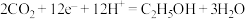 |
C.溶液中的 由 由 极区移向 极区移向 极区 极区 |
D.每转移 , , 极上产生气体 极上产生气体 (标准状况) (标准状况) |
您最近一年使用:0次
9 . 由实验操作和现象,可得出相应正确结论的是
| 实验操作 | 现象 | 结论 | |
| A | 向盛有饱和 溶液的试管中滴加稀盐酸 溶液的试管中滴加稀盐酸 | 溶液变浑浊且有气泡逸出 | 生成了 和 和 |
| B | 向 溶液中滴入适量饱和 溶液中滴入适量饱和 溶液,继续煮沸 溶液,继续煮沸 | 溶液中出现红褐色浑浊 | 生成了 胶体 胶体 |
| C | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 悬浊液,加热 悬浊液,加热 | 无砖红色沉淀 | 蔗糖未发生水解 |
| D | 把水滴入盛有少量 的试管中,立即把带火星木条放在试管口 的试管中,立即把带火星木条放在试管口 | 木条复燃 | 反应生成了 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 某阴离子由原子序数依次增大的同周期元素 、
、 、
、 、
、 组成,其结构如图,
组成,其结构如图, 的最外层电子数等于
的最外层电子数等于 的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
 、
、 、
、 、
、 组成,其结构如图,
组成,其结构如图, 的最外层电子数等于
的最外层电子数等于 的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是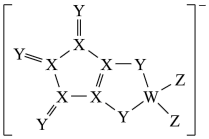
A.最高价含氧酸酸性: |
B. 、 、 的简单氢化物中 的简单氢化物中 的沸点高 的沸点高 |
C.原子半径: |
D.仅由 与 与 形成的化合物中可能含有非极性键 形成的化合物中可能含有非极性键 |
您最近一年使用:0次



