1 . 有机物M是新型苯二氮卓类镇静剂,其合成路线如下:
(1)G中所含官能团名称为___________ 。
(2)已知B的分子式为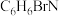 ,写出B的结构简式:
,写出B的结构简式:___________ ,其化学名称为___________ 。
(3)K的结构简式为___________ ,J→K的反应类型为___________ 。
(4)F+G→H分两步进行,第1步为加成反应,第2步为消去反应。写出第1步反应的化学方程式:___________ 。
(5)E的芳香族同分异构体中,符合下列条件的有种(不考虑立体异构体,不考虑 环状化合物)。
环状化合物)。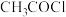 )、苯和甲胺(
)、苯和甲胺(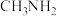 )为原料,设计制备
)为原料,设计制备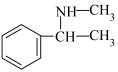 的合成路线:
的合成路线:___________ (其他无机试剂任选)。

(1)G中所含官能团名称为
(2)已知B的分子式为
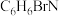 ,写出B的结构简式:
,写出B的结构简式:(3)K的结构简式为
(4)F+G→H分两步进行,第1步为加成反应,第2步为消去反应。写出第1步反应的化学方程式:
(5)E的芳香族同分异构体中,符合下列条件的有种(不考虑立体异构体,不考虑
 环状化合物)。
环状化合物)。①分子中含有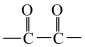 ;②核磁共振氢谱有四组峰。
;②核磁共振氢谱有四组峰。
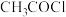 )、苯和甲胺(
)、苯和甲胺(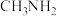 )为原料,设计制备
)为原料,设计制备 的合成路线:
的合成路线:
您最近一年使用:0次
2 . 铬酸铅[常温下,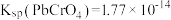 ]又称铬黄,常用于染料或颜料,某同学在实验室以
]又称铬黄,常用于染料或颜料,某同学在实验室以 为原料制备
为原料制备 ,实验步骤如下:
,实验步骤如下:
步骤1:称取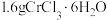 于
于 的烧杯中,加入
的烧杯中,加入 蒸馏水,搅拌使其溶解,逐滴滴入稍微过量的
蒸馏水,搅拌使其溶解,逐滴滴入稍微过量的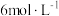 的
的 溶液;
溶液;
步骤2:向上述溶液中逐滴滴入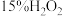 溶液,溶液由绿色变为黄色。加热煮沸
溶液,溶液由绿色变为黄色。加热煮沸 ,将多余的
,将多余的 赶尽,此时溶液变为亮黄色。再逐滴滴入
赶尽,此时溶液变为亮黄色。再逐滴滴入 的硝酸溶液,亮黄色溶液又变为橙红色,此时溶液的
的硝酸溶液,亮黄色溶液又变为橙红色,此时溶液的 为4.6;
为4.6;
步骤3:在煮沸条件下逐滴滴入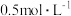 的
的 溶液,加入第一滴后先搅拌
溶液,加入第一滴后先搅拌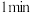 再加第2滴,每滴加一滴可以看到有黄色沉淀产生,滴加到不再有新的黄色沉淀产生时停止加入
再加第2滴,每滴加一滴可以看到有黄色沉淀产生,滴加到不再有新的黄色沉淀产生时停止加入 溶液。继续煮沸
溶液。继续煮沸 ,取下静置片刻,检验是否沉淀完全,过滤,产品用蒸馏水洗涤2~3次;
,取下静置片刻,检验是否沉淀完全,过滤,产品用蒸馏水洗涤2~3次;
步骤4:将沉淀放入烘箱中干燥、称重、计算产率。
已知:元素铬( )在溶液中主要以
)在溶液中主要以 (蓝紫色)、
(蓝紫色)、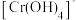 (绿色)、
(绿色)、 (橙红色)、
(橙红色)、 (黄色)等形式存在,
(黄色)等形式存在, 为难溶于水的灰蓝色固体。回答下列问题:
为难溶于水的灰蓝色固体。回答下列问题:
(1)实验室在配制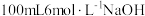 溶液时,下列仪器一定不需要的是___________(填字母)。
溶液时,下列仪器一定不需要的是___________(填字母)。
(2)步骤1中加入稍微过量的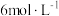 的
的 溶液过程中的现象是
溶液过程中的现象是___________ , 溶液不能过量太多,其原因是
溶液不能过量太多,其原因是___________ 。
(3)步骤2溶液中逐滴滴入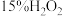 溶液,溶液由绿色变为黄色。发生反应的离子方程式为
溶液,溶液由绿色变为黄色。发生反应的离子方程式为___________ 。
(4)步骤2用硝酸调节 ,存在如下平衡:
,存在如下平衡: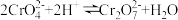 。已知
。已知 随
随 的变化如图所示。
的变化如图所示。 的平衡转化率
的平衡转化率___________ (填“增大”“减小”或“不变”)。
②升高温度,溶液中 的平衡转化率减小,则该反应的
的平衡转化率减小,则该反应的
___________ (填“>”或“<”)0。
(5)步骤3采用倾析法过滤,如图所示。下列关于该过滤方法的说法不正确的是___________(填字母)。
(6)对于步骤3,甲同学提出可用 代替
代替 作为原料,乙同学认为
作为原料,乙同学认为 难溶于水
难溶于水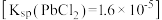 ,故设想不可能。甲同学进行实验,发现可以得到产品,但产量很低,其原因是
,故设想不可能。甲同学进行实验,发现可以得到产品,但产量很低,其原因是___________ 。
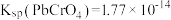 ]又称铬黄,常用于染料或颜料,某同学在实验室以
]又称铬黄,常用于染料或颜料,某同学在实验室以 为原料制备
为原料制备 ,实验步骤如下:
,实验步骤如下:步骤1:称取
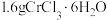 于
于 的烧杯中,加入
的烧杯中,加入 蒸馏水,搅拌使其溶解,逐滴滴入稍微过量的
蒸馏水,搅拌使其溶解,逐滴滴入稍微过量的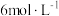 的
的 溶液;
溶液;步骤2:向上述溶液中逐滴滴入
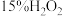 溶液,溶液由绿色变为黄色。加热煮沸
溶液,溶液由绿色变为黄色。加热煮沸 ,将多余的
,将多余的 赶尽,此时溶液变为亮黄色。再逐滴滴入
赶尽,此时溶液变为亮黄色。再逐滴滴入 的硝酸溶液,亮黄色溶液又变为橙红色,此时溶液的
的硝酸溶液,亮黄色溶液又变为橙红色,此时溶液的 为4.6;
为4.6;步骤3:在煮沸条件下逐滴滴入
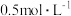 的
的 溶液,加入第一滴后先搅拌
溶液,加入第一滴后先搅拌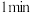 再加第2滴,每滴加一滴可以看到有黄色沉淀产生,滴加到不再有新的黄色沉淀产生时停止加入
再加第2滴,每滴加一滴可以看到有黄色沉淀产生,滴加到不再有新的黄色沉淀产生时停止加入 溶液。继续煮沸
溶液。继续煮沸 ,取下静置片刻,检验是否沉淀完全,过滤,产品用蒸馏水洗涤2~3次;
,取下静置片刻,检验是否沉淀完全,过滤,产品用蒸馏水洗涤2~3次;步骤4:将沉淀放入烘箱中干燥、称重、计算产率。
已知:元素铬(
 )在溶液中主要以
)在溶液中主要以 (蓝紫色)、
(蓝紫色)、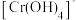 (绿色)、
(绿色)、 (橙红色)、
(橙红色)、 (黄色)等形式存在,
(黄色)等形式存在, 为难溶于水的灰蓝色固体。回答下列问题:
为难溶于水的灰蓝色固体。回答下列问题:(1)实验室在配制
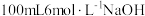 溶液时,下列仪器一定不需要的是___________(填字母)。
溶液时,下列仪器一定不需要的是___________(填字母)。A.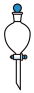 | B. | C.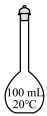 | D.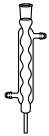 |
(2)步骤1中加入稍微过量的
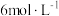 的
的 溶液过程中的现象是
溶液过程中的现象是 溶液不能过量太多,其原因是
溶液不能过量太多,其原因是(3)步骤2溶液中逐滴滴入
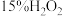 溶液,溶液由绿色变为黄色。发生反应的离子方程式为
溶液,溶液由绿色变为黄色。发生反应的离子方程式为(4)步骤2用硝酸调节
 ,存在如下平衡:
,存在如下平衡: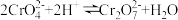 。已知
。已知 随
随 的变化如图所示。
的变化如图所示。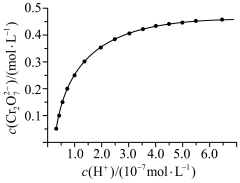
 的平衡转化率
的平衡转化率②升高温度,溶液中
 的平衡转化率减小,则该反应的
的平衡转化率减小,则该反应的
(5)步骤3采用倾析法过滤,如图所示。下列关于该过滤方法的说法不正确的是___________(填字母)。
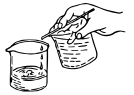
| A.该方法适用于过滤胶状沉淀或颗粒较小的沉淀 |
| B.使用该方法过滤后,若沉淀物要洗涤,可注入水(或其他洗涤液),充分搅拌后使沉淀沉降,再进行过滤 |
| C.这种过滤方法可以避免沉淀堵塞滤纸小孔而影响过滤速度 |
| D.该操作中玻璃棒的作用为引流 |
(6)对于步骤3,甲同学提出可用
 代替
代替 作为原料,乙同学认为
作为原料,乙同学认为 难溶于水
难溶于水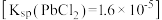 ,故设想不可能。甲同学进行实验,发现可以得到产品,但产量很低,其原因是
,故设想不可能。甲同学进行实验,发现可以得到产品,但产量很低,其原因是
您最近一年使用:0次
3 . 室温下,用 的二甲胺
的二甲胺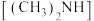 溶液(二甲胺在水中的电离与一水合氨相似)滴定
溶液(二甲胺在水中的电离与一水合氨相似)滴定 盐酸溶液。溶液
盐酸溶液。溶液 随加入二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
随加入二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
 的二甲胺
的二甲胺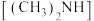 溶液(二甲胺在水中的电离与一水合氨相似)滴定
溶液(二甲胺在水中的电离与一水合氨相似)滴定 盐酸溶液。溶液
盐酸溶液。溶液 随加入二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
随加入二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是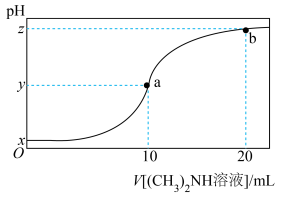
| A.x=1,y=7 |
B.a、b两点的溶液中, 不相等 不相等 |
| C.本实验应该选择酚酞作指示剂 |
D.b点溶液中存在: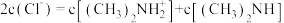 |
您最近一年使用:0次
解题方法
4 . 硼(B)、钴( )和锰(
)和锰( )形成的物质在生产、生活中应用广泛。回答下列问题:
)形成的物质在生产、生活中应用广泛。回答下列问题:
(1)基态 原子核外电子排布式为
原子核外电子排布式为___________ ,在第二周期中,第一电离能比N高的元素是___________ (填元素符号)。
(2)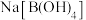 可用于织物漂白。
可用于织物漂白。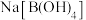 的化学键除了共价键外,还存在
的化学键除了共价键外,还存在___________ 。
(3)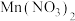 工业制备中常用的催化剂,
工业制备中常用的催化剂,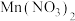 中阴离子的空间构型为
中阴离子的空间构型为___________ ;写出一种与其互为等电子体的分子式:___________ 。
(4)如图1表示偏硼酸根的一种无限长的链式结构,其化学式可表示为___________ (以n表示硼原子的个数);___________ 。
(5)立方 和立方
和立方 均为共价晶体,结构相似,
均为共价晶体,结构相似, 的熔点高于
的熔点高于 的原因是
的原因是___________ 。
(6)一种新型轻质储氢材料的晶胞结构如图所示,设阿伏加德罗常数的值为 ,该晶体的密度为
,该晶体的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
 )和锰(
)和锰( )形成的物质在生产、生活中应用广泛。回答下列问题:
)形成的物质在生产、生活中应用广泛。回答下列问题:(1)基态
 原子核外电子排布式为
原子核外电子排布式为(2)
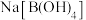 可用于织物漂白。
可用于织物漂白。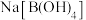 的化学键除了共价键外,还存在
的化学键除了共价键外,还存在(3)
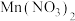 工业制备中常用的催化剂,
工业制备中常用的催化剂,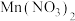 中阴离子的空间构型为
中阴离子的空间构型为(4)如图1表示偏硼酸根的一种无限长的链式结构,其化学式可表示为
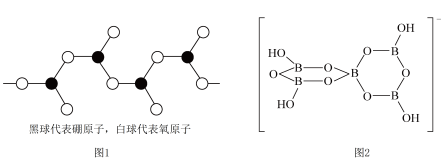
(5)立方
 和立方
和立方 均为共价晶体,结构相似,
均为共价晶体,结构相似, 的熔点高于
的熔点高于 的原因是
的原因是(6)一种新型轻质储氢材料的晶胞结构如图所示,设阿伏加德罗常数的值为
 ,该晶体的密度为
,该晶体的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
5 . 铁及其化合物在化工生产中发挥着重要作用。回答下列问题:
(1)一定温度下,在某密闭无氧环境中热分解 ,反应的热化学方程式为
,反应的热化学方程式为 。反应生成的混合气体中
。反应生成的混合气体中 的物质的量分数为
的物质的量分数为___________ 。反应达平衡后,缩小容器体积,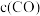
___________ (填“增大”“减小”或“不变”)。
(2)将 置入抽空的刚性容器中,升高温度,发生分解反应:
置入抽空的刚性容器中,升高温度,发生分解反应: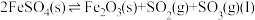 。平衡时
。平衡时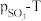 的关系如图所示。
的关系如图所示。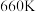 时,该反应的平衡总压
时,该反应的平衡总压
___________  ,压强平衡常数
,压强平衡常数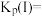
___________ 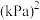 (压强平衡常数是用分压代表平衡浓度,分压=总压×物质的量分数)。
(压强平衡常数是用分压代表平衡浓度,分压=总压×物质的量分数)。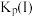 随反应温度升高而
随反应温度升高而___________ (填“增大”“减小”或“不变”)。 可用作脱除
可用作脱除 气体的脱硫剂。
气体的脱硫剂。 首先与表面的
首先与表面的 产生疏松多孔的产物
产生疏松多孔的产物 ,随着反应的进行,Fe2O3不断减少,产物层不断加厚,如图所示。失效的脱硫剂可在氧气中加热重新转化为Fe2O3实现“再生”。
,随着反应的进行,Fe2O3不断减少,产物层不断加厚,如图所示。失效的脱硫剂可在氧气中加热重新转化为Fe2O3实现“再生”。 “再生”时转化为Fe2O3的化学方程式:
“再生”时转化为Fe2O3的化学方程式:___________ 。
②“再生”时若 浓度过大、反应温度过高,“再生”后的脱硫剂脱硫效果明显变差的原因可能是
浓度过大、反应温度过高,“再生”后的脱硫剂脱硫效果明显变差的原因可能是___________ 。
(1)一定温度下,在某密闭无氧环境中热分解
 ,反应的热化学方程式为
,反应的热化学方程式为 。反应生成的混合气体中
。反应生成的混合气体中 的物质的量分数为
的物质的量分数为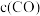
(2)将
 置入抽空的刚性容器中,升高温度,发生分解反应:
置入抽空的刚性容器中,升高温度,发生分解反应: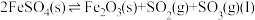 。平衡时
。平衡时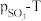 的关系如图所示。
的关系如图所示。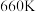 时,该反应的平衡总压
时,该反应的平衡总压
 ,压强平衡常数
,压强平衡常数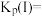
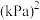 (压强平衡常数是用分压代表平衡浓度,分压=总压×物质的量分数)。
(压强平衡常数是用分压代表平衡浓度,分压=总压×物质的量分数)。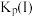 随反应温度升高而
随反应温度升高而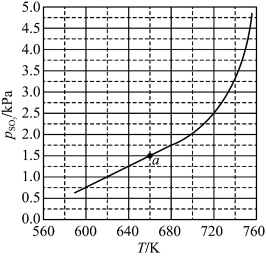
 可用作脱除
可用作脱除 气体的脱硫剂。
气体的脱硫剂。 首先与表面的
首先与表面的 产生疏松多孔的产物
产生疏松多孔的产物 ,随着反应的进行,Fe2O3不断减少,产物层不断加厚,如图所示。失效的脱硫剂可在氧气中加热重新转化为Fe2O3实现“再生”。
,随着反应的进行,Fe2O3不断减少,产物层不断加厚,如图所示。失效的脱硫剂可在氧气中加热重新转化为Fe2O3实现“再生”。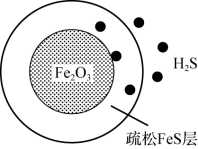
 “再生”时转化为Fe2O3的化学方程式:
“再生”时转化为Fe2O3的化学方程式:②“再生”时若
 浓度过大、反应温度过高,“再生”后的脱硫剂脱硫效果明显变差的原因可能是
浓度过大、反应温度过高,“再生”后的脱硫剂脱硫效果明显变差的原因可能是
您最近一年使用:0次
6 . 电镀在工业生产中具有重要作用,某电镀厂生产的废水经预处理后含有 和少量的
和少量的 、
、 ,能够采用如图流程进行逐一分离,实现资源再利用。
,能够采用如图流程进行逐一分离,实现资源再利用。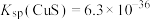 和
和 。
。
回答下列问题:
(1) 中Cr元素的化合价为
中Cr元素的化合价为___________ 。
(2)还原池中有 生成,反应的离子方程式为
生成,反应的离子方程式为___________ 。
(3)沉淀1为 ,其性质与
,其性质与 相似,则
相似,则 与NaOH溶液反应的化学方程式
与NaOH溶液反应的化学方程式___________ 。
(4) 溶液呈碱性的原因是
溶液呈碱性的原因是___________ (用离子方程式表示),沉淀2为___________ 。
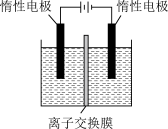
(5)利用膜电解技术(装置如图所示),以 为主要原料制备
为主要原料制备 的总反应方程式为:
的总反应方程式为: 。
。___________ (填“阴”或“阳”,下同)离子交换膜, 在
在___________ (填“阴”或“阳”)极室制得。
 和少量的
和少量的 、
、 ,能够采用如图流程进行逐一分离,实现资源再利用。
,能够采用如图流程进行逐一分离,实现资源再利用。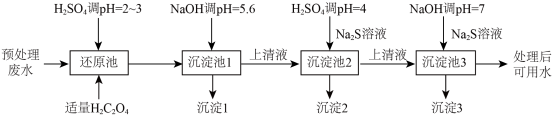
 和
和 。
。回答下列问题:
(1)
 中Cr元素的化合价为
中Cr元素的化合价为(2)还原池中有
 生成,反应的离子方程式为
生成,反应的离子方程式为(3)沉淀1为
 ,其性质与
,其性质与 相似,则
相似,则 与NaOH溶液反应的化学方程式
与NaOH溶液反应的化学方程式(4)
 溶液呈碱性的原因是
溶液呈碱性的原因是(5)利用膜电解技术(装置如图所示),以
 为主要原料制备
为主要原料制备 的总反应方程式为:
的总反应方程式为: 。
。
 在
在
您最近一年使用:0次
7 . 手性甲脒四氢异喹啉( )是D-荷态牡丹碱全合成的重要原料。其合成路线如下:
)是D-荷态牡丹碱全合成的重要原料。其合成路线如下:
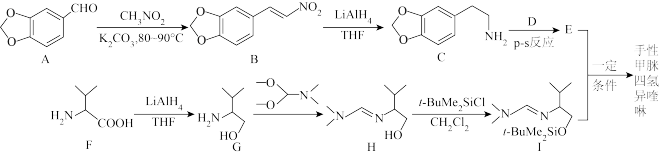
已知: 反应为
反应为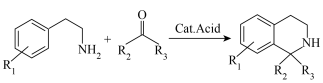 。
。
(1)等浓度的F和G的水溶液的碱性:F比G
(2)A与
 反应生成B经历了如下反应过程:A→X→B,X的分子式为
反应生成B经历了如下反应过程:A→X→B,X的分子式为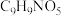 ,则X→B的反应类型为
,则X→B的反应类型为(3)E的结构简式为
(4)G→H的另一种有机产物的结构简式为
(5)写出同时满足下列条件的C的一种同分异构体的结构简式:
①能发生银镜反应和水解反应,且水解产物之一遇
 溶液能发生显色反应;
溶液能发生显色反应;②含有4种等效氢原子。
(6)已知:

 ,写出以
,写出以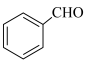 和
和 为原料制备
为原料制备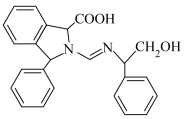 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
8 . W、X、Y、Z是原子序数依次增大的短周期主族元素。已知W原子的最外层电子数是电子层数的2倍,X元素存在两种气态同素异形体,其中一种可吸收大气中的紫外线,Y原子最外层电子数等于电子层数,Z离子在同周期稳定的最简单阴离子中,半径最小。下列说法正确的是
A.简单离子半径: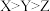 |
B. 可用于污水的杀菌消毒 可用于污水的杀菌消毒 |
| C.X的氢化物常温常压下处于气态 |
D.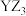 的水溶液能导电,故 的水溶液能导电,故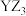 为离子化合物 为离子化合物 |
您最近一年使用:0次
9 . 下列实验中,由实验现象得出的结论正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向 溶液中通入足量的 溶液中通入足量的 | 生成淡黄色沉淀 |  不溶于盐酸 不溶于盐酸 |
| B | 少量 粉加到 粉加到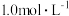 的 的 溶液中 溶液中 | 溶液颜色变浅 | 金属 比Fe活泼 比Fe活泼 |
| C | 向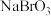 溶液中滴入1滴新制氯水 溶液中滴入1滴新制氯水 | 溶液变橙色 | 氧化性: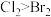 |
| D | 向浓度均为 的 的 和 和 混合溶液中滴加少量 混合溶液中滴加少量 溶液 溶液 | 仅出现浅蓝色沉淀 |  的溶度积比 的溶度积比 的小 的小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 已知反应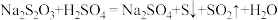 ,
, 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
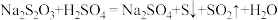 ,
, 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.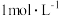 的 的 溶液中含有 溶液中含有 数目为 数目为 |
B.该反应中每生成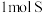 转移电子数为 转移电子数为 |
C.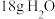 中含有孤电子对数目为 中含有孤电子对数目为 |
D.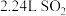 中含有的电子总数为 中含有的电子总数为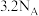 |
您最近一年使用:0次



