解题方法
1 . 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:
(1)将大小相同的钠、镁、铝(除去氧化膜)分别投入到冷水中,反应最剧烈的是___________ ;分别向新制取的 沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明
沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明 是
是___________ 氢氧化物,其中 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为___________ 。
(2)利用如图装置验证碳、硅、硫三种元素的非金属性强弱。
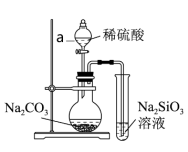
①图中仪器a的名称是___________ ,圆底烧瓶中发生反应的离子方程式为___________ 。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是___________ ,该实验能证明非金属性强弱,依据的原理是___________ 。
(1)将大小相同的钠、镁、铝(除去氧化膜)分别投入到冷水中,反应最剧烈的是
 沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明
沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明 是
是 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为(2)利用如图装置验证碳、硅、硫三种元素的非金属性强弱。

①图中仪器a的名称是
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是
您最近半年使用:0次
名校
解题方法
2 . 下列设计的实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 探究化学反应的限度 | 取5mL0.1 mol·L-1 KI溶液,滴加0.1 mol·L-1 FeCl3溶液5~6滴,充分反应后,再滴加淀粉溶液 |
| B | 比较Mg与Al的金属性强弱 | 常温下,将Mg、Al与NaOH溶液组成原电池 |
| C | 比较Cl2、Br2、I2的氧化性强弱 | 向NaBr溶液中滴加少量氯水,充分反应后,再加入淀粉KI溶液 |
| D | 检验某溶液中是否含有K+ | 用洁净的铂丝蘸取待测液,在酒精灯火焰上灼烧 直接观察火焰的颜色 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
3 . W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。Y的最外层电子数与其K层电子数相等,WX2是形成酸雨的物质之一,下列说法正确的是
| A.原子半径:X>W | B.Z的含氧酸是强酸 |
| C.YX对应的水化物具有两性 | D.原子的得电子能力:X>Z |
您最近半年使用:0次
名校
4 . 下列事实不能说明元素的金属性或非金属性相对强弱的是
| 选项 | 事实 | 推论 |
| A | 与冷水反应,K比Mg剧烈 | 金属性:K>Mg |
| B |  的碱性强于 的碱性强于 | 金属性:Ca>Mg |
| C | SO2与 溶液反应生成 溶液反应生成 | 非金属性:S>C |
| D | 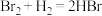 、 、 | 非金属性:Br>I |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
5 . 下表是元素周期表的一部分。请按要求回答下列问题:___________ ,⑦的最高价氧化物对应水化物的化学式___________ 。
(2)上述所列元素最高价氧化物对应水化物碱性最强的是___________ (填化学式)。
(3)写出由上述所列元素形成的18电子的双原子分子的化学式___________ 。
(4)下列说法不正确的是___________。
(5)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式___________ 。
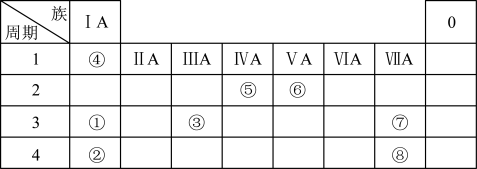
(2)上述所列元素最高价氧化物对应水化物碱性最强的是
(3)写出由上述所列元素形成的18电子的双原子分子的化学式
(4)下列说法不正确的是___________。
| A.⑥形成的最简单氢化物比⑤形成的最简单氢化物的稳定性高 |
| B.元素最高正价与最低负价绝对值相等的元素一定处于第ⅣA族 |
| C.第5周期第ⅦA族元素的原子序数为53 |
| D.周期表中当某元素的周期序数大于其主族序数时,该元素可能属于金属或非金属 |
(5)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式
您最近半年使用:0次
名校
6 . 化学与生活、科技、社会发展息息相关。下列说法正确的是
A.碳纳米材料中,碳纳米管和 互为同位素 互为同位素 |
| B.用于火箭发动机的碳化硅陶瓷是一种新型无机非金属材料 |
C.华为新上市手机的芯片材料是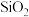 |
D.“北斗卫星”授时系统的“星载铷钟”含铷元素,其单质遇水能极其缓慢地反应放出 |
您最近半年使用:0次
7 . X、Y、Z、M和W五种短周期主族元素,原子序数依次增大,X元素最高化合价=|最低化合价|,Y在周期表中电负性最大,W与M、X相邻,基态Z的价电子层上只有1个电子,下列说法不正确的是
| A.单核离子半径:M<Z<Y |
| B.W与O原子可形成以平面三角形为结构单元的长链阴离子 |
| C.简单气态氢化物的沸点:Y>W>X |
| D.最高价氧化物中离子键成分百分数:Z>M>X |
您最近半年使用:0次
7日内更新
|
177次组卷
|
2卷引用:浙江省金华市十校2023-2024学年高三下学期4月模拟考试化学试题
名校
解题方法
8 . 铝及其合金是金属材料界后起之秀。铝的冶炼历史较短,这是由于炼铝原料Al2O3的熔点较高的缘故,直到人们找到助熔剂冰晶石(Na3AlF6) 才实现了Al2O3在较低温度下的熔融电离。据此判断:Al2O3属于
才实现了Al2O3在较低温度下的熔融电离。据此判断:Al2O3属于___________ (选填“离子”或“共价”)化合物。列举一个事实证明并判断:组成冰晶石的两种金属元素,它们金属性的相对强弱___________ 。
 才实现了Al2O3在较低温度下的熔融电离。据此判断:Al2O3属于
才实现了Al2O3在较低温度下的熔融电离。据此判断:Al2O3属于
您最近半年使用:0次
9 . 在1~18号元素中,除稀有气体元素外,回答下列问题(用元素符号或化学式回答):
(1)原子半径最大的元素是___________ 。
(2)非金属性最强的元素是___________ 。
(3)金属性最强的元素是___________ 。
(4)最高价氧化物对应水化物碱性最强的碱的化学式为___________ 。
(5)最高价氧化物对应水化物酸性最强的酸是___________ 。
(6)气态氢化物中最稳定的是___________ 。
(1)原子半径最大的元素是
(2)非金属性最强的元素是
(3)金属性最强的元素是
(4)最高价氧化物对应水化物碱性最强的碱的化学式为
(5)最高价氧化物对应水化物酸性最强的酸是
(6)气态氢化物中最稳定的是
您最近半年使用:0次
名校
10 . 分析与推测能力是学习化学的必备能力之一,下列推测合理的是
A.非金属性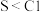 ,可以推测酸性 ,可以推测酸性 |
B.最外层电子数: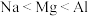 ,可以推测失电子能力: ,可以推测失电子能力: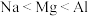 |
C.Cs和Ba分别位于第六周期ⅠA族和ⅡA族,可以推测碱性: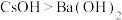 |
D.已知元素铊(Tl)是与铝(Al)同主族的第六周期元素,可以推测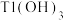 具有两性 具有两性 |
您最近半年使用:0次



