2024·上海·模拟预测
1 . 钯催化剂(主要成分为Pd、α-Al2O3,还含少量铁、铜等)是石油化工中催化加氢和催化氧化等反应的重要催化剂。一种从废钯催化剂中回收海绵钯的工艺流程如下:
②常温下,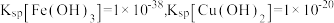 。
。
回答下列问题:
(1)“还原Ⅰ”过程中加入甲酸的主要目的是还原___________ (填化学式)。
(2)“酸浸”过程中Pd转化的离子方程式为___________ 。
(3)“酸浸”过程中温度、固液比对浸取率的影响如图,则“酸浸”最佳条件为___________ 。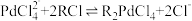 ,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是
,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是___________ 。
(5)“沉钯”过程钯元素主要发生如下转化:H2PdCl4 (稀溶液) [Pd(NH3)4]Cl2 (稀溶液)
[Pd(NH3)4]Cl2 (稀溶液) [Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为
[Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为___________ (填化学式)。
(6)N2H4的电子式为___________ 。
(7)“还原Ⅱ”过程中产生无毒无害气体。由[Pd(NH3)2]Cl2生成海绵钯的化学方程式为___________ 。
(8)H2和O2在钯的配合物离子[PdCl4]2-的作用下合成H2O2,反应历程如图。下列说法不正确的是 。
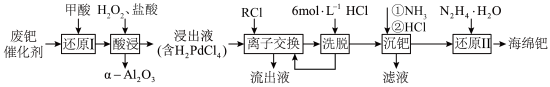
②常温下,
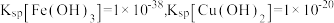 。
。回答下列问题:
(1)“还原Ⅰ”过程中加入甲酸的主要目的是还原
(2)“酸浸”过程中Pd转化的离子方程式为
(3)“酸浸”过程中温度、固液比对浸取率的影响如图,则“酸浸”最佳条件为

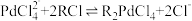 ,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是
,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是(5)“沉钯”过程钯元素主要发生如下转化:H2PdCl4 (稀溶液)
 [Pd(NH3)4]Cl2 (稀溶液)
[Pd(NH3)4]Cl2 (稀溶液) [Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为
[Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为(6)N2H4的电子式为
(7)“还原Ⅱ”过程中产生无毒无害气体。由[Pd(NH3)2]Cl2生成海绵钯的化学方程式为
(8)H2和O2在钯的配合物离子[PdCl4]2-的作用下合成H2O2,反应历程如图。下列说法不正确的是 。

| A.H2O2中存在极性键和非极性键 |
| B.[PdCl4]2-中Pd2+提供空轨道形成配位键 |
| C.反应①、②、③均属于氧化还原反应 |
| D.等物质的量的H2和O2发生反应时,反应①和反应②转移的电子数之比为1:1 |
您最近一年使用:0次
2024·上海·模拟预测
2 . 某研究组模拟三种已装固体V2O5催化剂的密闭容器装置,发生的反应为:2SO2(g)+O2(g) 2SO3(g) ΔH1=-197.7kJ·mol-1
2SO3(g) ΔH1=-197.7kJ·mol-1
(1)在初始体积与温度相同的条件下,甲、乙、丙中均按2molSO2、1molO2投料,达平衡时;三个容器中SO2的转化率从大到小的顺序为___________ (用“甲、乙、丙”表示)。
(3)400℃,在容器丙中投入4molSO2、2molO2进行反应时,放出akJ热量;若在500℃,投入2molSO2、1molO2进行反应,放出bkJ热量,则a___________ 2b(填“﹥”、“﹤”或“=”)。
 2SO3(g) ΔH1=-197.7kJ·mol-1
2SO3(g) ΔH1=-197.7kJ·mol-1(1)在初始体积与温度相同的条件下,甲、乙、丙中均按2molSO2、1molO2投料,达平衡时;三个容器中SO2的转化率从大到小的顺序为
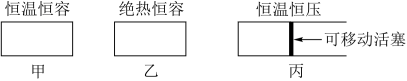
| A.温度不变 | B.密度保持不变 | C.压强保持不变 | D.O2浓度保持不变 |
(3)400℃,在容器丙中投入4molSO2、2molO2进行反应时,放出akJ热量;若在500℃,投入2molSO2、1molO2进行反应,放出bkJ热量,则a
您最近一年使用:0次
2024·上海·模拟预测
3 . 铋酸钠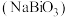 是一种强氧化剂,在钢铁工业中常用作锰元素的分析测定。某实验小组在实验室用氯气将
是一种强氧化剂,在钢铁工业中常用作锰元素的分析测定。某实验小组在实验室用氯气将 (白色,难溶于水)氧化制取
(白色,难溶于水)氧化制取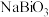 (淡黄色,难溶于水),并探究其性质。各实验装置如下图所示:
(淡黄色,难溶于水),并探究其性质。各实验装置如下图所示:
(1)装置的连接顺序是: ___________(填装置标号和“→”)。
___________(填装置标号和“→”)。
(2)室温下,装置 中的
中的 晶体不能用
晶体不能用 粉末代替,原因是
粉末代替,原因是___________ 。装置 的作用是
的作用是___________ 。
(3)B中发生反应的离子方程式为___________ 。
(4)判断B中反应已经完成的实验现象是___________ 。
(5)B中反应结束时,关闭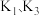 ,打开
,打开 。这样操作的目的是
。这样操作的目的是___________ 。
(6)将铋酸钠固体加到足量的浓盐酸中,观察到淡黄色固体溶解,并有黄绿色气体产生,该实验现象说明氧化性: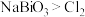 ;但从
;但从 中的反应来看,氧化性:
中的反应来看,氧化性: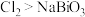 。原因是
。原因是___________ 。
(7)为测定产品的纯度。取上述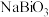 产品
产品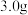 ,用足量稀硫酸和
,用足量稀硫酸和 稀溶液使其还原为
稀溶液使其还原为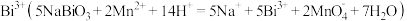 ,再将其准确配制成
,再将其准确配制成 溶液,取出
溶液,取出 溶液,用
溶液,用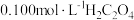 标准溶液滴定生成的
标准溶液滴定生成的 ,滴定终点时消耗
,滴定终点时消耗 标准溶液
标准溶液 ,则该产品的纯度为
,则该产品的纯度为___________  (保留1位小数)。
(保留1位小数)。
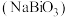 是一种强氧化剂,在钢铁工业中常用作锰元素的分析测定。某实验小组在实验室用氯气将
是一种强氧化剂,在钢铁工业中常用作锰元素的分析测定。某实验小组在实验室用氯气将 (白色,难溶于水)氧化制取
(白色,难溶于水)氧化制取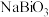 (淡黄色,难溶于水),并探究其性质。各实验装置如下图所示:
(淡黄色,难溶于水),并探究其性质。各实验装置如下图所示: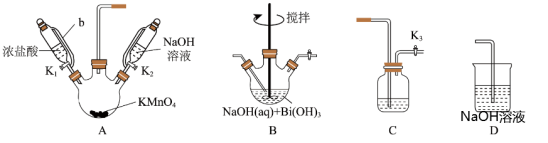
(1)装置的连接顺序是:
 ___________(填装置标号和“→”)。
___________(填装置标号和“→”)。A.C B B D D | B.B C C D D | C.C D D B B | D.B D D C C |
(2)室温下,装置
 中的
中的 晶体不能用
晶体不能用 粉末代替,原因是
粉末代替,原因是 的作用是
的作用是(3)B中发生反应的离子方程式为
(4)判断B中反应已经完成的实验现象是
(5)B中反应结束时,关闭
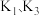 ,打开
,打开 。这样操作的目的是
。这样操作的目的是(6)将铋酸钠固体加到足量的浓盐酸中,观察到淡黄色固体溶解,并有黄绿色气体产生,该实验现象说明氧化性:
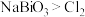 ;但从
;但从 中的反应来看,氧化性:
中的反应来看,氧化性: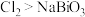 。原因是
。原因是(7)为测定产品的纯度。取上述
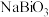 产品
产品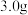 ,用足量稀硫酸和
,用足量稀硫酸和 稀溶液使其还原为
稀溶液使其还原为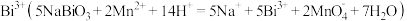 ,再将其准确配制成
,再将其准确配制成 溶液,取出
溶液,取出 溶液,用
溶液,用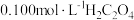 标准溶液滴定生成的
标准溶液滴定生成的 ,滴定终点时消耗
,滴定终点时消耗 标准溶液
标准溶液 ,则该产品的纯度为
,则该产品的纯度为 (保留1位小数)。
(保留1位小数)。
您最近一年使用:0次
2024·上海·模拟预测
4 .  与环氧丙烷(
与环氧丙烷( )在一定条件下反应制得碳酸丙烯酯。
)在一定条件下反应制得碳酸丙烯酯。
 是
是(2)环氧丙烷中,O原子的杂化轨道类型是
(3)沸点:环氧丙烷
 (填“>”或“<”),解释其原因:
(填“>”或“<”),解释其原因:
您最近一年使用:0次
名校
解题方法
5 .  和
和 是硫元素的重要氧化物,下列说法中正确的是
是硫元素的重要氧化物,下列说法中正确的是
 和
和 是硫元素的重要氧化物,下列说法中正确的是
是硫元素的重要氧化物,下列说法中正确的是A. 和 和 中S原子杂化方式均为 中S原子杂化方式均为 |
B. 和 和 中S原子杂化方式不同,前者为 中S原子杂化方式不同,前者为 ,后者为 ,后者为 |
C. 的VSFPR模型为平面三角形,键角为120° 的VSFPR模型为平面三角形,键角为120° |
D. 的VSEPR模型为角形,键角小于120° 的VSEPR模型为角形,键角小于120° |
您最近一年使用:0次
名校
解题方法
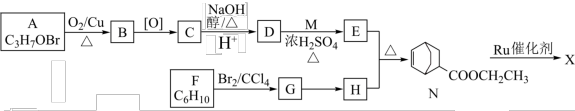
6 . 利喘贝是一种新的平喘药,其合成过程如图: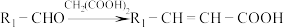
1.B的名称为___________ 。E的官能团的名称为___________ 。
2.反应①所需试剂为___________ 。D→E的反应类型为___________ 。
3.H苯环上的一氯代物有两种,能发生银镜反应,也能与氯化铁溶液发生显色反应。由H生成I反应的化学方程式为___________ 。
4.L的结构简式为___________ 。
5.在J的同分异构体中,同时满足下列条件的结构简式为___________ 。
①含有一个苹环
②能与NaHCO3反应
③遇FeCl3显示紫色
④核磁共振氢谱显示有五组峰,峰面积之比为1:1:2:2:2
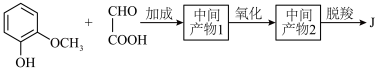
6.J俗称香兰素,在食品行业中主要作为—种增香剂。香兰素的一种合成路线如下。___________ ;___________ 。

已知:i.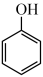
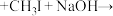

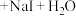
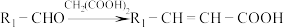
1.B的名称为
2.反应①所需试剂为
3.H苯环上的一氯代物有两种,能发生银镜反应,也能与氯化铁溶液发生显色反应。由H生成I反应的化学方程式为
4.L的结构简式为
5.在J的同分异构体中,同时满足下列条件的结构简式为
①含有一个苹环
②能与NaHCO3反应
③遇FeCl3显示紫色
④核磁共振氢谱显示有五组峰,峰面积之比为1:1:2:2:2
6.J俗称香兰素,在食品行业中主要作为—种增香剂。香兰素的一种合成路线如下。
您最近一年使用:0次
名校
7 . 聚合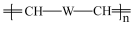 (W是链接中的部分结构)是一类重要的功能高分子材料,功能高分子聚合物X的转化路线如下
(W是链接中的部分结构)是一类重要的功能高分子材料,功能高分子聚合物X的转化路线如下
②
 (R表示烃基或氢原子)。
(R表示烃基或氢原子)。(1)B所含的官能团名称是
(2)E的名称是
(3)写出D生成E的化学方程式是
(4)下列关于N的说法中错误的是_______。
A.N的分子式为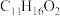 |
| B.N分子中有4个手性碳原子 |
| C.N可以和NaOH溶液发生反应 |
| D.N可以发生加聚反应 |
(5)X的结构简式
(6)E存在多种同分异构体,与E具有相同官能团且不能发生银镜反应的同分异构体有
(7)以
 为原料(无机试剂任选)合成环丁烯,试写出合成流程图
为原料(无机试剂任选)合成环丁烯,试写出合成流程图
您最近一年使用:0次
名校
8 . 炼油、石化等工业会产生含硫(-2价)废水,处理的方法有沉淀法、氧化法。
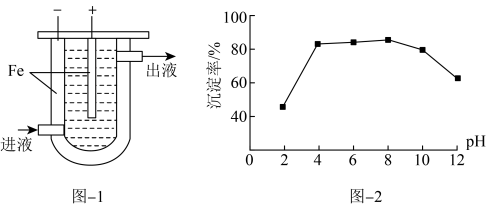
Ⅰ.沉淀法。用如下图-1装置可以将废水中的硫转化为FeS沉淀。控制其他条件一定,测得出口处硫转化为FeS的沉淀率与溶液pH的关系如题图-2所示。
(2)该装置沉淀废水中的硫(-2价)的原理可描述为_______ 。
(3) 时,pH越大,硫转化为FeS的沉淀率越低,可能的原因是_______。
时,pH越大,硫转化为FeS的沉淀率越低,可能的原因是_______。
Ⅱ.氧化法。 氧化法、
氧化法、 氧化法、催化氧化法等可以将含硫废水中硫元素氧化。
氧化法、催化氧化法等可以将含硫废水中硫元素氧化。
i. 氧化法:向含
氧化法:向含 的废水中,加入一定量的
的废水中,加入一定量的 溶液,控制溶液的pH为5,可以生成S沉淀。
溶液,控制溶液的pH为5,可以生成S沉淀。
(4)写出该反应的离子方程式:_______ 。
ii. 氧化法:向含
氧化法:向含 的废水中,加入
的废水中,加入 溶液,其他条件一定,测得硫(-2价)的去除率、S(单质)的生成率与所加
溶液,其他条件一定,测得硫(-2价)的去除率、S(单质)的生成率与所加 溶液体积的关系如题图-3所示。
溶液体积的关系如题图-3所示。
(6)当所加 溶液体积大于9mL时,所加
溶液体积大于9mL时,所加 溶液越多,S生成率越低,原因是
溶液越多,S生成率越低,原因是____ 。
iii.催化氧化法: 苯胺(
苯胺( 为催化剂、聚苯胺为催化剂载体)可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如题图-4所示。
为催化剂、聚苯胺为催化剂载体)可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如题图-4所示。_______ 。
(8)催化剂使用一段时间后催化效率会下降,结合图中相关信息,分析可能原因为_______ ,要使催化剂恢复催化效率,处理的方法是用氯仿( )浸取催化剂,再干燥即可。
)浸取催化剂,再干燥即可。
Ⅰ.沉淀法。用如下图-1装置可以将废水中的硫转化为FeS沉淀。控制其他条件一定,测得出口处硫转化为FeS的沉淀率与溶液pH的关系如题图-2所示。
A.负极: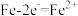 | B.阳极: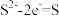 |
C.正极: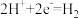 | D.阴极: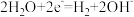 |
(2)该装置沉淀废水中的硫(-2价)的原理可描述为
(3)
 时,pH越大,硫转化为FeS的沉淀率越低,可能的原因是_______。
时,pH越大,硫转化为FeS的沉淀率越低,可能的原因是_______。A.pH越大, 越高, 越高, 与 与 结合转化为 结合转化为 逸出 逸出 |
B.pH越大, 越低,废水中 越低,废水中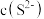 低,则FeS的沉淀率越低 低,则FeS的沉淀率越低 |
C.pH越大,废水中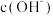 越高, 越高, 与 与 生成 生成 ,导致 ,导致 浓度越小,废水中 浓度越小,废水中 与 与 结合FeS沉淀的硫的量越少 结合FeS沉淀的硫的量越少 |
D.pH越大,废水中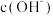 越低,废水中 越低,废水中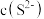 低, 低, 与 与 结合FeS沉淀量越少 结合FeS沉淀量越少 |
Ⅱ.氧化法。
 氧化法、
氧化法、 氧化法、催化氧化法等可以将含硫废水中硫元素氧化。
氧化法、催化氧化法等可以将含硫废水中硫元素氧化。i.
 氧化法:向含
氧化法:向含 的废水中,加入一定量的
的废水中,加入一定量的 溶液,控制溶液的pH为5,可以生成S沉淀。
溶液,控制溶液的pH为5,可以生成S沉淀。(4)写出该反应的离子方程式:
ii.
 氧化法:向含
氧化法:向含 的废水中,加入
的废水中,加入 溶液,其他条件一定,测得硫(-2价)的去除率、S(单质)的生成率与所加
溶液,其他条件一定,测得硫(-2价)的去除率、S(单质)的生成率与所加 溶液体积的关系如题图-3所示。
溶液体积的关系如题图-3所示。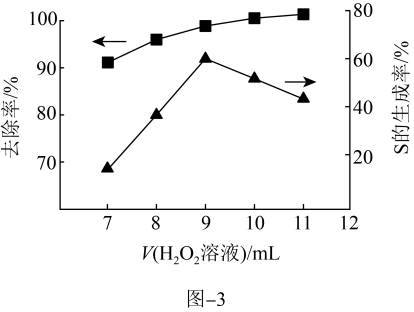
A.加 溶液就是将 溶液就是将 氧化为单质S 氧化为单质S |
B.随着 溶液的不断加入,废水中硫元素的去除率一直在升高 溶液的不断加入,废水中硫元素的去除率一直在升高 |
C. 溶液加入量越多,废水中含硫量越低 溶液加入量越多,废水中含硫量越低 |
D. 在处理一定量的废水中,其加入量不同氧化产物可能有差异 在处理一定量的废水中,其加入量不同氧化产物可能有差异 |
(6)当所加
 溶液体积大于9mL时,所加
溶液体积大于9mL时,所加 溶液越多,S生成率越低,原因是
溶液越多,S生成率越低,原因是iii.催化氧化法:
 苯胺(
苯胺( 为催化剂、聚苯胺为催化剂载体)可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如题图-4所示。
为催化剂、聚苯胺为催化剂载体)可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如题图-4所示。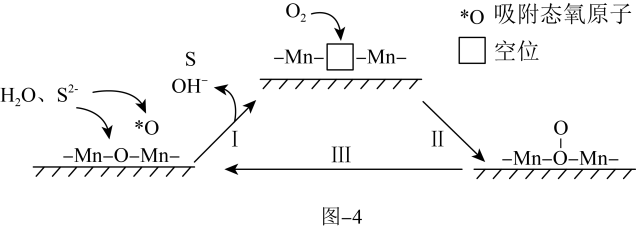
(8)催化剂使用一段时间后催化效率会下降,结合图中相关信息,分析可能原因为
 )浸取催化剂,再干燥即可。
)浸取催化剂,再干燥即可。
您最近一年使用:0次
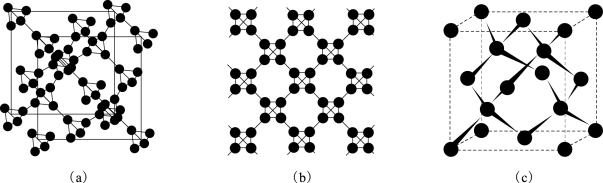
9 . 利用皮秒激光照射悬浮在甲醇溶液中的多壁碳纳米管可以合成T-碳。T-碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成)取代,如图所示[其中图(a)、(b)为T-碳的晶胞和晶胞俯视图,图(c)为金刚石晶胞]。_______ 个碳原子。T-碳的密度非常小,是金刚石的一半,则T-碳晶胞的棱长和金刚石晶胞的棱长之比为_______ 。
您最近一年使用:0次
名校
解题方法
10 . 从化学键的角度解释石墨的熔点高于金刚石的原因_______ 。
您最近一年使用:0次



