名校
1 . 工业上可利用 制备
制备 :
:
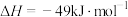
1.500℃时,该反应的平衡常数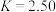 ,该温度下某时刻测得体系内四种物质的浓度均为
,该温度下某时刻测得体系内四种物质的浓度均为 ,则此时
,则此时 ___________
___________ 。
。
2.提高反应速率且增大 的平衡产率,可采取的措施___________。(不定项)
的平衡产率,可采取的措施___________。(不定项)
 制备
制备 :
:
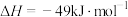
1.500℃时,该反应的平衡常数
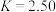 ,该温度下某时刻测得体系内四种物质的浓度均为
,该温度下某时刻测得体系内四种物质的浓度均为 ,则此时
,则此时 ___________
___________ 。
。A. | B. | C. | D.无法确定 |
 的平衡产率,可采取的措施___________。(不定项)
的平衡产率,可采取的措施___________。(不定项)| A.升高反应温度 | B.使用合适的催化剂 |
| C.增大体系压强 | D.从平衡体系中及时分离出 |
您最近一年使用:0次
名校
解题方法
2 .  还原
还原 是实现“双碳”经济的有效途径之一,相关的主要反应有:
是实现“双碳”经济的有效途径之一,相关的主要反应有:
Ⅰ.

Ⅱ.
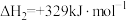
反应 的
的
___________  。
。
 还原
还原 是实现“双碳”经济的有效途径之一,相关的主要反应有:
是实现“双碳”经济的有效途径之一,相关的主要反应有:Ⅰ.


Ⅱ.

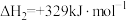
反应
 的
的
 。
。
您最近一年使用:0次
3 . 氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
2.铁镁合金的化学式为___________ 。
3.若该晶胞的晶胞边长为d nm,阿伏加德罗常数为 ,则该合金的密度为
,则该合金的密度为___________  (用含
(用含 的式子表达)。
的式子表达)。
4.若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的体积约为___________L。
的体积约为___________L。

| A.4 | B.6 | C.8 | D.12 |
3.若该晶胞的晶胞边长为d nm,阿伏加德罗常数为
 ,则该合金的密度为
,则该合金的密度为 (用含
(用含 的式子表达)。
的式子表达)。4.若该晶体储氢时,
 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的体积约为___________L。
的体积约为___________L。| A.5.6 | B.11.2 | C.22.4 | D.44.8 |
您最近一年使用:0次
名校
解题方法
4 .  (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度( 350℃)而成为颇具潜力的化学储氢材料之一,它可通过环硼氨烷、
350℃)而成为颇具潜力的化学储氢材料之一,它可通过环硼氨烷、 与
与 进行合成。
进行合成。
1.上述涉及的元素H、B、C、N、O原子半径最大的是___________ ,电负性最大的是___________ 。
2.键角:
___________  (填“
(填“ ”“
”“ ”或“
”或“ ”),原因是
”),原因是___________ 。
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度( 350℃)而成为颇具潜力的化学储氢材料之一,它可通过环硼氨烷、
350℃)而成为颇具潜力的化学储氢材料之一,它可通过环硼氨烷、 与
与 进行合成。
进行合成。1.上述涉及的元素H、B、C、N、O原子半径最大的是
2.键角:

 (填“
(填“ ”“
”“ ”或“
”或“ ”),原因是
”),原因是
您最近一年使用:0次
名校
解题方法
5 . 咔唑(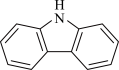 )是一种新型有机液体储氢材料,它的沸点比(
)是一种新型有机液体储氢材料,它的沸点比( )的高,其主要影响因素是
)的高,其主要影响因素是
| A.分子量 | B.极性 | C.氢键 | D.键能 |
您最近一年使用:0次
6 . 钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态锰的价层电子排布式为___________ 。
您最近一年使用:0次
名校
7 . 氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂为___________ 。(写化学式)
您最近一年使用:0次
解题方法
8 . 工业上、高温煅烧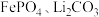 和草酸的混合物制取电池材料磷酸铁锂
和草酸的混合物制取电池材料磷酸铁锂 ,发生的反应为
,发生的反应为
1.配平上述化学方程式并标出电于转移的方向和数目___________ 。
2.一种以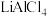 为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。
为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。
3.钠电池与锂离子电池工作原理相似,未来在大规模储能中有广阔的应用前景。与锂电池相比,请分析钠电池可能的优劣(各写一条) ___________ 。
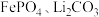 和草酸的混合物制取电池材料磷酸铁锂
和草酸的混合物制取电池材料磷酸铁锂 ,发生的反应为
,发生的反应为
1.配平上述化学方程式并标出电于转移的方向和数目
2.一种以
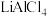 为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。
为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。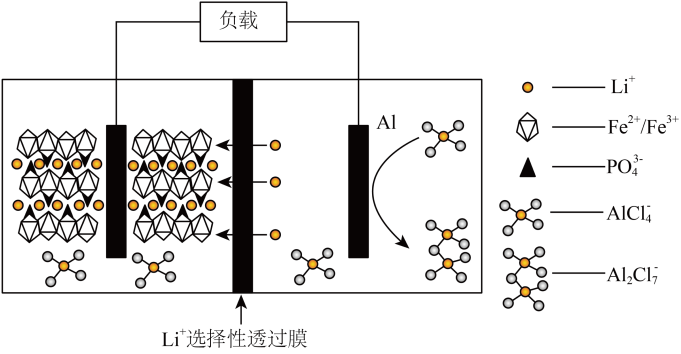
A.放电时,铝电极的电极反应为: | B.放电时, 电极做负极 电极做负极 |
C.充电时, 透过离子交换膜从左向右迁移 透过离子交换膜从左向右迁移 | D.充电时,阳极的电极反应为: |
您最近一年使用:0次
名校
解题方法
9 . 下列有关说法正确的是
A.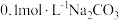 与 与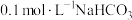 溶液等体积混合: 溶液等体积混合: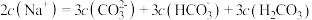 |
B.用相同浓度的 溶液分别滴定等体积 溶液分别滴定等体积 均为3的盐酸和甲酸至终点,消耗 均为3的盐酸和甲酸至终点,消耗 溶液的体积相等 溶液的体积相等 |
C.将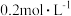 的 的 与 与 的 的 溶液等体积混合后 溶液等体积混合后 ,则: ,则: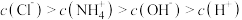 |
D.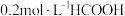 与 与 等体积混合后的溶液中: 等体积混合后的溶液中: |
您最近一年使用:0次
2024-04-21更新
|
59次组卷
|
4卷引用:上海市青浦区2021-2022学年高三下学期适应性练习(二模)化学试题
上海市青浦区2021-2022学年高三下学期适应性练习(二模)化学试题上海市上海师范大学附属中学闵行分校2023-2024学年高二下学期期中考试化学试卷 (已下线)专题05 水溶液中的离子反应与平衡-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(上海专用)(已下线)第八章 水溶液中的离子平衡(测)-2023年高考化学一轮复习讲练测(全国通用)
10 . 氮及其化合物在工农业生产、生活中有着重要作用。
1.下列元素中电负性最大的是____。
2.NH3和PH3都具有四面体结构,NH3比PH3的分解温度高的原因是____。
3.配合物Ni(CO)4也具有四面体结构,常温下Ni(CO)4为液态,易溶于CCl4、苯等有机溶剂。写出基态Ni的电子排布式____ ;Ni(CO)4属于____ 晶体。
4.Zn(NH3)42+离子也具有四面体结构,Zn2+可提供4个能量最低的空轨道与NH3参与形成配位键,这4个空轨道是____。
氨在某催化剂作用下只发生如下反应:
主反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H =-905kJ/mol
4NO(g)+6H2O(g) △H =-905kJ/mol
副反应:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H =-1268kJ/mol
2N2(g)+6H2O(g) △H =-1268kJ/mol
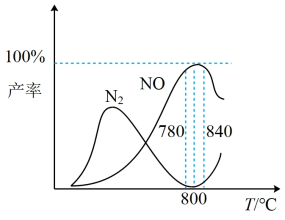
有关物质产率与温度的关系如图。_________ 。
6.工业上采用物料比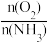 在1.7~2.0,主要目的是:
在1.7~2.0,主要目的是:______________ 。
7.下列说法正确的是______________ 。
A. 工业上进行氨催化氧化生成NO时,温度应控制在780~840℃之间
B. 在加压条件下生产能力可提高5~6倍,是因为加压可提高转化率
C. 选择合适的催化剂,可以大幅度提高NO在最终产物中的比率
8.一定温度下,在3.0L密闭容器中,通入0.10molCH4和0.20molNO2进行反应,CH4(g)+2NO2(g) CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:
CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:
表中数据计算0~4min内υ(NO2)=_________ 。
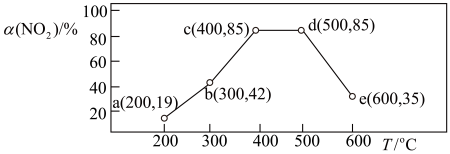
9.在一恒容密闭容器中,通入一定量CH4和NO2,测得在相同时间内,在不同温度下,NO2的转化率 [α(NO2)/%] 如下图;c点___ (填“是”或“不是”)反应达平衡的点。d点之后,转化率随温度升高而降低的原因是___ 。
1.下列元素中电负性最大的是____。
| A.N | B.P | C.Si | D.C |
| A.NH3分子间有氢键 | B.NH3分子极性强 |
| C.N-H键键能大于P-H键 | D.氨极易液化 |
4.Zn(NH3)42+离子也具有四面体结构,Zn2+可提供4个能量最低的空轨道与NH3参与形成配位键,这4个空轨道是____。
| A.3p | B.3d | C.4s | D.4p |
氨在某催化剂作用下只发生如下反应:
主反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H =-905kJ/mol
4NO(g)+6H2O(g) △H =-905kJ/mol副反应:4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H =-1268kJ/mol
2N2(g)+6H2O(g) △H =-1268kJ/mol有关物质产率与温度的关系如图。
6.工业上采用物料比
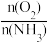 在1.7~2.0,主要目的是:
在1.7~2.0,主要目的是:7.下列说法正确的是
A. 工业上进行氨催化氧化生成NO时,温度应控制在780~840℃之间
B. 在加压条件下生产能力可提高5~6倍,是因为加压可提高转化率
C. 选择合适的催化剂,可以大幅度提高NO在最终产物中的比率
8.一定温度下,在3.0L密闭容器中,通入0.10molCH4和0.20molNO2进行反应,CH4(g)+2NO2(g)
 CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:
CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:| 时间(t/min) | 0 | 2 | 4 | 6 | 8 | 10 |
| 总压强(p/100kPa) | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
9.在一恒容密闭容器中,通入一定量CH4和NO2,测得在相同时间内,在不同温度下,NO2的转化率 [α(NO2)/%] 如下图;c点
您最近一年使用:0次



