1 .  时,将
时,将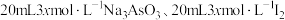 和
和 溶液混合,发生反应:
溶液混合,发生反应: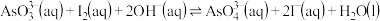 。溶液中
。溶液中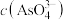 与反应时间(t)的关系如图所示。(忽略混合前后溶液体积的变化)
与反应时间(t)的关系如图所示。(忽略混合前后溶液体积的变化)
2.比较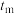 和
和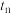 时的化学反应速率,其中
时的化学反应速率,其中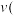 逆)较大的时刻为___________。
逆)较大的时刻为___________。
3.若平衡时溶液的 ,则该反应的平衡常数
,则该反应的平衡常数
___________ 。(用含 和
和 的代数式表示)
的代数式表示)
 时,将
时,将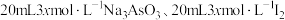 和
和 溶液混合,发生反应:
溶液混合,发生反应: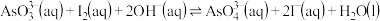 。溶液中
。溶液中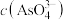 与反应时间(t)的关系如图所示。(忽略混合前后溶液体积的变化)
与反应时间(t)的关系如图所示。(忽略混合前后溶液体积的变化)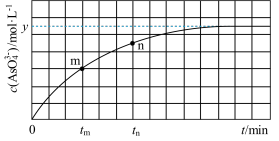
A.溶液的 不再变化 不再变化 | B.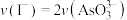 |
C.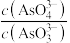 不再变化 不再变化 | D.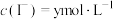 |
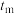 和
和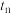 时的化学反应速率,其中
时的化学反应速率,其中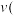 逆)较大的时刻为___________。
逆)较大的时刻为___________。A. | B.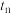 | C.两者相等 | D.无法比较 |
 ,则该反应的平衡常数
,则该反应的平衡常数
 和
和 的代数式表示)
的代数式表示)
您最近一年使用:0次
解题方法
2 . 草酸 是一种白色粉末,
是一种白色粉末,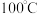 左右开始少量升华,熔点为
左右开始少量升华,熔点为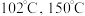 左右分解产生
左右分解产生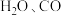 和
和 ;可与酸性
;可与酸性 溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为
溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为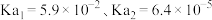 。
。
1.草酸可用于实验室制备少量 气体,应选择的发生装置为
气体,应选择的发生装置为___________ 。
常温下,向某浓度的草酸溶液中加入一定量等浓度的 溶液。
溶液。
3.当 时,溶液呈___________。
时,溶液呈___________。
A.酸性 B.碱性 C.中性 D.无法判断
此时,溶液中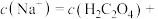
___________ 。
4.当 时,计算该溶液的
时,计算该溶液的
___________ 。(结果保留两位小数)计算过程。
 是一种白色粉末,
是一种白色粉末,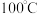 左右开始少量升华,熔点为
左右开始少量升华,熔点为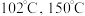 左右分解产生
左右分解产生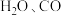 和
和 ;可与酸性
;可与酸性 溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为
溶液反应;其钠盐易溶于水,钙盐难溶于水;电离平衡常数为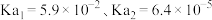 。
。1.草酸可用于实验室制备少量
 气体,应选择的发生装置为
气体,应选择的发生装置为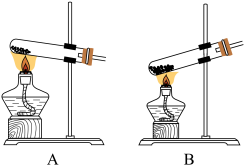
A.用足量的 溶液充分吸收后,可收集得到纯净的 溶液充分吸收后,可收集得到纯净的 |
| B.通过灼热的氧化铜,若出现黑色变红色现象,则产生的气体中一定有CO |
C.通入足量的澄清石灰水中,若能产生白色沉淀,则产生的气体中一定有 |
D.通入酸性 溶液中,若能使溶液褪色,说明草酸具有还原性 溶液中,若能使溶液褪色,说明草酸具有还原性 |
常温下,向某浓度的草酸溶液中加入一定量等浓度的
 溶液。
溶液。3.当
 时,溶液呈___________。
时,溶液呈___________。A.酸性 B.碱性 C.中性 D.无法判断
此时,溶液中
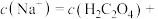
4.当
 时,计算该溶液的
时,计算该溶液的
您最近一年使用:0次
解题方法
3 . 工业上、高温煅烧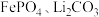 和草酸的混合物制取电池材料磷酸铁锂
和草酸的混合物制取电池材料磷酸铁锂 ,发生的反应为
,发生的反应为
1.配平上述化学方程式并标出电于转移的方向和数目___________ 。
2.一种以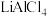 为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。
为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。
3.钠电池与锂离子电池工作原理相似,未来在大规模储能中有广阔的应用前景。与锂电池相比,请分析钠电池可能的优劣(各写一条) ___________ 。
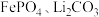 和草酸的混合物制取电池材料磷酸铁锂
和草酸的混合物制取电池材料磷酸铁锂 ,发生的反应为
,发生的反应为
1.配平上述化学方程式并标出电于转移的方向和数目
2.一种以
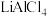 为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。
为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。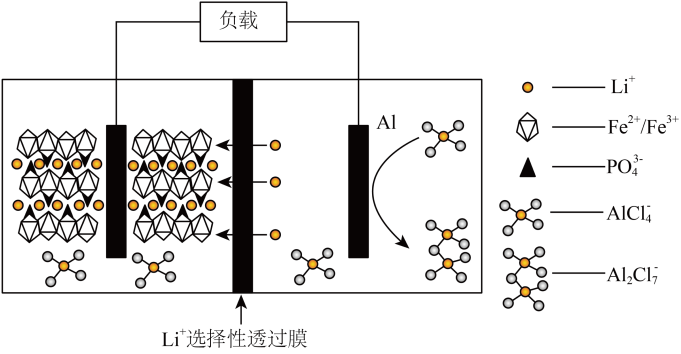
A.放电时,铝电极的电极反应为: | B.放电时, 电极做负极 电极做负极 |
C.充电时, 透过离子交换膜从左向右迁移 透过离子交换膜从左向右迁移 | D.充电时,阳极的电极反应为: |
您最近一年使用:0次
解题方法
4 . 84消毒液的有效成分为
A. | B. | C. | D. |
您最近一年使用:0次
5 . 利用不对称催化合成方法选择性的引入手性碳原于,对天然分子的人工合成意义重大。一种天然分子的部分合成路线如下。(省略部分条件)
2.物质 的名称
的名称___________ 。
3.物质B中含氧官能团的名称___________ 。
4.反应③的反应类型___________ 。___________ 。
6.写出一种满足下列条件的 的同分异构体
的同分异构体___________ 。(填结构简式)
①能与 反应②核磁共振氢谱有3组峰
反应②核磁共振氢谱有3组峰
7.用“*”标出G中的手性碳原子___________ 。
8.结合相关信息,以甲苯和 为原料,制备
为原料,制备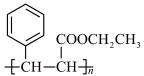 的合成路线
的合成路线___________ 。(无机试剂任选)

| A.油脂 | B.蛋白质 | C.纤维素 | D.聚氯乙烯 |
 的名称
的名称3.物质B中含氧官能团的名称
4.反应③的反应类型
若反应③使用的试剂为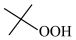 ,除D之外,另一种产物为
,除D之外,另一种产物为
6.写出一种满足下列条件的
 的同分异构体
的同分异构体①能与
 反应②核磁共振氢谱有3组峰
反应②核磁共振氢谱有3组峰7.用“*”标出G中的手性碳原子
8.结合相关信息,以甲苯和
 为原料,制备
为原料,制备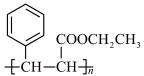 的合成路线
的合成路线
您最近一年使用:0次
解题方法
6 . 三氯异氰尿酸( )被广泛用于工业循环水的消毒。下列说法正确的是
)被广泛用于工业循环水的消毒。下列说法正确的是
| A.第一电离能:N>O>C | B.原子半径:C<N<O | C.所有原子均共面 | D.与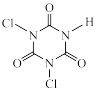 互为同系物 互为同系物 |
您最近一年使用:0次
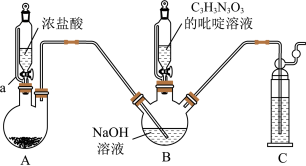
7 . 二氯异氰尿酸钠为白色固体,难溶于冷水,是一种高效、安全的氧化性消毒剂。实验室可用如图所示装置制备(夹持装置已略去)。
1.仪器a中侧管的作用为___________ 。
2.装置A中的药品可以选择 。
3.实验后发现装置 中
中 溶液的利用率较低,改进方法是
溶液的利用率较低,改进方法是___________ 。
4.当从装置B中观察到___________ 时,加入 的吡啶溶液。实验过程中
的吡啶溶液。实验过程中 的温度必须保持在
的温度必须保持在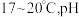 控制在
控制在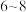 ,则该实验的受热方式是
,则该实验的受热方式是___________ 。
5.反应结束后,装置B中的悬浊液,经过滤、___________ 、干燥,得粗产品。二氯异氰尿酸钠样品的有效氯测定。
(1)准确称取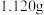 样品,用容量瓶配成
样品,用容量瓶配成 溶液;
溶液;
(2)取 上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封,在暗处静置
上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封,在暗处静置 ;
;
(3)用 标准溶液滴定至溶液呈微黄色,加入淀粉,继续滴定至终点,平均消耗
标准溶液滴定至溶液呈微黄色,加入淀粉,继续滴定至终点,平均消耗 溶液的体积为
溶液的体积为 。
。
已知①部分反应:

②有效氯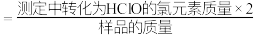
6.步骤(2)中用到的定量仪器有___________ 。
7.该样品的有效氯测定值=___________ 。(结果保留两位小数)
8.下列操作可能会导致样品的有效氯测定值偏低的是 。

1.仪器a中侧管的作用为
2.装置A中的药品可以选择 。
| A.浓硫酸 | B. | C. | D.漂白粉 |
 中
中 溶液的利用率较低,改进方法是
溶液的利用率较低,改进方法是4.当从装置B中观察到
 的吡啶溶液。实验过程中
的吡啶溶液。实验过程中 的温度必须保持在
的温度必须保持在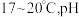 控制在
控制在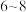 ,则该实验的受热方式是
,则该实验的受热方式是5.反应结束后,装置B中的悬浊液,经过滤、
(1)准确称取
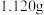 样品,用容量瓶配成
样品,用容量瓶配成 溶液;
溶液;(2)取
 上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封,在暗处静置
上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封,在暗处静置 ;
;(3)用
 标准溶液滴定至溶液呈微黄色,加入淀粉,继续滴定至终点,平均消耗
标准溶液滴定至溶液呈微黄色,加入淀粉,继续滴定至终点,平均消耗 溶液的体积为
溶液的体积为 。
。已知①部分反应:


②有效氯
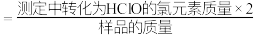
6.步骤(2)中用到的定量仪器有
7.该样品的有效氯测定值=
8.下列操作可能会导致样品的有效氯测定值偏低的是 。
| A.容量瓶水洗后未进行干燥 | B.滴定至溶液蓝色刚好褪去,振荡后又恢复 |
| C.碘量瓶未使用待测液润洗 | D.未在暗处静置 |
您最近一年使用:0次
解题方法
8 . 钙钛矿是指通式为ABO3的一类化合物,最早发现钙钛矿石中的CaTiO3,因此而得名。钙钛矿型化合物可用于生产太阳能电池、传感器、固体电阻器等的功能材料。
1.基态 原子中未成对电子数为
原子中未成对电子数为___________ 。
2. 的四卤化物熔点如下表所示,
的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是___________ 。
 的立方晶胞如图1所示。
的立方晶胞如图1所示。___________ 。
4.金属离子与氧离子间的作用力为 。
5.晶胞中与 距离最近且相等的
距离最近且相等的 数目为 。
数目为 。
一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子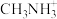 ,其晶胞如图2所示。
,其晶胞如图2所示。 具有相同的空间位置的微粒是 。
具有相同的空间位置的微粒是 。
7.有机碱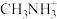 中,
中, 原子的杂化轨道类型是
原子的杂化轨道类型是___________ 。
8.若晶胞参数为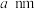 ,则晶体密度为
,则晶体密度为___________  (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
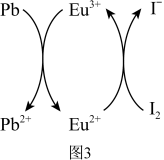
用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了的器件效率和使用寿命。我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图3所示。___________ 、___________ 。
1.基态
 原子中未成对电子数为
原子中未成对电子数为2.
 的四卤化物熔点如下表所示,
的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是| 化合物 |  |  |  |  |
熔点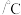 | 377 | -24.12 | 38.3 | 155 |
 的立方晶胞如图1所示。
的立方晶胞如图1所示。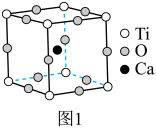
4.金属离子与氧离子间的作用力为 。
| A.离子键 | B.金属键 | C.共价键 | D.分子间作用力 |
 距离最近且相等的
距离最近且相等的 数目为 。
数目为 。| A.4 | B.8 | C.12 | D.16 |
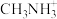 ,其晶胞如图2所示。
,其晶胞如图2所示。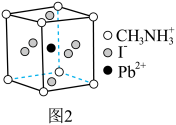
 具有相同的空间位置的微粒是 。
具有相同的空间位置的微粒是 。A. | B. | C. | D.无 |
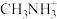 中,
中, 原子的杂化轨道类型是
原子的杂化轨道类型是8.若晶胞参数为
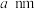 ,则晶体密度为
,则晶体密度为 (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了的器件效率和使用寿命。我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图3所示。
您最近一年使用:0次
解题方法
9 . 自然界中的砷以雄黄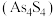 和雌黄
和雌黄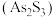 等形式存在,工业上常用雌黄制成浆状,通入
等形式存在,工业上常用雌黄制成浆状,通入 氧化,生成
氧化,生成 和单质硫。
和单质硫。
1.该反应需要在加压下进行,原因是___________ 。
2.已知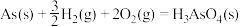

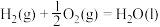

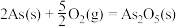

则反应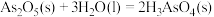 的
的
___________ 。
3.用 去除酸性废水中
去除酸性废水中 的机理如下(“HS·”为自由基,“。”表示孤电子),方框中
的机理如下(“HS·”为自由基,“。”表示孤电子),方框中 的化学式为
的化学式为___________ 。
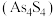 和雌黄
和雌黄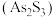 等形式存在,工业上常用雌黄制成浆状,通入
等形式存在,工业上常用雌黄制成浆状,通入 氧化,生成
氧化,生成 和单质硫。
和单质硫。1.该反应需要在加压下进行,原因是
2.已知
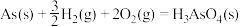

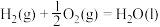

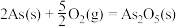

则反应
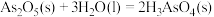 的
的
3.用
 去除酸性废水中
去除酸性废水中 的机理如下(“HS·”为自由基,“。”表示孤电子),方框中
的机理如下(“HS·”为自由基,“。”表示孤电子),方框中 的化学式为
的化学式为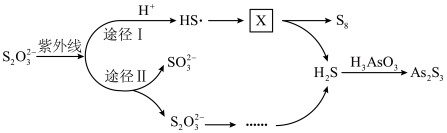
您最近一年使用:0次
10 . 《本草衍义》中对精制砒霜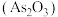 过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒霜上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”
过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒霜上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”
1.精制砒霜过程中涉及的分离提纯方法是 。
2.砒霜的晶体类型为 。
3.检验某混合物中是否含有砒霜,可通过砒霜、锌和盐酸混合反应,生成 来检验。下列说法正确的是 。
来检验。下列说法正确的是 。
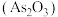 过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒霜上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”
过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒霜上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”1.精制砒霜过程中涉及的分离提纯方法是 。
| A.蒸馏 | B.升华 | C.干馏 | D.萃取 |
| A.分子晶体 | B.离子晶体 | C.共价晶体 | D.金属晶体 |
 来检验。下列说法正确的是 。
来检验。下列说法正确的是 。A. 是氧化产物 是氧化产物 | B. 的电子式: 的电子式: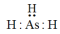 |
C.热稳定性: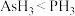 | D. 的空间结构:平面三角形 的空间结构:平面三角形 |
您最近一年使用:0次



