名校
解题方法
1 . 1962年化学家N.Bartlett基于以下两点合成了第一个含有化学键的“惰性气体”化合物——橙黄色固体配合物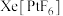 。
。
①一个现象: 能够氧化
能够氧化 生成
生成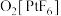 。
。
②一个事实: 的电离能
的电离能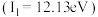 与
与 的电离能
的电离能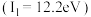 相近。
相近。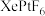 不溶于
不溶于 ,遇水则迅速分解,并放出气体:
,遇水则迅速分解,并放出气体: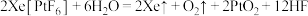 。
。
以 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
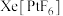 。
。①一个现象:
 能够氧化
能够氧化 生成
生成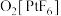 。
。②一个事实:
 的电离能
的电离能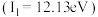 与
与 的电离能
的电离能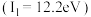 相近。
相近。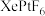 不溶于
不溶于 ,遇水则迅速分解,并放出气体:
,遇水则迅速分解,并放出气体: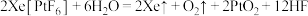 。
。以
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.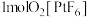 固体中阳离子含有的电子数为 固体中阳离子含有的电子数为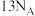 |
B. 中,含有 中,含有 键数为 键数为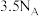 |
C.反应产生 (标况) (标况) ,转移的电子数为 ,转移的电子数为 |
D. 固体中中阴阳离子数共有 固体中中阴阳离子数共有 |
您最近一年使用:0次
2 . 下列有关物质制备的反应方程式错误的是
A.实验室制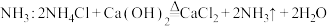 |
B.冶炼金属铝的阴极反应式: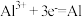 |
C.葡萄糖的银镜反应: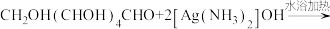  |
D.酚醛树脂的合成原理: |
您最近一年使用:0次
7日内更新
|
174次组卷
|
2卷引用:2024届东北三省四市教研联合体高三下学期高考模拟(二)化学试卷
名校
3 . 胺碘酮(G),属 类抗心律失常药物,已有机物A为原料,其合成路线如下:
类抗心律失常药物,已有机物A为原料,其合成路线如下:
(1)胺碘酮(G)中含氧官能团名称为___________ 。
(2)化合物 中
中 和
和 杂化碳原子的比例为
杂化碳原子的比例为___________ 。
(3)请写出 生成
生成 的反应方程式
的反应方程式___________ 。
(4)B生成 的反应类型为
的反应类型为___________ 。
(5)请写出化合物D的结构简式___________ 。
(6)请写出满足以下条件的D的同分异构体___________ 。
①含有苯环且苯环上只有一个取代基
② 该物质水解消耗
该物质水解消耗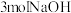
(7)由苯和乙酸酐 合成苯乙烯的路线如下,反应条件已省略。
合成苯乙烯的路线如下,反应条件已省略。 的结构简式:M
的结构简式:M___________ ;N___________ 。
 类抗心律失常药物,已有机物A为原料,其合成路线如下:
类抗心律失常药物,已有机物A为原料,其合成路线如下: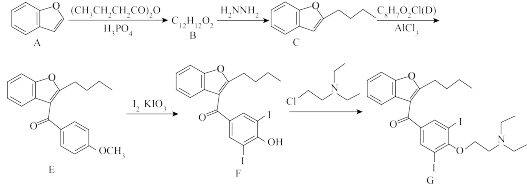
已知: +(RCO)2O
+(RCO)2O
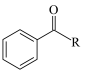 +RCOOH。
+RCOOH。
(1)胺碘酮(G)中含氧官能团名称为
(2)化合物
 中
中 和
和 杂化碳原子的比例为
杂化碳原子的比例为(3)请写出
 生成
生成 的反应方程式
的反应方程式(4)B生成
 的反应类型为
的反应类型为(5)请写出化合物D的结构简式
(6)请写出满足以下条件的D的同分异构体
①含有苯环且苯环上只有一个取代基
②
 该物质水解消耗
该物质水解消耗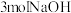
(7)由苯和乙酸酐
 合成苯乙烯的路线如下,反应条件已省略。
合成苯乙烯的路线如下,反应条件已省略。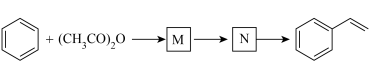
 的结构简式:M
的结构简式:M
您最近一年使用:0次
名校
解题方法
4 . 化合物 可作肥料,其中
可作肥料,其中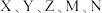 为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有
为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有 和
和 同族。
同族。 的基态原子价层
的基态原子价层 轨道半充满,
轨道半充满, 的基态原子价层电子排布式为
的基态原子价层电子排布式为 在地壳中含量最多。下列说法不正确的是
在地壳中含量最多。下列说法不正确的是
 可作肥料,其中
可作肥料,其中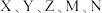 为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有
为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有 和
和 同族。
同族。 的基态原子价层
的基态原子价层 轨道半充满,
轨道半充满, 的基态原子价层电子排布式为
的基态原子价层电子排布式为 在地壳中含量最多。下列说法不正确的是
在地壳中含量最多。下列说法不正确的是A.元素电负性: | B.最简单氢化物沸点: |
C.第一电离能: | D. 和 和 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
解题方法
5 . 芳基亚胺酯是重要的有机反应中间体,受热易分解,可由腈在酸催化下与醇发生Pinner反应制备,原理如下图所示。
Ⅱ.向容器中持续通入HCl气体4小时,密封容器。
Ⅲ.室温下在HCl氛围中继续搅拌反应液24小时,冷却至0℃,抽滤得白色固体,用乙腈洗涤。
Ⅳ.将洗涤后的白色固体加入饱和Na2CO3溶液中,在15℃低温下反应,用有机溶剂萃取3次,合并有机相。
V.向有机相中加入无水硫酸钠,抽滤,蒸去溶剂得产品19.50g。
回答下列问题:
(1)实验室中可用浓盐酸和浓硫酸制备干燥HCl气体,下列仪器中一定需要的为_______ (填仪器名称)。_______ (填标号)。_______ ;实验中选择低温的原因为_______ 。
(4)第Ⅳ步萃取时可选用的有机溶剂为_______(填标号)。
(5)第Ⅳ将洗涤后的白色固体加入饱和Na2CO3溶液中,饱和Na2CO3的作用是_______ 。
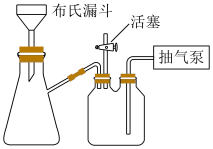
(6)抽滤装置如下图所示,其相对于普通过滤的优点是_______ 。
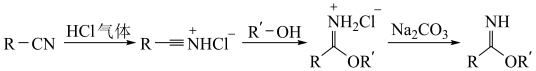
某实验小组以苯甲腈(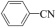 )和三氟乙醇(CF3CH2OH)为原料合成苯甲亚胺三氟乙酯。步骤如下:
)和三氟乙醇(CF3CH2OH)为原料合成苯甲亚胺三氟乙酯。步骤如下:
Ⅱ.向容器中持续通入HCl气体4小时,密封容器。
Ⅲ.室温下在HCl氛围中继续搅拌反应液24小时,冷却至0℃,抽滤得白色固体,用乙腈洗涤。
Ⅳ.将洗涤后的白色固体加入饱和Na2CO3溶液中,在15℃低温下反应,用有机溶剂萃取3次,合并有机相。
V.向有机相中加入无水硫酸钠,抽滤,蒸去溶剂得产品19.50g。
回答下列问题:
(1)实验室中可用浓盐酸和浓硫酸制备干燥HCl气体,下列仪器中一定需要的为

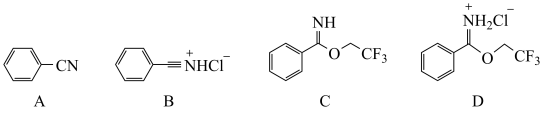
(4)第Ⅳ步萃取时可选用的有机溶剂为_______(填标号)。
| A.甲醇 | B.乙酸 | C.丙酮 | D.乙酸乙酯 |
(5)第Ⅳ将洗涤后的白色固体加入饱和Na2CO3溶液中,饱和Na2CO3的作用是
(6)抽滤装置如下图所示,其相对于普通过滤的优点是
您最近一年使用:0次
解题方法
6 . 我国是最早制得和使用金属锌的国家。某湿法炼锌的萃余液中含有H+、Na+、Zn2+、Fe2+、Mn2+、Co2+、Cd2+、Ni2+、 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
回答下列问题:
(1)按照核外电子排布可把元素周期表分成5个区,Zn元素在_______ 区。
(2)“氧化”时,pH=1,所用氧化剂过二硫酸钠(Na2S2O8)中硫元素化合价为_______ ,Mn2+被氧化为MnO2,Fe2+与Na2S2O8反应的离子方程式是_______ 。
(3)“调pH”时,pH=4,所得滤渣1中除含有MnO2外,还有_______ 。
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理可表示为: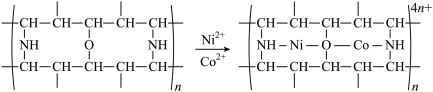 ,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为
,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为_____ 。
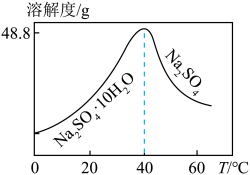
(5)“沉锌” 所得滤液经处理可得Na2SO4溶液,已知Na2SO4的溶解度随温度变化如图所示,由该溶液制备无水Na2SO4的操作为_____ 、洗涤、干燥。_____ 。
 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图: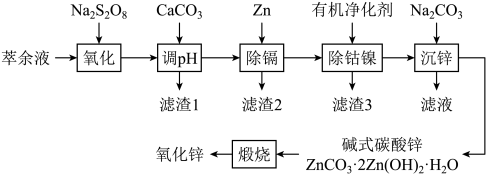
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
| Ksp近似值 | 10-38 | 10-17 | 10-17 |
(1)按照核外电子排布可把元素周期表分成5个区,Zn元素在
(2)“氧化”时,pH=1,所用氧化剂过二硫酸钠(Na2S2O8)中硫元素化合价为
(3)“调pH”时,pH=4,所得滤渣1中除含有MnO2外,还有
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理可表示为:
 ,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为
,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为(5)“沉锌” 所得滤液经处理可得Na2SO4溶液,已知Na2SO4的溶解度随温度变化如图所示,由该溶液制备无水Na2SO4的操作为
您最近一年使用:0次
7 . 化合物 是合成抗病毒药物普拉那韦的原料,其合成路线如下。
是合成抗病毒药物普拉那韦的原料,其合成路线如下。_______ 。
(2)D的化学名称为_______ 。
(3)E→F的反应类型为_______ 。
(4)J的结构简式为_______ 。
(5)M分子中含有两个六元环,则 →M的反应方程式为
→M的反应方程式为_______ 。
(6)在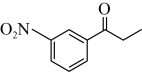 的同分异构体中,满足下列条件的结构有
的同分异构体中,满足下列条件的结构有_______ 种(不考虑立体异构)。
①核磁共振氢谱有5组峰
②遇FeCl3溶液显色
③1mol该物质与银氨溶液反应,最多可生成4molAg
写出其中一种结构简式:_______ 。
 是合成抗病毒药物普拉那韦的原料,其合成路线如下。
是合成抗病毒药物普拉那韦的原料,其合成路线如下。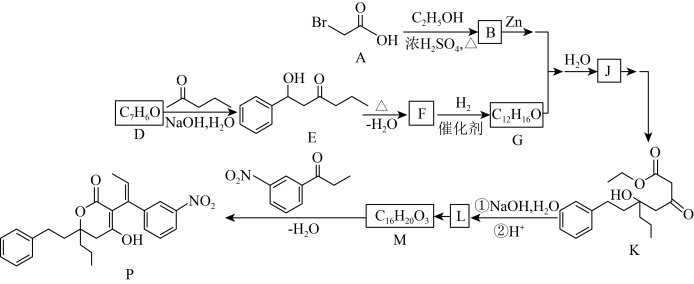
已知: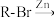
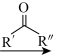

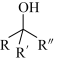
(2)D的化学名称为
(3)E→F的反应类型为
(4)J的结构简式为
(5)M分子中含有两个六元环,则
 →M的反应方程式为
→M的反应方程式为(6)在
 的同分异构体中,满足下列条件的结构有
的同分异构体中,满足下列条件的结构有①核磁共振氢谱有5组峰
②遇FeCl3溶液显色
③1mol该物质与银氨溶液反应,最多可生成4molAg
写出其中一种结构简式:
您最近一年使用:0次
8 . 类比pH,对于稀溶液pc=-lgc,pKa=-lgKa.常温下,向某浓度H2A溶液中加入NaOH(s),保持溶液体积和温度不变,测得pH与pc(H2A)、pc(HA-)、pc(A2-)变化如图所示。下列说法正确的是
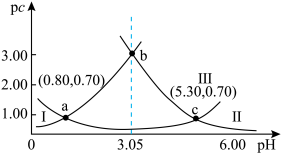
| A.pH=3.05时,c(HA-)>c(A2-)>c(H2A) |
| B.Ka1(H2A)的数量级为10-6 |
| C.c点时,c(Na+)=(10-8.70+3×10-0.7-10-5.30 ) mol·L-1 |
| D.若醋酸的pKa=4.76,则HA-与CH3COO-不能大量共存 |
您最近一年使用:0次
9 . 我国科学家成功合成了世界上首个五氮阴离子盐,局部结构如图所示。其中含有两种10电子离子、一种18电子离子,W、X、Y、Z为原子序数依次增大的短周期元素,Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
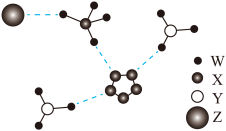
| A.五氮阴离子盐中两种阳离子的立体结构相同 |
| B.X、Y、Z对应的最简单氢化物中沸点最高的是X |
| C.Z的氧化物对应的水化物均为强酸 |
D.五氮阴离子盐中含有的大π键为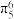 |
您最近一年使用:0次
解题方法
10 . 微生物脱盐电池既可以处理废水中的乙酸和铵盐,又可以实现海水淡化,原理如图所示。下列说法正确的是
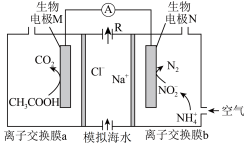
| A.离子交换膜a为阳离子交换膜,b为阴离子交换膜 |
| B.出口R处一定为纯水 |
| C.生成CO2的电极反应式为CH3COOH+2H2O-8e- = 2CO2↑+8H+ |
| D.M极每生成0.1mol CO2,理论上可以从模拟海水中除去117gNaCl |
您最近一年使用:0次



