解题方法
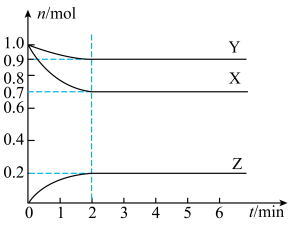
1 . I.某温度下,在2 L的密闭容器中,X、Y、Z三种气体随时间变化的曲线如图所示。
(1)由图中数据分析:该反应的化学方程式为______________ 。
(2)反应开始至2 min,Z的平均反应速率为_____________ 。
(3)5 min时Z的生成速率与6 min时Z的生成速率相比较,前者________ 后者(填“大于”、“小于”或“等于”)。
(4)上述反应过程中,如果降低温度,则其反应速率________ (填“增大”、“减小”或“不变)。如果使用合适的催化剂,则其反应速率________ (填“增大”、“减小”或“不变)。
II.在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)⇌3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,D的化学反应速率v(D)=0.2mol/(L·min)。请回答:
(5)5min末A的物质的量浓度为______________ ;
(6)前5min内用B表示的化学反应速率v(B)为_____________ ;
(7)前5min内A的转化率为____________ ;(转化率是指某一反应物的转化百分率)
(8)化学方程式中n的值为_________ 。
(1)由图中数据分析:该反应的化学方程式为
(2)反应开始至2 min,Z的平均反应速率为
(3)5 min时Z的生成速率与6 min时Z的生成速率相比较,前者
(4)上述反应过程中,如果降低温度,则其反应速率
II.在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)⇌3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,D的化学反应速率v(D)=0.2mol/(L·min)。请回答:
(5)5min末A的物质的量浓度为
(6)前5min内用B表示的化学反应速率v(B)为
(7)前5min内A的转化率为
(8)化学方程式中n的值为
您最近一年使用:0次
解题方法
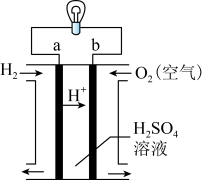
2 . 氢氧燃料电池是一种常见化学电源,其工作示意图如图。___________ (用a或b填写),其电极反应为___________ 。
(2)关于该电池,下列说法正确的是___________。
(3)若用 作燃料,以KOH溶液为电解质溶液,则
作燃料,以KOH溶液为电解质溶液,则 通入电池的
通入电池的___________ (填“正极”或“负极”),该电极反应方程式为___________ 。
(2)关于该电池,下列说法正确的是___________。
A. 由正极流向负极 由正极流向负极 |
B. 溶液的作用是传导电子 溶液的作用是传导电子 |
| C.该电池工作一段时间后,电解质溶液的酸性减弱 |
D.标准状况下a电极若每消耗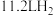 ,外电路转移电子数为 ,外电路转移电子数为 |
(3)若用
 作燃料,以KOH溶液为电解质溶液,则
作燃料,以KOH溶液为电解质溶液,则 通入电池的
通入电池的
您最近一年使用:0次
解题方法
3 . 探究SO2和氯水的漂白性,设计如图实验装置。____________ ,浓硫酸表现出的性质是____________ 。
(2)写出E中反应的离子方程式____________ ,该反应中氧化剂与还原剂的物质的量之比是___________ 。
(3)B、D两试管中溶液褪色后停止通气,再分别加热B、D,现象分别为B:_________ ,D:___________ 。
(4)有同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,于是他将SO2和Cl2按同温同压下体积比1:1同时通入到品红溶液中,结果发现品红溶液未褪色,请分析原因:_________ (用化学方程式表示)。

(2)写出E中反应的离子方程式
(3)B、D两试管中溶液褪色后停止通气,再分别加热B、D,现象分别为B:
(4)有同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,于是他将SO2和Cl2按同温同压下体积比1:1同时通入到品红溶液中,结果发现品红溶液未褪色,请分析原因:
您最近一年使用:0次
4 . 非金属元素与人类的生产生活关系密切,根据常见非金属元素及其化合物的性质回答下列问题。
(1)硅酸盐材料是传统无机非金属材料,硅酸盐具有特殊的性质与应用。下列产品属于硅酸盐的是___________ (填序号)。
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤光导纤维 ⑥水泥 ⑦砖瓦
(2)实验室盛放氢氧化钠溶液的试剂瓶采用橡胶塞的原因是:______________ (用化学方程式表示)。
(3)工业废气中的SO2可以和具有臭鸡蛋气味的气体发生氧化还原反应,其中还原剂和氧化剂的物质的量之比为____________ 。
(4)在汽车排气管安装催化转化装置,CO和NO相互作用生成两种无污染气体,反应的化学方程式为_______________ 。
(1)硅酸盐材料是传统无机非金属材料,硅酸盐具有特殊的性质与应用。下列产品属于硅酸盐的是
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤光导纤维 ⑥水泥 ⑦砖瓦
(2)实验室盛放氢氧化钠溶液的试剂瓶采用橡胶塞的原因是:
(3)工业废气中的SO2可以和具有臭鸡蛋气味的气体发生氧化还原反应,其中还原剂和氧化剂的物质的量之比为
(4)在汽车排气管安装催化转化装置,CO和NO相互作用生成两种无污染气体,反应的化学方程式为
您最近一年使用:0次
解题方法
5 . 在2A+B=3C+4D反应中,表示该反应速率最快的是
| A.v(A)=1.5mol·(L·min)−1 | B.v(D)=0.8mol·(L·min)−1 |
| C.v(C)=3.0mol·(L·min)−1 | D.v(B)=1.2mol·(L·min)−1 |
您最近一年使用:0次
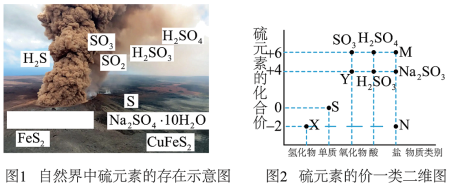
6 . 硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。___________ 。
(2)X与Y反应的化学方程式___________ ,其中还原剂与氧化剂的物质的量之比为___________ 。
(3) 和氯水都有漂白性,有人为增强漂白效果,将
和氯水都有漂白性,有人为增强漂白效果,将 和
和 混合使用,结果适得其反,几乎没有漂白效果,其原因是
混合使用,结果适得其反,几乎没有漂白效果,其原因是___________ (用化学方程式表示)。
(4)下列四种有色溶液与 作用均能褪色:
作用均能褪色:
①酸性 溶液 ②品红溶液 ③淀粉—碘溶液 ④滴有酚酞的NaOH溶液
溶液 ②品红溶液 ③淀粉—碘溶液 ④滴有酚酞的NaOH溶液
体现 漂白性的是
漂白性的是___________ (用序号填空)。体现 还原性的是
还原性的是___________ (用序号填空)。写出 通入酸性
通入酸性 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(5)硝酸是用途广泛的化工原料。铜与浓稀硝酸均能反应,写出铜和稀硝酸反应的离子方程式是___________ 。若64.0gCu与一定量的 溶液反应,当Cu反应完时,共产生标准状况下的4.48L气体(NO和
溶液反应,当Cu反应完时,共产生标准状况下的4.48L气体(NO和 ),则消耗的
),则消耗的 溶液中溶质的物质的量为
溶液中溶质的物质的量为___________ 。
(2)X与Y反应的化学方程式
(3)
 和氯水都有漂白性,有人为增强漂白效果,将
和氯水都有漂白性,有人为增强漂白效果,将 和
和 混合使用,结果适得其反,几乎没有漂白效果,其原因是
混合使用,结果适得其反,几乎没有漂白效果,其原因是(4)下列四种有色溶液与
 作用均能褪色:
作用均能褪色:①酸性
 溶液 ②品红溶液 ③淀粉—碘溶液 ④滴有酚酞的NaOH溶液
溶液 ②品红溶液 ③淀粉—碘溶液 ④滴有酚酞的NaOH溶液体现
 漂白性的是
漂白性的是 还原性的是
还原性的是 通入酸性
通入酸性 溶液反应的离子方程式
溶液反应的离子方程式(5)硝酸是用途广泛的化工原料。铜与浓稀硝酸均能反应,写出铜和稀硝酸反应的离子方程式是
 溶液反应,当Cu反应完时,共产生标准状况下的4.48L气体(NO和
溶液反应,当Cu反应完时,共产生标准状况下的4.48L气体(NO和 ),则消耗的
),则消耗的 溶液中溶质的物质的量为
溶液中溶质的物质的量为
您最近一年使用:0次
解题方法
7 . 工业合成氨的反应如下: 。某温度下,在容积恒定为2.0L的密闭容器中充入
。某温度下,在容积恒定为2.0L的密闭容器中充入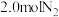 和
和 ,一段时间后反应达平衡状态,实验数据如下表所示:
,一段时间后反应达平衡状态,实验数据如下表所示:
(1)0~50s内的平均反应速率
___________ 。
(2)150s时, 的转化率为
的转化率为___________ 。
(3)反应达最大限度时 的体积分数为
的体积分数为___________ %(保留三位有效数字)。
(4)已知N≡N的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成 过程中的热量变化
过程中的热量变化___________ 。
(5)为加快反应速率,可以采取的措施___________ 。
a.降低温度 b.增大压强 c.恒容时充入He气 d.恒压时充入He气 e.及时分离 f.使用适合催化剂
f.使用适合催化剂
(6)下列说法错误的是___________。
 。某温度下,在容积恒定为2.0L的密闭容器中充入
。某温度下,在容积恒定为2.0L的密闭容器中充入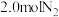 和
和 ,一段时间后反应达平衡状态,实验数据如下表所示:
,一段时间后反应达平衡状态,实验数据如下表所示:| t/s | 0 | 50 | 150 | 250 | 350 |
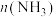 | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0~50s内的平均反应速率

(2)150s时,
 的转化率为
的转化率为(3)反应达最大限度时
 的体积分数为
的体积分数为(4)已知N≡N的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成
 过程中的热量变化
过程中的热量变化(5)为加快反应速率,可以采取的措施
a.降低温度 b.增大压强 c.恒容时充入He气 d.恒压时充入He气 e.及时分离
 f.使用适合催化剂
f.使用适合催化剂(6)下列说法错误的是___________。
| A.使用催化剂是为了加快反应速率,提高生产效率 |
B.上述条件下, 不可能100%转化为 不可能100%转化为 |
C.为了提高 的转化率,应适当提高 的转化率,应适当提高 的浓度 的浓度 |
| D.250~350s生成物浓度保持不变,反应停止 |
您最近一年使用:0次
解题方法
8 . 在一密闭容器中进行反应: ,已知反应过程中某一时刻
,已知反应过程中某一时刻 、
、 、
、 的浓度分别为0.1mol/L、0.05mol/L、0.3mol/L。当反应达到平衡时,可能存在的数据是
的浓度分别为0.1mol/L、0.05mol/L、0.3mol/L。当反应达到平衡时,可能存在的数据是
 ,已知反应过程中某一时刻
,已知反应过程中某一时刻 、
、 、
、 的浓度分别为0.1mol/L、0.05mol/L、0.3mol/L。当反应达到平衡时,可能存在的数据是
的浓度分别为0.1mol/L、0.05mol/L、0.3mol/L。当反应达到平衡时,可能存在的数据是A. 为0.2mol/L, 为0.2mol/L, 为0.15mol/L 为0.15mol/L | B. 、 、 均为0.35mol/L 均为0.35mol/L |
C. 为0.4mol/L 为0.4mol/L | D. 为0.35mol/L 为0.35mol/L |
您最近一年使用:0次
9 . 关于化合物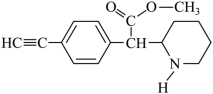 下列说法正确的是
下列说法正确的是
| A.该化合物不可以使溴水褪色 |
| B.该分子苯环上的一氯代物有2种 |
| C.分子中含有1个手性碳原子 |
| D.分子中的所有原子共面 |
您最近一年使用:0次
10 . 苯酚是一种重要的化工原料,其废水对生物具有毒害作用,在排放前必须经过处理。
为回收利用含苯酚的废水,某小组设计如下方案,有关说法正确的是
为回收利用含苯酚的废水,某小组设计如下方案,有关说法正确的是

| A.步骤①中,分液时从分液漏斗下口先放出废水,再放出有机溶液 |
| B.试剂①可用NaOH溶液或Na2CO3溶液 |
| C.步骤①②的操作为分液,步骤③的操作为过滤 |
D.试剂②若为少量CO2,则反应为2 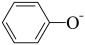 +CO2+H2O=2 +CO2+H2O=2  + + |
您最近一年使用:0次



