名校
解题方法
1 . 三氯三(四氢呋喃)合铬(Ⅲ)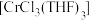 可催化烯烃加聚,制备的方法如下。
可催化烯烃加聚,制备的方法如下。
已知:①CrCl3易潮解,易升华,高温下易被氧气氧化。
②COCl2气体有毒,遇水发生水解产生两种酸性气体。
Ⅰ.制备无水CrCl3:
某化学小组用CCl4(沸点76.8℃)和1.52g Cr2O3在高温下制备无水CrCl3,同时生成COCl2气体,实验装置如图所示:___________ 。
(2)实验装置合理的连接顺序为A___________ B(填装置字母标号,装置不能重复使用)。
(3)g的作用是___________ 。
(4)尾气处理时发生反应的离子方程式___________ 。
Ⅱ.合成CrCl3(THF)3: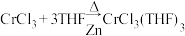
实验操作:按如图组装仪器,将步骤Ⅰ所得无水CrCl3和0.15g锌粉放入滤纸套筒内,双颈烧瓶中加入100mL无水四氢呋喃(THF),通N2 5min后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流2.5h后再通入N2冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品5.39g。___________ 。
(6)索氏提取器的提取管两侧分别是虹吸管和连接管,虹吸管是___________ (填2或3)。
(7)用电加热而不用明火加热的原因___________ 。
(8)产品产率为___________ %(结果保留小数点后一位)。
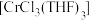 可催化烯烃加聚,制备的方法如下。
可催化烯烃加聚,制备的方法如下。已知:①CrCl3易潮解,易升华,高温下易被氧气氧化。
②COCl2气体有毒,遇水发生水解产生两种酸性气体。
Ⅰ.制备无水CrCl3:
某化学小组用CCl4(沸点76.8℃)和1.52g Cr2O3在高温下制备无水CrCl3,同时生成COCl2气体,实验装置如图所示:

(2)实验装置合理的连接顺序为A
(3)g的作用是
(4)尾气处理时发生反应的离子方程式
Ⅱ.合成CrCl3(THF)3:
①四氢呋喃( ,简写THF)为常见的有机溶剂,沸点66℃,易燃。
,简写THF)为常见的有机溶剂,沸点66℃,易燃。
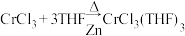
实验操作:按如图组装仪器,将步骤Ⅰ所得无水CrCl3和0.15g锌粉放入滤纸套筒内,双颈烧瓶中加入100mL无水四氢呋喃(THF),通N2 5min后关闭,接通冷却水,加热四氢呋喃至沸腾,在索氏提取器中发生反应,回流2.5h后再通入N2冷却至室温;取下双颈烧瓶,在通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品5.39g。
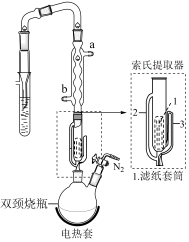
(6)索氏提取器的提取管两侧分别是虹吸管和连接管,虹吸管是
(7)用电加热而不用明火加热的原因
(8)产品产率为
您最近一年使用:0次
名校
解题方法
2 . 近日,西湖大学团队开发了一类水溶性有机储能小分子(M),并提出在电池充放电过程中实现电化学碳捕获一体化,其反应装置与原理如图所示。
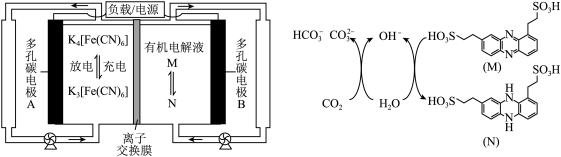
| A.充电时,电极B连接电源的负极 |
B.放电时电极B发生的反应为: |
| C.该电池可采用阳离子交换膜 |
| D.充电时,外电路通过1mole-,理论上该电池最多能够捕获22.4LCO2(标况下) |
您最近一年使用:0次
名校
解题方法
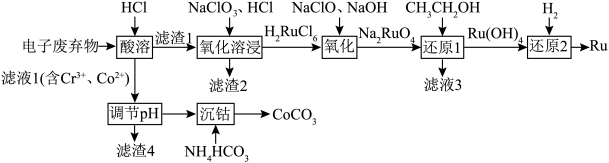
3 . 被誉为“工业维他命”的金属钌(Ru)广泛用于航天航空、制药等领域。以下工艺实现了电子废弃物中金属钌(Ru)的回收利用。已知电子废弃物主要成分为Ru、Co、Cr、Si等物质,请回答以下问题:
(1)电子废弃物在“酸溶”前需要进行粉碎处理,目的是___________ 。
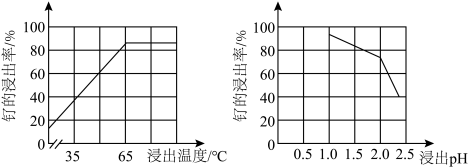
(2)“酸溶”中钌的浸出率与浸出温度、pH的关系如图所示,“酸溶”的最佳条件是___________ 。___________ 。
(4)“沉钴”的离子反应方程式为___________ 。
(5)滤液1中含Cr3+和Co2+的浓度分别为520mg/L、106.2mg/L,“调pH”时调pH的范围为___________ 。(已知:当 时,可认为Mn+已经沉淀完全)
时,可认为Mn+已经沉淀完全)
(6)除加NH4HCO3沉钴外,也可向除杂后的CoCl2溶液中加入(NH4)2C2O4溶液作沉淀剂,可得到草酸钴晶体(CoC2O4·2H2O),但不能用同浓度的Na2C2O4溶液代替(NH4)2C2O4溶液,原因是___________ 。
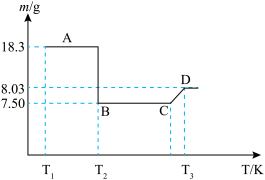
(7)将18.3g草酸钴晶体(CoC2Q4·2H2O)高温灼烧,其热重分析曲线如图:___________ 。
| 化合物 | Cr(OH)3 | Co(OH)2 |
| Ksp | 6.4×10-31 | 1.8×10-15 |
(1)电子废弃物在“酸溶”前需要进行粉碎处理,目的是
(2)“酸溶”中钌的浸出率与浸出温度、pH的关系如图所示,“酸溶”的最佳条件是
(4)“沉钴”的离子反应方程式为
(5)滤液1中含Cr3+和Co2+的浓度分别为520mg/L、106.2mg/L,“调pH”时调pH的范围为
 时,可认为Mn+已经沉淀完全)
时,可认为Mn+已经沉淀完全)(6)除加NH4HCO3沉钴外,也可向除杂后的CoCl2溶液中加入(NH4)2C2O4溶液作沉淀剂,可得到草酸钴晶体(CoC2O4·2H2O),但不能用同浓度的Na2C2O4溶液代替(NH4)2C2O4溶液,原因是
(7)将18.3g草酸钴晶体(CoC2Q4·2H2O)高温灼烧,其热重分析曲线如图:
您最近一年使用:0次
名校
解题方法
4 . 已知X、Y、Z、W都是短周期元素,它们的原子半径大小顺序为Y>Z>W>X。Y的基态原子的电子占据三种能量不同的原子轨道,且有2个单电子;W原子s能级与p能级的电子总数相等。X、Y、W三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体。下列叙述错误的是
| A.W3分子是极性键构成的极性分子 |
| B.M分子中Y的杂化轨道类型为sp2 |
| C.X、Z、W三种元素可形成离子化合物,也可形成共价化合物 |
| D.Z的简单氢化物可作制冷剂,原因是存在分子内氢键,汽化时吸收大量的热 |
您最近一年使用:0次
名校
5 . 有机物G的结构简式为 ,G是合成药物奥美拉挫的重要中间体,实验室可以通过如下合成路线合成G。
,G是合成药物奥美拉挫的重要中间体,实验室可以通过如下合成路线合成G。

(1)苯转化为A的反应条件与试剂是
(2)写出B所含有的官能团名称
(3)C→D的反应类型分别是
(4)X的结构简式为:
(5)试写出D转化E的化学方程式:
(6)D的同分异构体中,能够与FeCl3发生显色反应的有
(7)以甲苯为有机原料(无机试剂任选)合成
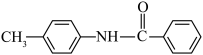 ,设计其合成路线
,设计其合成路线
您最近一年使用:0次
名校
6 . 环戊二烯(C5H6)是一种重要的有机合成原料,常用于有机合成及树脂交联等。
Ⅰ.用其制备环戊烯:
方法一:___________ kJ·mol-1。
①平衡时HI的体积分数为___________ %。
②用平衡分压代替平衡浓度计算压强平衡常数KP=___________ (KPa)-1(要求用最简整数比,含P0的代数式表示)。
③保持温度和体积不变,向平衡体系中再充入等物质的量的环戊二烯和环戊烯,平衡___________ 移动(填“正向”“逆向”或“不”)。___________ T2(填“>"“<”或“=”)。
(4)一定量的环戊二烯气体在恒温恒压的密闭容器中发生上述反应,可说明一定达化学平衡状态的是___________ 。
a.容器内混合气体的密度不再变化
b.容器内混合气体的平均相对分子质量不再变化
c.
d.容器内气体压强不再变化
(5)用环戊二烯制备的二茂铁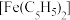 易升华且可溶于有机溶剂中,其晶体类型为
易升华且可溶于有机溶剂中,其晶体类型为___________ 。二茂铁的晶胞结构如图所示(未画出微粒),密度为ρg/cm-3,设阿伏加德罗常数的值为NA,则一个晶胞中含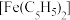 的数目为
的数目为___________ 。
Ⅰ.用其制备环戊烯:
方法一:
反应①: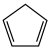 (g)+H2(g)
(g)+H2(g)
 (g) ΔH1=-100.3 kJ·mol-1
(g) ΔH1=-100.3 kJ·mol-1
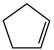
反应②: (g)+H2(g)
(g)+H2(g)
 (g) ΔH2=-109.4 kJ·mol-1
(g) ΔH2=-109.4 kJ·mol-1
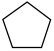
反应③: (g)+
(g)+ (g)
(g) 2
2 (g) ΔH3
(g) ΔH3
方法二: (g)+2HI
(g)+2HI
 (g)+I2(g) ΔH4=-89.3 kJ·mol-1
(g)+I2(g) ΔH4=-89.3 kJ·mol-1
①平衡时HI的体积分数为
②用平衡分压代替平衡浓度计算压强平衡常数KP=
③保持温度和体积不变,向平衡体系中再充入等物质的量的环戊二烯和环戊烯,平衡
Ⅱ.环戊二烯(C5H6)容易二聚生成双环戊二烯(C10H12):2 (g)
(g)
 (g)。不同温度下,溶液中环戊二烯的浓度(初始浓度为1.5mol·L-1)与反应时间的关系如图所示。
(g)。不同温度下,溶液中环戊二烯的浓度(初始浓度为1.5mol·L-1)与反应时间的关系如图所示。

(4)一定量的环戊二烯气体在恒温恒压的密闭容器中发生上述反应,可说明一定达化学平衡状态的是
a.容器内混合气体的密度不再变化
b.容器内混合气体的平均相对分子质量不再变化
c.

d.容器内气体压强不再变化
(5)用环戊二烯制备的二茂铁
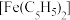 易升华且可溶于有机溶剂中,其晶体类型为
易升华且可溶于有机溶剂中,其晶体类型为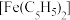 的数目为
的数目为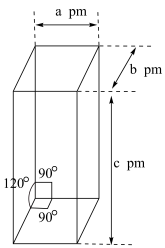
您最近一年使用:0次
名校
7 . 向难溶ACl的饱和溶液(有足量ACl固体)中滴加氨水,发生反应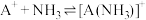 和
和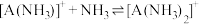 ,
,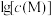 与
与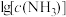 的关系如图所示{其中M代表A+、Cl-、
的关系如图所示{其中M代表A+、Cl-、 、
、 }。
}。
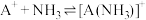 和
和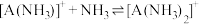 ,
,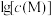 与
与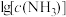 的关系如图所示{其中M代表A+、Cl-、
的关系如图所示{其中M代表A+、Cl-、 、
、 }。
}。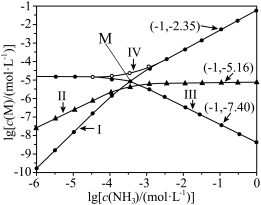
A.曲线Ⅳ表示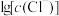 随 随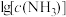 的变化曲线 的变化曲线 |
B.M点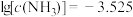 |
C.反应 的平衡常数为10-5.51 的平衡常数为10-5.51 |
| D.完全溶解0.1molACl至少需要含有(0.2+100.35)mol NH3的氨水 |
您最近一年使用:0次
名校
解题方法
8 . 化合物Y是合成丹参醇的中间体,其合成路线如下,下列说法正确的是

| A.Y与Br2以物质的量1:1发生加成反应时可得2种产物 |
B.1)中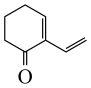 与CH3MgBr反应生成 与CH3MgBr反应生成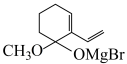 |
| C.一定条件下,X与足量H2加成后的产物分子中含2个手性碳原子 |
| D.X、Y可用酸性KMnO4溶液进行鉴别 |
您最近一年使用:0次
名校
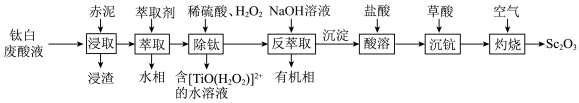
9 . 钪(Sc)及其化合物在电子、超导合金和催化剂等领域有重要应用。一种利用钛白废酸液(含Sc3+、TiO2+、Fe3+的硫酸废液)和赤泥(含有Sc2O3、Al2O3、Fe2O3、SiO2)联合制备Sc2O3的工艺流程如图所示。下列说法错误的是 (当
(当 时,可认为Mn+已经沉淀完全)
时,可认为Mn+已经沉淀完全)
 (当
(当 时,可认为Mn+已经沉淀完全)
时,可认为Mn+已经沉淀完全)| A.水相中含有的金属离子主要是Fe3+、Al3+ |
| B.在“除钛”时,加入H2O2的作用是作氧化剂 |
| C.若使“反萃取”后水溶液中的Sc3+完全沉淀,应控制溶液的pH≥5.7 |
D.草酸钪晶体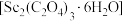 “灼烧”时发生反应的化学方程式: “灼烧”时发生反应的化学方程式: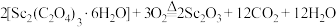 |
您最近一年使用:0次
名校
解题方法
10 . Buchwald-Hartwig偶联反应(布赫瓦尔德-哈特维希反应)是合成芳胺的重要方法,反应机理如图(图中Ar表示芳香烃基,——表示为副反应)。下列说法错误的是
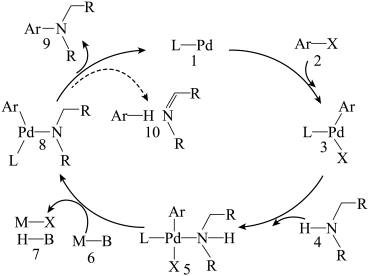
| A.L-Pd是Buchwald-Hartwig偶联反应的催化剂,3、5和8都是反应的中间体 |
B.若原料用Br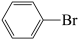 和 和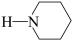 ,则可能得到的产物为 ,则可能得到的产物为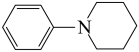 、 、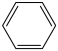 和 和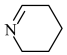 |
C.主反应为:Ar-X+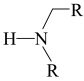 +M-B→H-B+M-X+ +M-B→H-B+M-X+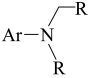 |
| D.该反应机理中所有步骤的原子利用率均为100% |
您最近一年使用:0次



