名校
解题方法
1 . 下列物质微粒间的作用力有饱和性和方向性的是
| A.冰 | B.氯化钠 | C. | D. |
您最近一年使用:0次
名校
2 . 下列化学用语的表述错误的是
A.C2H2的球棍模型: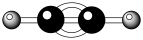 | B.2—丁烯的键线式: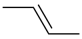 |
C.乙烯中碳碳π键的电子云形状: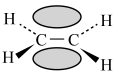 | D.甲基的电子式: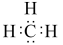 |
您最近一年使用:0次
名校
解题方法
3 . 化学与生产生活密切相关,下列说法错误的是
| A.二氧化硅是制造水泥、玻璃和光导纤维的原料 |
| B.离子液体有良好的导电性,可用作电化学研究的电解质 |
| C.天然气水合物是一种潜在的能源,可燃冰是甲烷水合物,甲烷和水之间存在氢键 |
D.以 为基础,用 为基础,用 取代部分 取代部分 ,用 ,用 取代部分 取代部分 获得的陶瓷,可用于制作LED发光材料 获得的陶瓷,可用于制作LED发光材料 |
您最近一年使用:0次
名校
解题方法
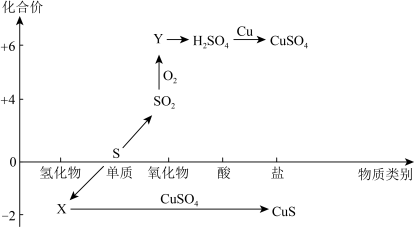
4 . 硫及其化合物的“价-类”二维图如下图所示,回答下列问题:___________ ,Y的化学式是___________ 。
(2)检验 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入___________ ,无明显现象,再加入___________ 溶液,若产生白色沉淀,则溶液中含有 。
。
(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓) CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。
①请用“双线桥”法标明该反应电子转移的方向和数目___________ 。
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为___________ L。
(2)检验
 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入 。
。(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓)
 CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。①请用“双线桥”法标明该反应电子转移的方向和数目
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为
您最近一年使用:0次
名校
5 . 按要求填空
(1)浓硫酸具有如下的性质: A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑___________ ;
②碳投入热的浓硫酸中溶解___________ ;
③浓硫酸与氧化铜反应___________ ;
④浓硫酸干燥氢气___________ 。
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存___________ ;
②常温下可用铝或者铁遇浓硝酸钝化___________ 。
(3)二氧化硫气体在下列反应中表现的性质填写在横线上(填字母序号)。
A氧化性 B.漂白性 C.还原性 D.酸性氧化物的性质
①SO2+2OH= +H2O
+H2O___________ ;
②SO2+2H2S=3S↓+2H2O___________ ;
③SO2+Ca(OH)2=CaSO3↓+H2O___________ ;
④SO2+Cl2+2H2O=2HCl+H2SO4___________ 。
(4)氮元素是地球大气中含量最多的元素,请完成下列有关问题:
①写出氮元素的原子结构示意图:___________ 。
②通常情况下,氮气性质不活泼,其原因是___________ 。
A氮分子是双原子分子 B.氮元素的非金属性很强
C.氮原子的半径较小 D.破坏氮分子中的化学键很难
③N2的电子式:___________ 。
④氨是一种重要的化工原料,请写出工业合成氨的化学方程式:___________ 。
⑤检验NH3的方法是___________ 。
(1)浓硫酸具有如下的性质: A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑
②碳投入热的浓硫酸中溶解
③浓硫酸与氧化铜反应
④浓硫酸干燥氢气
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存
②常温下可用铝或者铁遇浓硝酸钝化
(3)二氧化硫气体在下列反应中表现的性质填写在横线上(填字母序号)。
A氧化性 B.漂白性 C.还原性 D.酸性氧化物的性质
①SO2+2OH=
 +H2O
+H2O②SO2+2H2S=3S↓+2H2O
③SO2+Ca(OH)2=CaSO3↓+H2O
④SO2+Cl2+2H2O=2HCl+H2SO4
(4)氮元素是地球大气中含量最多的元素,请完成下列有关问题:
①写出氮元素的原子结构示意图:
②通常情况下,氮气性质不活泼,其原因是
A氮分子是双原子分子 B.氮元素的非金属性很强
C.氮原子的半径较小 D.破坏氮分子中的化学键很难
③N2的电子式:
④氨是一种重要的化工原料,请写出工业合成氨的化学方程式:
⑤检验NH3的方法是
您最近一年使用:0次
名校
解题方法
6 . 嫦娥5号月球探测器带回的月壤样品的元素分析结果如图,关于含量前六位元素的说法正确的是
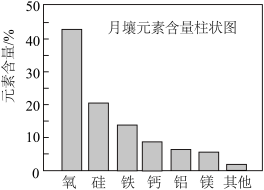
| A.原子半径:Mg<Al<Si | B.第一电离能:Mg<Ca<O |
| C.Fe位于元素周期表的p区 | D.这六种元素中,电负性最大的是O |
您最近一年使用:0次
名校
7 . 金属元素Mg、A1、Ti、Fe、Cu等在电池、储氢材料、催化剂等方面都有广泛应用。请回答下列问题:
(1)储氢材料是一类能可逆地吸收和释放氢气的材料。 是一种储氢材料。H、B、Ti的电负性由大到小的顺序为
是一种储氢材料。H、B、Ti的电负性由大到小的顺序为___________ 。
(2)原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,
表示, 即称为电子的自旋磁量子数。对于基态Fe原子,其价电子自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态Fe原子,其价电子自旋磁量子数的代数和为___________ 。
(3) 是有机催化剂,其水溶液为天蓝色。使溶液呈现天蓝色的四水合铜离子,写出四水合铜离子的结构简式(将配位键表示出来)
是有机催化剂,其水溶液为天蓝色。使溶液呈现天蓝色的四水合铜离子,写出四水合铜离子的结构简式(将配位键表示出来)___________ 。
(4)向上述天蓝色溶液中滴加过量氨水,写出反应的总方程式___________ 。
(5)如图为一种 形成的配离子的结构,该配离子的空间结构为狭长八面体。加热时该离子先失去的配位体是
形成的配离子的结构,该配离子的空间结构为狭长八面体。加热时该离子先失去的配位体是___________ (填化学式),当完全失去该配体时,生成的配离子溶液的颜色为___________ 色。
(1)储氢材料是一类能可逆地吸收和释放氢气的材料。
 是一种储氢材料。H、B、Ti的电负性由大到小的顺序为
是一种储氢材料。H、B、Ti的电负性由大到小的顺序为(2)原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,
表示, 即称为电子的自旋磁量子数。对于基态Fe原子,其价电子自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态Fe原子,其价电子自旋磁量子数的代数和为(3)
 是有机催化剂,其水溶液为天蓝色。使溶液呈现天蓝色的四水合铜离子,写出四水合铜离子的结构简式(将配位键表示出来)
是有机催化剂,其水溶液为天蓝色。使溶液呈现天蓝色的四水合铜离子,写出四水合铜离子的结构简式(将配位键表示出来)(4)向上述天蓝色溶液中滴加过量氨水,写出反应的总方程式
(5)如图为一种
 形成的配离子的结构,该配离子的空间结构为狭长八面体。加热时该离子先失去的配位体是
形成的配离子的结构,该配离子的空间结构为狭长八面体。加热时该离子先失去的配位体是
您最近一年使用:0次
名校
解题方法
8 . 硫是一种重要的非金属元素,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是___________ 。
(2)硫单质的一种结构为 ,S原子的杂化方式为
,S原子的杂化方式为___________ 。
(3)① 、②
、② 、③
、③ 键角由大到小的顺序是
键角由大到小的顺序是___________ 。(用序号回答即可)
(4)熔点:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(5)分析并比较A: 与B:
与B: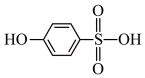 的沸点高低:
的沸点高低:___________ (用A、B表示),原因是___________ 。
(6)ZnS晶胞如图所示: 填在了
填在了 形成的
形成的___________ 空隙中。
②已知晶胞密度为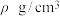 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为___________ cm。
(1)基态硫原子的价层电子排布图是
(2)硫单质的一种结构为
 ,S原子的杂化方式为
,S原子的杂化方式为(3)①
 、②
、② 、③
、③ 键角由大到小的顺序是
键角由大到小的顺序是(4)熔点:

 (填“>”或“<”)。
(填“>”或“<”)。(5)分析并比较A:
 与B:
与B: 的沸点高低:
的沸点高低:(6)ZnS晶胞如图所示:

 填在了
填在了 形成的
形成的②已知晶胞密度为
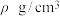 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为
您最近一年使用:0次
名校
解题方法
9 . 原子序数小于等于36的Q、W、X、Y、Z五种元素,原子序数逐渐增大,其中Q是原子半径最小的元素,W和Y的基态原子2p能级所含成单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子,回答下列问题(涉及元素时用对应的元素符号表示):
(1)X、Y、Z三种元素的电负性由大到小的顺序是___________ 。
(2)1mol QWX与1mol 所含
所含 键的比值为
键的比值为___________ 。
(3)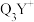 中心原子采用
中心原子采用___________ 杂化,其键角比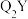 中键角
中键角___________ (填“大”或“小”),原因是:___________ 。
(4)根据VSEPR理论预测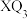 的空间构型为
的空间构型为___________ 。
(5)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为___________ 。
①该化合物的化学式为:___________ 。
②预测该化合物熔点应___________ 金刚石(填“高于”或“低于”),原因是:___________ 。
(1)X、Y、Z三种元素的电负性由大到小的顺序是
(2)1mol QWX与1mol
 所含
所含 键的比值为
键的比值为(3)
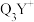 中心原子采用
中心原子采用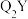 中键角
中键角(4)根据VSEPR理论预测
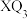 的空间构型为
的空间构型为(5)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为
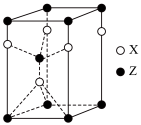
①该化合物的化学式为:
②预测该化合物熔点应
您最近一年使用:0次
名校
10 . 硼的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的电子排布式为:___________ 。
(2) 和过量NaF作用可生成
和过量NaF作用可生成 ,
, 的空间结构为
的空间结构为___________ ; 的电子式为
的电子式为___________ 。
(3)正硼酸( )是一种片层状结构的白色晶体,层内的
)是一种片层状结构的白色晶体,层内的 分子通过氢键相连(如图)。下列有关说法正确的有___________。
分子通过氢键相连(如图)。下列有关说法正确的有___________。
(4)已知硼酸为一元弱酸,写出硼酸的电离方程式___________ 。
(5)硼砂是含结晶水的四硼酸钠。硼砂中阴离子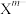 (含B、O、H三种元素)的球棍模型如图所示,则在
(含B、O、H三种元素)的球棍模型如图所示,则在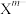 中,2号硼原子的杂化类型为
中,2号硼原子的杂化类型为___________ ;4号硼原子参与形成的化学键有___________ (填选项)。
m=___________ (填数字)。
(1)基态硼原子的电子排布式为:
(2)
 和过量NaF作用可生成
和过量NaF作用可生成 ,
, 的空间结构为
的空间结构为 的电子式为
的电子式为(3)正硼酸(
 )是一种片层状结构的白色晶体,层内的
)是一种片层状结构的白色晶体,层内的 分子通过氢键相连(如图)。下列有关说法正确的有___________。
分子通过氢键相连(如图)。下列有关说法正确的有___________。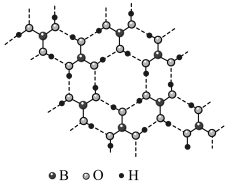
| A.正硼酸晶体属于共价晶体 | B.分子中硼原子最外层为8电子稳定结构 |
C. 分子的稳定性与氢键有关 分子的稳定性与氢键有关 | D.1mol  晶体中平均含3mol氢键 晶体中平均含3mol氢键 |
(4)已知硼酸为一元弱酸,写出硼酸的电离方程式
(5)硼砂是含结晶水的四硼酸钠。硼砂中阴离子
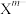 (含B、O、H三种元素)的球棍模型如图所示,则在
(含B、O、H三种元素)的球棍模型如图所示,则在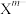 中,2号硼原子的杂化类型为
中,2号硼原子的杂化类型为 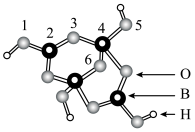
m=
您最近一年使用:0次



