名校
1 . 下列物质沸点的比较,错误的是
A.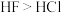 | B.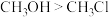 |
C.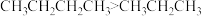 | D.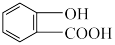   |
您最近一年使用:0次
2024-04-26更新
|
387次组卷
|
2卷引用:黑龙江省哈三中2023-2024学年高二下学期第一次验收考试化学试卷
名校
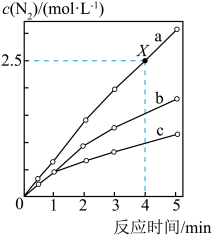
2 . 相同条件下,在固定容积的密闭容器中选用不同的催化剂(a、b、c)发生反应:4NH3(g)+6NO(g) 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
| A.催化剂的催化效率:a>b>c |
| B.X点时,NH3的化学反应速率为0.5 mol·L-1·min-1 |
| C.使用催化剂a、b、c达到平衡时NO的转化率相等 |
| D.若在恒容绝热的密闭容器中发生该反应,当K值不变时,说明反应已经达到平衡 |
您最近一年使用:0次
2024-04-26更新
|
65次组卷
|
2卷引用:黑龙江省大庆市实验中学实验二部2023-2024学年高三下学期得分训练化学试题(七)
3 . 下列实验操作及现象、结论有误的一项是
| 选项 | 实验方案 | 现象 | 结论或解释 |
| A | 浓硫酸与过量 充分反应后,加入 充分反应后,加入 固体 固体 |  继续溶解并产生红棕色气体 继续溶解并产生红棕色气体 | 硫酸有剩余 |
| B | 加热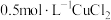 溶液 溶液 | 溶液由蓝色变为黄绿色 | [Cu(H2O)4]2++4Cl-⇌[CuCl4]2-+4H2O反应的 |
| C | 用 试纸测定等物质的量浓度的 试纸测定等物质的量浓度的 和 和 溶液的 溶液的 | 前者 大 大 | 非金属性: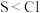 |
| D | 向 溶液中通入 溶液中通入 和气体 和气体 | 出现白色沉淀 | 气体 不一定具有氧化性 不一定具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
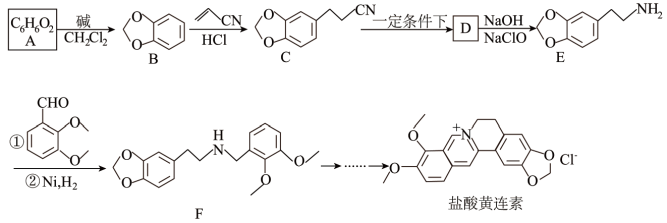
4 . 盐酸黄连素人工合成的路线如下图所示:
(1)B→C的化学方程式为___________ 。
(2)化合物D的分子式为___________ 含有的官能团名称___________ 、___________ 。
(3)E→F中①涉及两步反应,反应类型分别为___________ 、消去反应。
(4)氨基与羧基连在同一碳原子上的氨基酸称为α−氨基酸,分子式与E相同的芳香族 氨基酸有
氨基酸有___________ 种(不考虑立体异构);其中苯环上的氢原子在核磁共振氢谱中有3组吸收峰的化合物的结构简式为___________ 、___________ 。
(5)已知: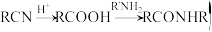 ,写出以乙烯、
,写出以乙烯、 为原料(其他无机试剂任选)制备
为原料(其他无机试剂任选)制备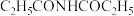 的合成路线。
的合成路线。___________
已知: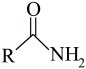

(1)B→C的化学方程式为
(2)化合物D的分子式为
(3)E→F中①涉及两步反应,反应类型分别为
(4)氨基与羧基连在同一碳原子上的氨基酸称为α−氨基酸,分子式与E相同的芳香族
 氨基酸有
氨基酸有(5)已知:
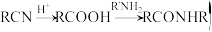 ,写出以乙烯、
,写出以乙烯、 为原料(其他无机试剂任选)制备
为原料(其他无机试剂任选)制备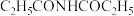 的合成路线。
的合成路线。
您最近一年使用:0次
5 . 用乙烷为原料制备乙烯,可以降低制备成本。
(1)传统制备方法:乙烷催化裂解法发生的反应为:C2H6(g) C2H4(g)+H2(g) ΔH。
C2H4(g)+H2(g) ΔH。
①已知:298K时,相关物质的相对能量如图:___________ 。
②___________ (填高温或低温)有利于此反应自发进行。
(2)乙烷氧化裂解制乙烯[主反应为C2H6(g)+ O2(g)
O2(g) C2H4(g)+H2O(g)
C2H4(g)+H2O(g)
①“乙烷催化裂解法”制备乙烯时,常会发生积碳反应:C2H6(g) 2C(s)+3H2(g),生成的碳会附着在催化剂的表面,降低催化剂的活性,而“乙烷氧化裂解制乙烯”时,很少有积碳,可能原因是
2C(s)+3H2(g),生成的碳会附着在催化剂的表面,降低催化剂的活性,而“乙烷氧化裂解制乙烯”时,很少有积碳,可能原因是___________ 。②探究该反应的适宜条件,得到下图数据:
乙烯的收率=C2H6的转化率×C2H4的选择性。
图甲:表示其它条件相同,不同温度条件下,组成相同的原料气,反应相同的时间,测得的C2H6的转化率、C2H4的选择性以及乙烯的收率与温度的关系;
图乙:表示其他条件相同,C2H6的转化率、C2H4的选择性以及乙烯的收率随原料气中 的变化情况。
的变化情况。
用该方法制备乙烯应该选择的适宜条件为:温度___________ ℃; =
=___________ 。
(3)温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g) HCOOH(g) △H<0 K=2。
HCOOH(g) △H<0 K=2。
①实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k正=___________ k逆。
②温度为T2℃时,k正=1.9k逆,则T2℃时平衡压强___________ (填“大于”“小于”或“等于”)T1℃时平衡压强,判断依据是___________ 。
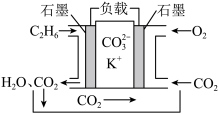
(4)某乙烷熔融燃料电池工作原理如下图所示:___________ 。
(1)传统制备方法:乙烷催化裂解法发生的反应为:C2H6(g)
 C2H4(g)+H2(g) ΔH。
C2H4(g)+H2(g) ΔH。①已知:298K时,相关物质的相对能量如图:
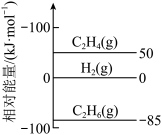
②
(2)乙烷氧化裂解制乙烯[主反应为C2H6(g)+
 O2(g)
O2(g) C2H4(g)+H2O(g)
C2H4(g)+H2O(g)①“乙烷催化裂解法”制备乙烯时,常会发生积碳反应:C2H6(g)
 2C(s)+3H2(g),生成的碳会附着在催化剂的表面,降低催化剂的活性,而“乙烷氧化裂解制乙烯”时,很少有积碳,可能原因是
2C(s)+3H2(g),生成的碳会附着在催化剂的表面,降低催化剂的活性,而“乙烷氧化裂解制乙烯”时,很少有积碳,可能原因是
乙烯的收率=C2H6的转化率×C2H4的选择性。
图甲:表示其它条件相同,不同温度条件下,组成相同的原料气,反应相同的时间,测得的C2H6的转化率、C2H4的选择性以及乙烯的收率与温度的关系;
图乙:表示其他条件相同,C2H6的转化率、C2H4的选择性以及乙烯的收率随原料气中
 的变化情况。
的变化情况。用该方法制备乙烯应该选择的适宜条件为:温度
 =
=(3)温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g)
 HCOOH(g) △H<0 K=2。
HCOOH(g) △H<0 K=2。①实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k正=
②温度为T2℃时,k正=1.9k逆,则T2℃时平衡压强
(4)某乙烷熔融燃料电池工作原理如下图所示:
您最近一年使用:0次
6 . 某工业废水主要含阳离子有 。净化再利用流程如下。
。净化再利用流程如下。 能够在
能够在 为
为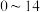 的范围内以离子态稳定存在,不易与
的范围内以离子态稳定存在,不易与 形成沉淀,在氧化过程中氧化不彻底。②
形成沉淀,在氧化过程中氧化不彻底。② 易与废水中的有机物分子形成稳定的配合物,为了简便,通常用
易与废水中的有机物分子形成稳定的配合物,为了简便,通常用 表示③排放标准:Tl的含量低于
表示③排放标准:Tl的含量低于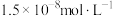
④25℃时部分物质的 如表格所示:
如表格所示:
(1)已知“氧化”步骤中 被还原为
被还原为 ,氧化剂与还原剂物质的量之比为:
,氧化剂与还原剂物质的量之比为:___________ 。
(2)“硫化”步骤的主要目的是除去___________ (填离子符号)。如果无“预中和”步骤,则“硫化”步骤中可能产生___________ (填化学式)。离子方程式为:___________ 。
(3)根据 计算,若使溶液中
计算,若使溶液中 的含量低于排放标准,溶液的
的含量低于排放标准,溶液的 应大于
应大于___________ ,但是实际工艺流程需在“中和”步骤加 至溶液的
至溶液的 约为9,此时仍只有
约为9,此时仍只有 左右的铊离子能得到去除,其可能原因是
左右的铊离子能得到去除,其可能原因是___________ 。
(4)“离子交换”步骤中可用普鲁士蓝{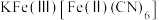 }(其摩尔质量为
}(其摩尔质量为 )中的
)中的 与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的
与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的 如下[
如下[ 未标出,占据四个互不相邻的小立方体(晶胞的
未标出,占据四个互不相邻的小立方体(晶胞的 部分)的体心]。若该晶体的密度为
部分)的体心]。若该晶体的密度为 ,则晶胞参数a为
,则晶胞参数a为___________  (设
(设 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。
 。净化再利用流程如下。
。净化再利用流程如下。
 能够在
能够在 为
为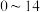 的范围内以离子态稳定存在,不易与
的范围内以离子态稳定存在,不易与 形成沉淀,在氧化过程中氧化不彻底。②
形成沉淀,在氧化过程中氧化不彻底。② 易与废水中的有机物分子形成稳定的配合物,为了简便,通常用
易与废水中的有机物分子形成稳定的配合物,为了简便,通常用 表示③排放标准:Tl的含量低于
表示③排放标准:Tl的含量低于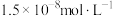
④25℃时部分物质的
 如表格所示:
如表格所示:| 物质 |  |  |  |  |
 | 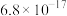 |  |  |  |
(1)已知“氧化”步骤中
 被还原为
被还原为 ,氧化剂与还原剂物质的量之比为:
,氧化剂与还原剂物质的量之比为:(2)“硫化”步骤的主要目的是除去
(3)根据
 计算,若使溶液中
计算,若使溶液中 的含量低于排放标准,溶液的
的含量低于排放标准,溶液的 应大于
应大于 至溶液的
至溶液的 约为9,此时仍只有
约为9,此时仍只有 左右的铊离子能得到去除,其可能原因是
左右的铊离子能得到去除,其可能原因是(4)“离子交换”步骤中可用普鲁士蓝{
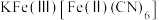 }(其摩尔质量为
}(其摩尔质量为 )中的
)中的 与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的
与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的 如下[
如下[ 未标出,占据四个互不相邻的小立方体(晶胞的
未标出,占据四个互不相邻的小立方体(晶胞的 部分)的体心]。若该晶体的密度为
部分)的体心]。若该晶体的密度为 ,则晶胞参数a为
,则晶胞参数a为 (设
(设 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。
您最近一年使用:0次
7 . 在实验室可用Cl2和NH4Cl溶液反应制取NCl3,所用仪器如图所示(忽略部分夹持装置):
回答下列问题:
(1)盛装NH4Cl的仪器名称为___________ ;药品X可为___________ ;根据气流方向,各仪器的连接顺序为___________ (用各接口字母表示,各接口所需橡胶塞已省略)。
(2)待反应至油状液体不再增加,用止水夹夹住ab间的橡胶管,控制水浴加热的温度范围为___________ ,将产品NCl3蒸出。
(3) NCl3含量测定:NCl3可将HCl氧化为Cl2其化学反应方程式为___________ 。
(4)利用间接碘量法测定氯气的量即可测定NCl3的纯度。实验步骤如下:
ⅰ.准确称量C中的产物0.5g置于三颈烧瓶中,加入10mL足量浓盐酸,使用磁力搅拌器搅拌,并鼓入氮气;
ⅱ.将混合气通入200mL0.1 mol∙L-1KI溶液中,待试管中无色液体变成黄色且颜色不再变化,关闭氮气(溶液体积变化忽略不计);
ⅲ.量取20.00mL吸收液,加入淀粉指示剂,用0.1 mol∙L-1 Na2S2O3标准液进行滴定,滴定至终点时消耗Na2S2O3溶液18.00mL。(已知:反应原理为I2+2Na2S2O3=2NaI+Na2S4O6)
①确定滴定终点的现象为___________ 。
②NCl3的质量为___________ g。(精确到小数点后四位)。
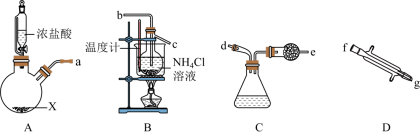
回答下列问题:
(1)盛装NH4Cl的仪器名称为
(2)待反应至油状液体不再增加,用止水夹夹住ab间的橡胶管,控制水浴加热的温度范围为
(3) NCl3含量测定:NCl3可将HCl氧化为Cl2其化学反应方程式为
(4)利用间接碘量法测定氯气的量即可测定NCl3的纯度。实验步骤如下:
ⅰ.准确称量C中的产物0.5g置于三颈烧瓶中,加入10mL足量浓盐酸,使用磁力搅拌器搅拌,并鼓入氮气;
ⅱ.将混合气通入200mL0.1 mol∙L-1KI溶液中,待试管中无色液体变成黄色且颜色不再变化,关闭氮气(溶液体积变化忽略不计);
ⅲ.量取20.00mL吸收液,加入淀粉指示剂,用0.1 mol∙L-1 Na2S2O3标准液进行滴定,滴定至终点时消耗Na2S2O3溶液18.00mL。(已知:反应原理为I2+2Na2S2O3=2NaI+Na2S4O6)
①确定滴定终点的现象为
②NCl3的质量为
您最近一年使用:0次
8 . 草酸(H2C2O4)是一种二元弱酸,在菠菜、苋菜等植物中含量较高。25℃时,向H2C2O4溶液中滴加NaOH溶液,混合溶液中lgX[X表示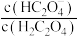 或
或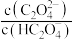 ]随pH的变化关系如图所示。下列说法不正确的是
]随pH的变化关系如图所示。下列说法不正确的是

A.Ⅰ中X表示的是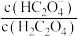 |
B.当溶液pH=4.19时,c(Na+)>3c( ) ) |
C.已知:25℃时,NH3∙H2O的电离常数为 ,则(NH4)2C2O4溶液呈酸性 ,则(NH4)2C2O4溶液呈酸性 |
D.0.1mol∙L-1NaHC2O4溶液中:c(Na+)>c( )>c( )>c( )>c(H2C2O4) )>c(H2C2O4) |
您最近一年使用:0次
9 . 已知: ,向恒温恒容的密闭容器中充入
,向恒温恒容的密闭容器中充入 和
和 发生反应,
发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
 ,向恒温恒容的密闭容器中充入
,向恒温恒容的密闭容器中充入 和
和 发生反应,
发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
| A.容器内压强不变,表明反应达到平衡 |
B.平衡常数 Ⅱ Ⅱ Ⅰ Ⅰ |
C. 时改变的条件:向容器中加入C 时改变的条件:向容器中加入C |
D.平衡时 的体积分数 的体积分数 Ⅱ Ⅱ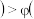 Ⅰ Ⅰ |
您最近一年使用:0次
10 . 下列说法正确的是
A.在 分子中的所有碳原子和氧原子不在同一平面 分子中的所有碳原子和氧原子不在同一平面 |
B.在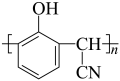 中单体为 中单体为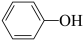 和 和 |
C. 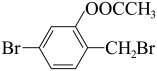 与 与 溶液完全反应,消耗 溶液完全反应,消耗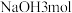 |
D.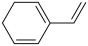 与 与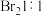 加成可有 加成可有 种加成产物 种加成产物 |
您最近一年使用:0次



