名校
解题方法
1 . 前四周期主族元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中C元素原子的最外层电子数与最内层电子数之和等于其电子总数的一半,下列说法正确的是
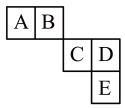
| A.C、D、E三种元素最高价氧化物对应的水化物中D的酸性最强 |
| B.元素C、D形成的简单离子的电子总数不同 |
| C.元素C、D、E形成的常见单质的熔沸点大小:E>D>C |
| D.A的原子半径小于B的原子半径 |
您最近一年使用:0次
2024-04-23更新
|
118次组卷
|
2卷引用:黑龙江省实验中学2022-2023学年高一下学期4月阶段性考试化学试题
名校
解题方法
2 . 高纯硅是现代信息等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:下列说法正确的是
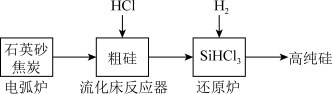
| A.自然界中存在大量的单质硅 |
B.步骤电弧炉中的化学方程式为 |
C.该工艺流程中被循环利用的物质只有 |
| D.该工艺涉及的反应均为氧化还原反应 |
您最近一年使用:0次
名校
解题方法
3 . 某实验小组以BaS溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:
可选用试剂:NaCl晶体、BaS溶液、浓 、稀
、稀 、
、 溶液、蒸馏水
溶液、蒸馏水
步骤1: 的制备
的制备
按如图所示装置进行实验,得到 溶液,经一系列步骤获得
溶液,经一系列步骤获得 产品。
产品。 的含量测定
的含量测定
①称取产品0.5000g,用100mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的0.100mol/L 溶液;
溶液;
③沉淀完全后,60℃水浴40分钟,经过滤、洗涤、烘干等步骤,称量所得白色固体,质量为0.4660g。
回答下列问题:
(1)Ⅰ是制取______ 气体的装置,Ⅱ中b仪器的作用是________ ;Ⅲ中的试剂应选用_______ 。
(2)Ⅱ中发生主要反应的化学方程式为_________ 。
(3)在沉淀过程中,某同学在加入一定量的热 溶液后,认为沉淀已经完全,判断沉淀已经完全的方法是
溶液后,认为沉淀已经完全,判断沉淀已经完全的方法是_________ 。
(4)沉淀过程中需加入过量的 溶液,原因是
溶液,原因是_________ 。
(5)在过滤操作中,下列仪器不需要用到的是_______ (填名称)。 的质量分数为
的质量分数为________ (保留三位有效数字)。
 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:可选用试剂:NaCl晶体、BaS溶液、浓
 、稀
、稀 、
、 溶液、蒸馏水
溶液、蒸馏水步骤1:
 的制备
的制备按如图所示装置进行实验,得到
 溶液,经一系列步骤获得
溶液,经一系列步骤获得 产品。
产品。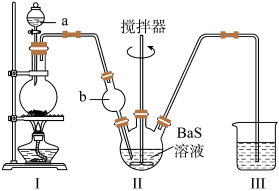
 的含量测定
的含量测定①称取产品0.5000g,用100mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的0.100mol/L
 溶液;
溶液;③沉淀完全后,60℃水浴40分钟,经过滤、洗涤、烘干等步骤,称量所得白色固体,质量为0.4660g。
回答下列问题:
(1)Ⅰ是制取
(2)Ⅱ中发生主要反应的化学方程式为
(3)在沉淀过程中,某同学在加入一定量的热
 溶液后,认为沉淀已经完全,判断沉淀已经完全的方法是
溶液后,认为沉淀已经完全,判断沉淀已经完全的方法是(4)沉淀过程中需加入过量的
 溶液,原因是
溶液,原因是(5)在过滤操作中,下列仪器不需要用到的是

 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
4 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。试回答:
(1)硅元素在元素周期表中位于第___ 周期第____ 族。
(2)下列属于晶体硅的用途的是_____ (填序号)。
①半导体材料 ②制芯片 ③制太阳能电池 ④制光导纤维
(3)写出不能用带有磨口玻璃塞的试剂瓶盛装NaOH的原因(用化学方程式表示)_______ 。
(1)硅元素在元素周期表中位于第
(2)下列属于晶体硅的用途的是
①半导体材料 ②制芯片 ③制太阳能电池 ④制光导纤维
(3)写出不能用带有磨口玻璃塞的试剂瓶盛装NaOH的原因(用化学方程式表示)
您最近一年使用:0次
5 . 我国科学家成功研制出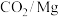 二次电池,在潮湿条件下的放电反应:
二次电池,在潮湿条件下的放电反应: ,模拟装置如图所示(已知放电时,
,模拟装置如图所示(已知放电时, 由负极向正极迁移)。下列说法正确的是
由负极向正极迁移)。下列说法正确的是
 二次电池,在潮湿条件下的放电反应:
二次电池,在潮湿条件下的放电反应: ,模拟装置如图所示(已知放电时,
,模拟装置如图所示(已知放电时, 由负极向正极迁移)。下列说法正确的是
由负极向正极迁移)。下列说法正确的是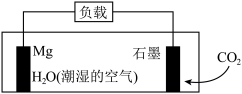
| A.充电时,Mg电极接外电源的正极 |
| B.放电时,电子由镁电极经电解质溶液流向石墨电极 |
C.充电时,阳极的电极反应式为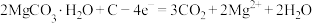 |
D.放电时, 在正极被还原,标准状况下,每消耗6.72L 在正极被还原,标准状况下,每消耗6.72L  转移的电子的物质的量为1.2mol 转移的电子的物质的量为1.2mol |
您最近一年使用:0次
名校
解题方法
6 . 在4L密闭容器中充入6mol A气体和5mol B气体,在一定条件下发生反应: ,5分钟时,生成了1mol C,经测定,D的浓度为0.5
,5分钟时,生成了1mol C,经测定,D的浓度为0.5 ,下列判断正确的是
,下列判断正确的是
 ,5分钟时,生成了1mol C,经测定,D的浓度为0.5
,5分钟时,生成了1mol C,经测定,D的浓度为0.5 ,下列判断正确的是
,下列判断正确的是A. |
B.5分钟时,A的浓度为1.50 |
| C.B的转化率为10% |
| D.5分钟时,在相同温度下容器内混合气体的压强是反应前的85% |
您最近一年使用:0次
名校
解题方法
7 . 下列反应的离子方程式书写正确的是
A. 溶液中加入过量醋酸溶液: 溶液中加入过量醋酸溶液: |
B. 溶液中通入过量 溶液中通入过量 : :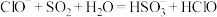 |
C.稀硝酸与FeS反应: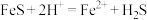 |
D.酸性高锰酸钾溶液中滴加 溶液: 溶液: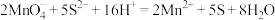 |
您最近一年使用:0次
8 . 高锰酸钾生产过程中产生的废锰渣(主要成分为MnO2、KOH、MgO和Fe2O3)可用于制备MnSO4晶体,工艺流程如下:
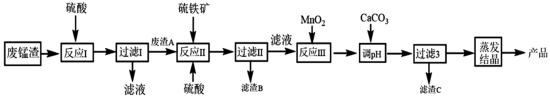
该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
回答以下问题:
(1)MnSO4中阴离子的空间构型为___________ 、阳离子的价电子排布式为___________ 。
(2)提高“反应I”速率可采取的措施是___________ (除“加热”外,任写一种),滤渣A的主要成分为___________ (填化学式)。
(3)“反应II”中硫铁矿(FeS2)的作用为___________ 。
(4)“反应III”的离子方程式为___________ 。
(5)“调pH”步骤中,应调节pH不低于___________ 。

该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀pH | 2.10 | 7.45 | 9 27 27 | 9.60 |
| 完全沉淀pH | 3.20 | 8.95 | 10.87 | 11.13 |
(1)MnSO4中阴离子的空间构型为
(2)提高“反应I”速率可采取的措施是
(3)“反应II”中硫铁矿(FeS2)的作用为
(4)“反应III”的离子方程式为
(5)“调pH”步骤中,应调节pH不低于
您最近一年使用:0次
解题方法
9 . 下列由事实得出的推断结论错误的是
| 选项 | 事实 | 推断结论 |
| A | 价电子排布为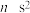 | 该元素不一定是第Ⅱ A族元素 |
| B | X元素的价电子排布为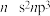 | X的最高正化合价为+5 |
| C | Cu原子有29个电子 | Cu核外有29个不同运动状态的电子 |
| D | 第Ⅰ A族基态原子最外层电子数都是1 | 基态原子价电子排布为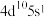 的元素位于第五周期第Ⅰ A族 的元素位于第五周期第Ⅰ A族 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-04更新
|
247次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
10 . X、Y、Z三种元素基态原子的价电子排布式分别为 、
、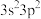 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是
 、
、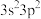 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是A. | B.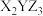 | C.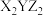 | D. |
您最近一年使用:0次
2024-04-04更新
|
152次组卷
|
10卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期12月月考化学试题
黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期12月月考化学试题宁夏银川市唐徕回民中学2017-2018学年高二4月月考化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题湖南省汨罗市楚雄中学2021-2022学年高二12月月考化学试题四川省广元中学2021-2022学年高二下学期第一次段考化学试题甘肃省武山县第一高级中学2023-2024学年高二下学期第一次月考化学试卷2014-2015河南省实验中学高二下学期期中考试化学试卷云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题



