名校
1 . 回答下列问题
(1)原子形成化合物时,电子云间的相互作用对物质的结构和性质会产生影响。碳原子有4个价电子,在形成化合物时价电子均参与成键,但杂化方式不一定相同。在乙烷、乙烯、乙炔和苯四种分子中,碳原子采取 杂化的是
杂化的是_______ (写结构简式),。试写出一种有机物分子的结构简式,要求同时含有三种不同杂化方式的碳原子:_______ 。
(2)金属钛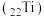 号称航空材料。回答下列问题:
号称航空材料。回答下列问题:
①纳米 是一种应用广泛的催化剂,纳米
是一种应用广泛的催化剂,纳米 催化的一个实例如图所示。
催化的一个实例如图所示。 杂化方式的碳原子个数为
杂化方式的碳原子个数为_______ ,化合物乙中采取 杂化的原子的第一电离能由小到大的顺序为
杂化的原子的第一电离能由小到大的顺序为_______ 。
②有一种氮化钛晶体的晶胞如图所示,该晶体的化学式为_______ ,该晶体中 原子周围距离最近且相等的
原子周围距离最近且相等的 原子的个数为
原子的个数为_______ 。已知晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞边长为
,则晶胞边长为_______ (用含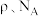 的式子表示)
的式子表示) 。
。
(1)原子形成化合物时,电子云间的相互作用对物质的结构和性质会产生影响。碳原子有4个价电子,在形成化合物时价电子均参与成键,但杂化方式不一定相同。在乙烷、乙烯、乙炔和苯四种分子中,碳原子采取
 杂化的是
杂化的是(2)金属钛
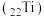 号称航空材料。回答下列问题:
号称航空材料。回答下列问题:①纳米
 是一种应用广泛的催化剂,纳米
是一种应用广泛的催化剂,纳米 催化的一个实例如图所示。
催化的一个实例如图所示。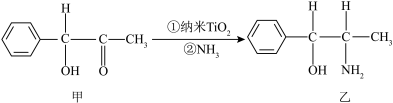
 杂化方式的碳原子个数为
杂化方式的碳原子个数为 杂化的原子的第一电离能由小到大的顺序为
杂化的原子的第一电离能由小到大的顺序为②有一种氮化钛晶体的晶胞如图所示,该晶体的化学式为
 原子周围距离最近且相等的
原子周围距离最近且相等的 原子的个数为
原子的个数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞边长为
,则晶胞边长为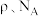 的式子表示)
的式子表示) 。
。
您最近一年使用:0次
名校
解题方法
2 . 按要求完成下列问题
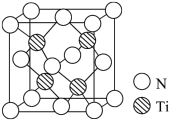
(1)根据下列有机物的结构简式写出其键线式: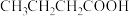
________ ;
(2)用系统命名法命名下列有机物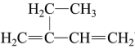
________ ;
(3)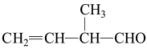 发生加聚反应后所得产物的结构简式为
发生加聚反应后所得产物的结构简式为________ ;
(4)支链只有一个乙基且式量最小的烷烃的结构简式________ ;
(5) 的一氯代物有
的一氯代物有________ 种;
(6)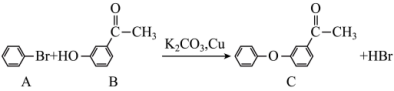 的反应类型为
的反应类型为________ 。
(1)根据下列有机物的结构简式写出其键线式:
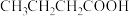
(2)用系统命名法命名下列有机物
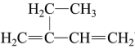
(3)
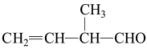 发生加聚反应后所得产物的结构简式为
发生加聚反应后所得产物的结构简式为(4)支链只有一个乙基且式量最小的烷烃的结构简式
(5)
 的一氯代物有
的一氯代物有(6)
 的反应类型为
的反应类型为
您最近一年使用:0次
名校
3 . 下列有机物的命名中正确的是
| A.3-甲基丁烷 | B.2-乙基戊烷 |
| C.2,2-二甲基戊烷 | D.4-甲基-3-乙基戊烷 |
您最近一年使用:0次
名校
解题方法
4 . 属于苯的同系物是
A.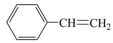 | B.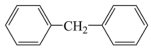 |
C.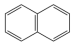 | D.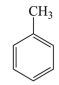 |
您最近一年使用:0次
名校
解题方法
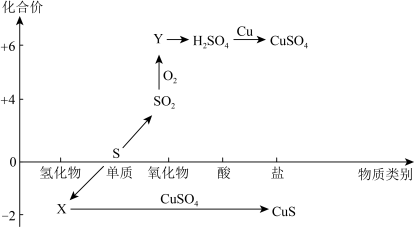
5 . 硫及其化合物的“价-类”二维图如下图所示,回答下列问题:___________ ,Y的化学式是___________ 。
(2)检验 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入___________ ,无明显现象,再加入___________ 溶液,若产生白色沉淀,则溶液中含有 。
。
(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓) CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。
①请用“双线桥”法标明该反应电子转移的方向和数目___________ 。
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为___________ L。
(2)检验
 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入 。
。(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓)
 CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。①请用“双线桥”法标明该反应电子转移的方向和数目
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为
您最近一年使用:0次
名校
6 . 按要求填空
(1)浓硫酸具有如下的性质: A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑___________ ;
②碳投入热的浓硫酸中溶解___________ ;
③浓硫酸与氧化铜反应___________ ;
④浓硫酸干燥氢气___________ 。
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存___________ ;
②常温下可用铝或者铁遇浓硝酸钝化___________ 。
(3)二氧化硫气体在下列反应中表现的性质填写在横线上(填字母序号)。
A氧化性 B.漂白性 C.还原性 D.酸性氧化物的性质
①SO2+2OH= +H2O
+H2O___________ ;
②SO2+2H2S=3S↓+2H2O___________ ;
③SO2+Ca(OH)2=CaSO3↓+H2O___________ ;
④SO2+Cl2+2H2O=2HCl+H2SO4___________ 。
(4)氮元素是地球大气中含量最多的元素,请完成下列有关问题:
①写出氮元素的原子结构示意图:___________ 。
②通常情况下,氮气性质不活泼,其原因是___________ 。
A氮分子是双原子分子 B.氮元素的非金属性很强
C.氮原子的半径较小 D.破坏氮分子中的化学键很难
③N2的电子式:___________ 。
④氨是一种重要的化工原料,请写出工业合成氨的化学方程式:___________ 。
⑤检验NH3的方法是___________ 。
(1)浓硫酸具有如下的性质: A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑
②碳投入热的浓硫酸中溶解
③浓硫酸与氧化铜反应
④浓硫酸干燥氢气
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存
②常温下可用铝或者铁遇浓硝酸钝化
(3)二氧化硫气体在下列反应中表现的性质填写在横线上(填字母序号)。
A氧化性 B.漂白性 C.还原性 D.酸性氧化物的性质
①SO2+2OH=
 +H2O
+H2O②SO2+2H2S=3S↓+2H2O
③SO2+Ca(OH)2=CaSO3↓+H2O
④SO2+Cl2+2H2O=2HCl+H2SO4
(4)氮元素是地球大气中含量最多的元素,请完成下列有关问题:
①写出氮元素的原子结构示意图:
②通常情况下,氮气性质不活泼,其原因是
A氮分子是双原子分子 B.氮元素的非金属性很强
C.氮原子的半径较小 D.破坏氮分子中的化学键很难
③N2的电子式:
④氨是一种重要的化工原料,请写出工业合成氨的化学方程式:
⑤检验NH3的方法是
您最近一年使用:0次
7 . Ⅰ肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH1=−19.5 kJ· mol−1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=−534 kJ· mol−1
(1)写出肼(l)和N2O4(l)完全反应生成N2和水蒸气时的热化学方程式:__________ 。
(2)已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,O—H为462,则断裂1 mol N—H键所需的能量是________ kJ。
Ⅱ.一定条件下铁可以和CO2发生反应Fe(s)+CO2 (g) FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度变化与时间的关系如图所示。
FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度变化与时间的关系如图所示。_______ v逆 (CO2 )(填“>”“<”或“=”)。
(4)0~4min内,CO2的转化率为____________ ,CO的平均反应速率为_________________ 。
(5)下列选项能说明上述反应已达平衡状态的是_______(填字母)。
(6)燃料电池因具有发电效率高。环境污染少等优点而备受人们关注。用于笔记本电脑的甲醇(CH3OH)燃料电池示意图如下,d是_______ 极,此电极反应为_______ 。
①N2(g)+2O2(g)=N2O4(l) ΔH1=−19.5 kJ· mol−1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=−534 kJ· mol−1
(1)写出肼(l)和N2O4(l)完全反应生成N2和水蒸气时的热化学方程式:
(2)已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,O—H为462,则断裂1 mol N—H键所需的能量是
Ⅱ.一定条件下铁可以和CO2发生反应Fe(s)+CO2 (g)
 FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度变化与时间的关系如图所示。
FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度变化与时间的关系如图所示。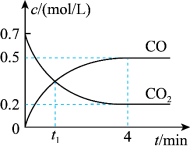
(4)0~4min内,CO2的转化率为
(5)下列选项能说明上述反应已达平衡状态的是_______(填字母)。
| A.v(CO2)=v(CO) |
| B.单位时间内生成n mol Fe的同时生成n mol FeO |
| C.容器中气体压强不随时间的变化而变化 |
| D.容器中CO2浓度不随时间的变化而变化 |

您最近一年使用:0次
2024-04-26更新
|
0次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2023-2024学年高二下学期三月月考化学试题
名校
8 . 完成下列化学方程式(是离子反应的写离子方程式):
(1)等物质的量二氧化硫和氯气通入水中:___________ 。
(2)二氧化硫通入酸性高锰酸钾溶液中:___________ 。
(3)高温煅烧黄铁矿:___________ 。
(4)炭与浓硫酸加热:___________ 。
(5)硫与浓硫酸加热:___________ 。
(6)铜和浓硫酸加热:___________ 。
(7)铜和浓硝酸(实验室制 ):
):___________ 。
(8)铜和稀硝酸(实验室制 ):
):___________ 。
(9)二氧化氮和一氧化氮混合气体通入苛性钠溶液中:___________ 。
(10)二氧化氮通入苛性钠溶液中:___________ 。
(1)等物质的量二氧化硫和氯气通入水中:
(2)二氧化硫通入酸性高锰酸钾溶液中:
(3)高温煅烧黄铁矿:
(4)炭与浓硫酸加热:
(5)硫与浓硫酸加热:
(6)铜和浓硫酸加热:
(7)铜和浓硝酸(实验室制
 ):
):(8)铜和稀硝酸(实验室制
 ):
):(9)二氧化氮和一氧化氮混合气体通入苛性钠溶液中:
(10)二氧化氮通入苛性钠溶液中:
您最近一年使用:0次
名校
解题方法
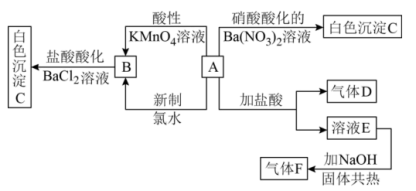
9 . 一种白色晶体A极易溶于水,将A配成溶液进行如下框图所示的实验,实验现象及转化关系如下列框图所示。其中A为正盐,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝。
(1)写出下列物质化学式:A___________ ;C___________ ;
(2)写出F的电子式:___________ ;
(3)写出溶液E与 共热反应的离子方程式:
共热反应的离子方程式:___________ ;
(4)写出A和新制氯水反应的离子方程式:___________ 。
(1)写出下列物质化学式:A
(2)写出F的电子式:
(3)写出溶液E与
 共热反应的离子方程式:
共热反应的离子方程式:(4)写出A和新制氯水反应的离子方程式:
您最近一年使用:0次
10 . 根据对角线规则,下列物质的性质具有相似性的是
| A.碳和铝 | B.铝和铁 | C.硼和硅 | D.铜和金 |
您最近一年使用:0次



