完成下列化学方程式(是离子反应的写离子方程式):
(1)等物质的量二氧化硫和氯气通入水中:___________ 。
(2)二氧化硫通入酸性高锰酸钾溶液中:___________ 。
(3)高温煅烧黄铁矿:___________ 。
(4)炭与浓硫酸加热:___________ 。
(5)硫与浓硫酸加热:___________ 。
(6)铜和浓硫酸加热:___________ 。
(7)铜和浓硝酸(实验室制 ):
):___________ 。
(8)铜和稀硝酸(实验室制 ):
):___________ 。
(9)二氧化氮和一氧化氮混合气体通入苛性钠溶液中:___________ 。
(10)二氧化氮通入苛性钠溶液中:___________ 。
(1)等物质的量二氧化硫和氯气通入水中:
(2)二氧化硫通入酸性高锰酸钾溶液中:
(3)高温煅烧黄铁矿:
(4)炭与浓硫酸加热:
(5)硫与浓硫酸加热:
(6)铜和浓硫酸加热:
(7)铜和浓硝酸(实验室制
 ):
):(8)铜和稀硝酸(实验室制
 ):
):(9)二氧化氮和一氧化氮混合气体通入苛性钠溶液中:
(10)二氧化氮通入苛性钠溶液中:
更新时间:2024-04-12 08:32:07
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(1)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中NH4Cl的作用是______________ 。
(2)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:______ Ce3++_______ H2O2+_____ H2O → _________ Ce(OH)4↓+______ _______
(1)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中NH4Cl的作用是
(2)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
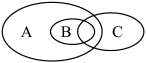
(1)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_______ (填字母)
(2)有同学认为所有酸碱中和反应均可表示为 。请举个例子反驳上述观点(用离子方程式表示)
。请举个例子反驳上述观点(用离子方程式表示)_______ 。
(3)下列反应属于分类中的氧化还原反应。
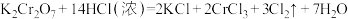
在参加反应的HCl中,起还原剂作用的HCl与起酸性作用的HCl的质量比为_______ ,每生成一个 转移的电子数为
转移的电子数为_______ 。
(4)配平化学方程式,并标出电子转移方向和数目。_______
_______ _______
_______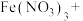 _______
_______ _______
_______ _______
_______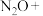 _______
_______
(1)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(2)有同学认为所有酸碱中和反应均可表示为
 。请举个例子反驳上述观点(用离子方程式表示)
。请举个例子反驳上述观点(用离子方程式表示)(3)下列反应属于分类中的氧化还原反应。
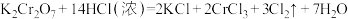
在参加反应的HCl中,起还原剂作用的HCl与起酸性作用的HCl的质量比为
 转移的电子数为
转移的电子数为(4)配平化学方程式,并标出电子转移方向和数目。
_______
 _______
_______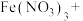 _______
_______ _______
_______ _______
_______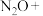 _______
_______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)在 、
、 、
、 、
、 、S微粒中只有氧化性的是
、S微粒中只有氧化性的是_______ ;既有氧化性又有还原性的是_______ 。
(2)在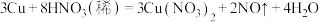 反应中:
反应中:
①_______ 是还原剂,_______ 是还原产物。(填写化学式)
②用单线桥法标出该反应电子转移的方向和数目:_______
③反应中稀硝酸表现出的性质是_______ 。(填写字母)
a.还原性 b.酸性 c.氧化性。
(3)某一反应体系有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 ;已知该反应中
;已知该反应中 只发生如下过程:
只发生如下过程: 。
。
①该反应中,发生还原反应的过程是_______ →_______ 。
②写出该反应的化学方程式:_______ 。
(1)在
 、
、 、
、 、
、 、S微粒中只有氧化性的是
、S微粒中只有氧化性的是(2)在
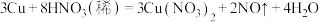 反应中:
反应中:①
②用单线桥法标出该反应电子转移的方向和数目:
③反应中稀硝酸表现出的性质是
a.还原性 b.酸性 c.氧化性。
(3)某一反应体系有反应物和生成物共五种物质:
 、
、 、
、 、
、 、
、 ;已知该反应中
;已知该反应中 只发生如下过程:
只发生如下过程: 。
。①该反应中,发生还原反应的过程是
②写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列八种物质:①Fe;②Ba(HCO3)2;③CaO;④CO2;⑤NaHSO4;⑥熔融KNO3⑦氢氧化铁胶体;⑧稀硝酸。
(1)其中能导电的是___ (填序号);属于非电解质的是___ (填序号)。
(2)⑤在熔融状态下的电离方程式为___ 。
(3)向盛有一定量②溶液的试管中逐滴加入一定量的⑤溶液至恰好沉淀完全,此时对应的离子方程式为___ ;之后继续向试管中加入⑤溶液,现象为___ ,对应的离子方程式为___ 。
(4)①与⑧发生反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,HNO3在此反应中表现的性质是___ 。
(1)其中能导电的是
(2)⑤在熔融状态下的电离方程式为
(3)向盛有一定量②溶液的试管中逐滴加入一定量的⑤溶液至恰好沉淀完全,此时对应的离子方程式为
(4)①与⑧发生反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,HNO3在此反应中表现的性质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】将32g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为___________ L, 的体积为
的体积为___________ L。
(2)参加反应的硝酸的物质的量是___________ mol。
(3)待产生的气体全部释放后,向溶液加入V mL a mol/L的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为___________ mol/L。(结果不需化简)
(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为 ,至少需要30%的双氧水
,至少需要30%的双氧水_________ g。
 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:(1)NO的体积为
 的体积为
的体积为(2)参加反应的硝酸的物质的量是
(3)待产生的气体全部释放后,向溶液加入V mL a mol/L的NaOH溶液,恰好使溶液中的
 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为
 ,至少需要30%的双氧水
,至少需要30%的双氧水
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.食醋是烹饪美食的调味品,有效成分主要为醋酸。
(1)配制250mL0.1mol/L的醋酸溶液,需5mol/L醋酸溶液的体积为_______ mL(保留到小数点后一位)
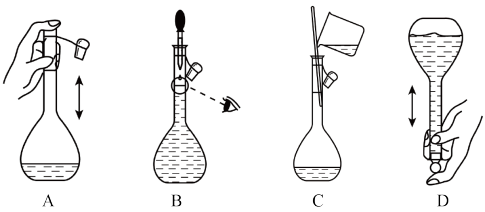
(2)下列关于某容积的容量瓶的操作,正确的是_______ 。
II.人工固氮合成氨,并通过氨氧化法制取硝酸的流程如图所示。
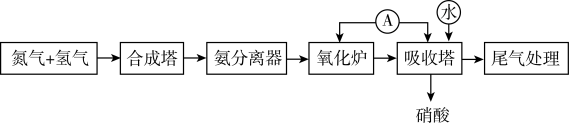
(3)“合成塔”内发生的化学反应中作氧化剂的是_______ (填化学式),金属镁在该氧化剂中燃烧的化学方程式为_______ ,其产物遇水生成的有刺激性气味气体的电子式为_______ ,分子构型为_______ ;“氧化炉”中氨气发生反应的化学方程式为_______ 。
(4)常温下,工业上选择铁或铝作盛装浓硝酸的罐体材料的主要原因是_______
(5)为了避免生成硝酸的过程中氮的氧化物污染环境,可用氨气处理尾气,将其转化为大气中含有的无害气体,以处理 为例,该反应中氧化剂与还原剂的物质的量之比为
为例,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(1)配制250mL0.1mol/L的醋酸溶液,需5mol/L醋酸溶液的体积为
(2)下列关于某容积的容量瓶的操作,正确的是

II.人工固氮合成氨,并通过氨氧化法制取硝酸的流程如图所示。

(3)“合成塔”内发生的化学反应中作氧化剂的是
(4)常温下,工业上选择铁或铝作盛装浓硝酸的罐体材料的主要原因是
(5)为了避免生成硝酸的过程中氮的氧化物污染环境,可用氨气处理尾气,将其转化为大气中含有的无害气体,以处理
 为例,该反应中氧化剂与还原剂的物质的量之比为
为例,该反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求书写化学方程式或离子方程式。
(1)除去氯化亚铁溶液中的氯化铁杂质,相应的离子方程式为___________ 。
(2)工业上用FeCl3溶液腐蚀铜线路板,相应的离子方程式为___________ 。
(3)浓硫酸和铜反应,相应的化学方程式为___________ 。
(4)Fe(OH)2在空气中被氧化,相应的化学方程式为___________ 。
(5)SO2能使氯水褪色,相应的离子方程式为___________ 。
(1)除去氯化亚铁溶液中的氯化铁杂质,相应的离子方程式为
(2)工业上用FeCl3溶液腐蚀铜线路板,相应的离子方程式为
(3)浓硫酸和铜反应,相应的化学方程式为
(4)Fe(OH)2在空气中被氧化,相应的化学方程式为
(5)SO2能使氯水褪色,相应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】运用比较方法是化学科学中研究物质性质的基本方法之一,请运用比较法解答下题:过氧化钠几乎可与所有的常见气态非金属氧化物反应。
如:2Na2O2+2CO2=2Na2CO3+O2↑,Na2O2+2CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:
_____________________ 。_______________________ 。
(2)通过比较可知,当非金属元素处于______________ 价时,其氧化物与过氧化钠反应有O2生成。
如:2Na2O2+2CO2=2Na2CO3+O2↑,Na2O2+2CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:
(2)通过比较可知,当非金属元素处于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】分别向盛有①紫色石蕊溶液、②NaOH溶液、③品红溶液、④酸性高锰酸钾溶液的试管中通入SO2气体。
(1)试管①中的现象:___________ ,发生反应的化学方程式是:___________ 。
(2)试管②中发生反应的化学方程式是:___________ ,如果通入过量的SO2,则发生反应的化学方程式为:___________ 。
(3)试管③中的现象:___________ ,如将吸收SO2后的该溶液加热,现象:___________ 。
(4)试管④中的现象:___________ 。
(5)写出实验室用浓硫酸和铜制SO2的化学方程式:___________ 。
(1)试管①中的现象:
(2)试管②中发生反应的化学方程式是:
(3)试管③中的现象:
(4)试管④中的现象:
(5)写出实验室用浓硫酸和铜制SO2的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】当硝酸与金属或非金属反应时,反应物或反应条件不同,硝酸被还原的产物也不同。请回答下列问题:
(1)金属Zn与某浓度的硝酸反应时无气体产生,那么硝酸的还原产物为_______ (填化学式)。
(2)某混酸由200mL3mol·L-1的稀硝酸和200mL2.5mol·L-1的稀硫酸均匀混合而成(忽略溶液的体积变化)。将其分成两等份,分别与铜和铁反应,还原产物只有NO,则最多能溶解_______ molCu,_______ gFe,并写出离子方程式_______ 。
(3)200mL16mol·L-1的浓硝酸与3.2gCu反应,反应过程中还原产物只有NO2,则反应结束后,产生气体的体积为_______ (标准状况下),溶液中c(H+)∶c( )=
)=_______ (忽略HNO3的挥发)。
(4)用试管将(3)反应产生的NO2收集满并倒立在足量的水中,待试管中液面不再上升时,试管中剩余气体的体积约为原气体体积的_______ 。试管中的液体的物质的量浓度为_______ (假设试管中的液体不对外扩散,此反应条件下1mol气体的体积为25.0L)。如果NO2中混有N2O4气体,试管中的液体的物质的量浓度将_______ (填“增大”“减小”或“不变”)。
(5)写出FeO和稀硝酸的离子方程式_______ 。
(1)金属Zn与某浓度的硝酸反应时无气体产生,那么硝酸的还原产物为
(2)某混酸由200mL3mol·L-1的稀硝酸和200mL2.5mol·L-1的稀硫酸均匀混合而成(忽略溶液的体积变化)。将其分成两等份,分别与铜和铁反应,还原产物只有NO,则最多能溶解
(3)200mL16mol·L-1的浓硝酸与3.2gCu反应,反应过程中还原产物只有NO2,则反应结束后,产生气体的体积为
 )=
)=(4)用试管将(3)反应产生的NO2收集满并倒立在足量的水中,待试管中液面不再上升时,试管中剩余气体的体积约为原气体体积的
(5)写出FeO和稀硝酸的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将一定质量的铜片加入到20 mL某浓度的浓硝酸中,充分反应后,铜片全部溶解,并收集到标准状况下的混合气体共896mL(假设气体中只有NO和NO2)。向反应后所得溶液中逐滴滴加1mol/L的NaOH溶液,产生沉淀质量与加入NaOH溶液体积(单位:mL)的关系如图所示。回答下列问题:
(1)B点所表示溶液中只含一种溶质,该物质是_______ (填化学式)。
(2)收集的气体中,NO2的物质的量为______ mol。
(3)铜片的质量为______ g。
(4)原浓硝酸的浓度为________________ mol/L。

(1)B点所表示溶液中只含一种溶质,该物质是
(2)收集的气体中,NO2的物质的量为
(3)铜片的质量为
(4)原浓硝酸的浓度为
您最近一年使用:0次



