运用比较方法是化学科学中研究物质性质的基本方法之一,请运用比较法解答下题:过氧化钠几乎可与所有的常见气态非金属氧化物反应。
如:2Na2O2+2CO2=2Na2CO3+O2↑,Na2O2+2CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:
_____________________ 。_______________________ 。
(2)通过比较可知,当非金属元素处于______________ 价时,其氧化物与过氧化钠反应有O2生成。
如:2Na2O2+2CO2=2Na2CO3+O2↑,Na2O2+2CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:
(2)通过比较可知,当非金属元素处于
9-10高一下·河北邯郸·期末 查看更多[1]
(已下线)09-10年邯郸市高一下学期期末质量检测化学卷
更新时间:2016-12-09 00:42:16
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】硫的氧化物、氮的氧化物是常见的大气污染物。
(1)酸雨是降水呈酸性(pH小于5.6)统称,个别地方甚至低于2.1(食醋的pH=3)。引起酸雨的罪魁祸首是大气中的硫的氧化物和氮的氧化物,它们的主要来源是煤和石油的燃烧。
①汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排放量约为5×107kg。NO2溶于水发生反应的化学方程式为:___________ 。
②为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫元素进行固化处理,对废气中氮的氧化物用______ 吸收,写出NO2与之反应的离子方程式_____ 。
(2)某化学兴趣小组选用如图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。
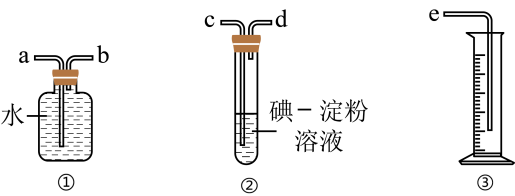
①若原料气从左向右流时,上述装置连接的顺序是______ (填字母)。
②装置②中发生反应的离子方程式为:______ ;当装置②中出现_______ 现象时,立即停止通气。
③你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是__________ 。
A.酸性KMnO4溶液 B.NaOH溶液 C.溴水 D.氨水
(1)酸雨是降水呈酸性(pH小于5.6)统称,个别地方甚至低于2.1(食醋的pH=3)。引起酸雨的罪魁祸首是大气中的硫的氧化物和氮的氧化物,它们的主要来源是煤和石油的燃烧。
①汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排放量约为5×107kg。NO2溶于水发生反应的化学方程式为:
②为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫元素进行固化处理,对废气中氮的氧化物用
(2)某化学兴趣小组选用如图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。

①若原料气从左向右流时,上述装置连接的顺序是
②装置②中发生反应的离子方程式为:
③你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是
A.酸性KMnO4溶液 B.NaOH溶液 C.溴水 D.氨水
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:___________ ;
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:___________ ;
(3)制漂白粉原理:___________ ;
(4)高温下Fe与水蒸气反应:___________ 。
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:___________ ;
(6)Al粉与NaOH溶液反应:___________ ;
(7)酸性条件下,向含铬废水中加FeSO4,将 还原为Cr3+:
还原为Cr3+:___________ ;
(8)制Fe(OH)3胶体:___________ 。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:
(3)制漂白粉原理:
(4)高温下Fe与水蒸气反应:
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:
(6)Al粉与NaOH溶液反应:
(7)酸性条件下,向含铬废水中加FeSO4,将
 还原为Cr3+:
还原为Cr3+:(8)制Fe(OH)3胶体:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硅、硫、氮是重要的非金属元素。回答下列问题:
(1)SiO2属于_______ (填“酸性”“碱性”或“两性”)氧化物。盛装NaOH等碱性溶液的试剂瓶不能用玻璃塞,其原因为_______ (用化学方程式表示)。
(2)工业上用石英砂和焦炭混合高温制取粗硅,其反应的化学方程式为_______ ;硅的用途有_______ (任写1个)。
(3)由SO3制备H2SO₄的过程中,一般用98.3%的浓硫酸吸收SO3,而不是直接用蒸馏水吸收的原因是_______ 。
(4)实验室利用含Fe3+的溶液吸收SO2,从而实现SO2的回收利用。写出Fe3+与SO2在水溶液中发生反应的离子方程式:_______ ;SO2_______ (填“被氧化”或“被还原”);每消耗32gSO2,转移电子的物质的量为_______ mol。
(5)氨气遇氯化氢时会产生白烟,写出白烟化学成分的电子式:_______ 。
(1)SiO2属于
(2)工业上用石英砂和焦炭混合高温制取粗硅,其反应的化学方程式为
(3)由SO3制备H2SO₄的过程中,一般用98.3%的浓硫酸吸收SO3,而不是直接用蒸馏水吸收的原因是
(4)实验室利用含Fe3+的溶液吸收SO2,从而实现SO2的回收利用。写出Fe3+与SO2在水溶液中发生反应的离子方程式:
(5)氨气遇氯化氢时会产生白烟,写出白烟化学成分的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了 C2H5OH、CO2、Fe2O3、FeCl3、KOH五种物质,图中相连的物质均可归为一类,相交部分 A、B、C、D 为相应的分类标准代号:
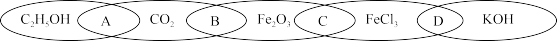
①相连的两种物质都是电解质的是_____ (填分类标准代号,下同)。
②图中相连的两种物质能够相互反应的是_____ ,所属基本反应类型的是_____ 反应。
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的化学方程式为_____
④用洁净的烧杯取 25mL 蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热至液体呈红褐色,证明该分散系生成的实验原理是_____ 。
(2)分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼。如:
①CO2、SiO2、SO2、SO3都属于酸性氧化物,由 CO2+Ca(OH)2=CaCO3↓+H2O,可完成 SO3与NaOH反应的方程式为_____ 。
②NaHCO3、NaHSO3、NaHS 都属于弱酸形成的酸式盐,由 NaHCO3+HCl=NaCl+H2O+CO2↑及NaHCO3+NaOH=Na2CO3+H2O,可完成 NaHS 分别与 HCl、NaOH 反应的方程式为___________ 。
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了 C2H5OH、CO2、Fe2O3、FeCl3、KOH五种物质,图中相连的物质均可归为一类,相交部分 A、B、C、D 为相应的分类标准代号:
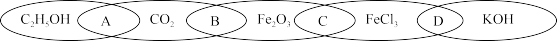
①相连的两种物质都是电解质的是
②图中相连的两种物质能够相互反应的是
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的化学方程式为
④用洁净的烧杯取 25mL 蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热至液体呈红褐色,证明该分散系生成的实验原理是
(2)分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼。如:
①CO2、SiO2、SO2、SO3都属于酸性氧化物,由 CO2+Ca(OH)2=CaCO3↓+H2O,可完成 SO3与NaOH反应的方程式为
②NaHCO3、NaHSO3、NaHS 都属于弱酸形成的酸式盐,由 NaHCO3+HCl=NaCl+H2O+CO2↑及NaHCO3+NaOH=Na2CO3+H2O,可完成 NaHS 分别与 HCl、NaOH 反应的方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】过氧化钠在分析化学中常用来氧化分解(碱熔)某些矿物。例如它能将硫、锰、铬、钒、锡等成分氧化成可溶的含氧酸盐而从试样中分离出来,因此常用作分解矿石的熔剂。例如:Cr2O3 +3Na2O2 →2Na2CrO4 +Na2O
(1)上述反应中涉及元素Na与O,其离子半径的大小关系是_____________ 。
(2)Na2O2与SO2反应可能的化学方程式为:____________ ,书写的理由是:________________
(3)Na2O的物质类别属于____________ ,电子式为____________ 。
(4)Cr2O3发生铝热反应的化学方程式为_______ 。
(1)上述反应中涉及元素Na与O,其离子半径的大小关系是
(2)Na2O2与SO2反应可能的化学方程式为:
(3)Na2O的物质类别属于
(4)Cr2O3发生铝热反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“比较”是化学研究物质性质的基本方法之一,请运用比较法解答下列问题:已知在一定条件下,过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:
2Na2O2+2CO2=2Na2CO3+O2Na2O2+CO=Na2CO3
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式。
____________________________________________________ ,
____________________________________________________ ;
(2)通过比较可知:在氧化物中,当非金属元素处于____________ 价时,其氧化物与过氧化钠反应就有O2生成。
2Na2O2+2CO2=2Na2CO3+O2Na2O2+CO=Na2CO3
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式。
(2)通过比较可知:在氧化物中,当非金属元素处于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)Na2O2__________ (填“是”或“否”)属于碱性氧化物,Na2O2是______ 色固体粉末。向包有Na2O2固体的棉花上滴几滴水,棉花很快燃烧起来,原因是该反应有氧气生成且该反应为__________ (填”吸热”或者“放热”)反应;
(2)Na2O2作为在潜水艇和消防员呼吸面具中的供氧剂,写出其中一个反应的化学方程式_________ ,某潜水艇中有50人,若每人每小时消耗O2在标准状况下的体积为44.8L,假设所需要的O2全由Na2O2所提供,则每小时所需Na2O2的质量为________ kg。
(3)3.1gNa2O溶于水配成1L溶液,溶液中Na+离子物质的量浓度为________
(4)制备Fe(OH)3胶体:用洁净的烧杯取一定量蒸馏水,用酒精灯加热至沸腾,向烧杯中加入几滴饱和FeCl3溶液继续加热至液体呈透明的红褐色。
①写出制备Fe(OH)3胶体反应的离子方程式______________________________
②验证制得的分散系是胶体的方法为_________________________________
(2)Na2O2作为在潜水艇和消防员呼吸面具中的供氧剂,写出其中一个反应的化学方程式
(3)3.1gNa2O溶于水配成1L溶液,溶液中Na+离子物质的量浓度为
(4)制备Fe(OH)3胶体:用洁净的烧杯取一定量蒸馏水,用酒精灯加热至沸腾,向烧杯中加入几滴饱和FeCl3溶液继续加热至液体呈透明的红褐色。
①写出制备Fe(OH)3胶体反应的离子方程式
②验证制得的分散系是胶体的方法为
您最近一年使用:0次



