1 . 物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据如图所示,回答下列问题: 的化学式为
的化学式为___________ 。食品中添加适量的 ,可以起到
,可以起到___________ (填两点即可)作用;燃煤时为减少 的排放,可在煤中添加
的排放,可在煤中添加___________ (填名称)。
(2) 与
与 反应时,随着
反应时,随着 的浓度逐渐增大,化学反应速率的变化是
的浓度逐渐增大,化学反应速率的变化是___________ ; 的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为___________ 。
(3)欲制备 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是___________ (填序号)。
a. b.
b. c.
c. d.
d. 
(4)将 与
与 混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为
混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为___________ 。

 的化学式为
的化学式为 ,可以起到
,可以起到 的排放,可在煤中添加
的排放,可在煤中添加(2)
 与
与 反应时,随着
反应时,随着 的浓度逐渐增大,化学反应速率的变化是
的浓度逐渐增大,化学反应速率的变化是 的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为(3)欲制备
 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是a.
 b.
b. c.
c. d.
d. 
(4)将
 与
与 混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为
混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为
您最近半年使用:0次
2 . 下列操作不符合实验安全规范的是
| A.点燃氢气前,先验纯确定其纯净 |
| B.稀释浓硫酸时,将水加入浓硫酸中 |
| C.制备有毒气体时,在通风橱内进行 |
| D.闻气体气味时用手轻轻扇动,使少量气体飘进鼻孔 |
您最近半年使用:0次
名校
3 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,5.6L NO和5.6LO2混合后分子总数少于0.5NA |
| B.常温下,将56gFe放入足量浓硝酸中,充分反应,生成NO2气体为3NA(不考虑NO2变成N2O4) |
| C.0.4mol Fe与足量的S反应,转移的电子数为1.2NA |
| D.含2mol H2SO4的浓硫酸与64gCu共热,生成SO2分子数为NA |
您最近半年使用:0次
4 . 下列关于浓硫酸的说法正确的是
| A.浓硫酸使蓝色胆矾变白体现了脱水性 |
B.浓硫酸不能干燥 、HI、 、HI、 等强还原性化合物 等强还原性化合物 |
| C.蔗糖和浓硫酸的“黑面包”实验中,浓硫酸主要体现了脱水性和强氧化性 |
| D.浓硫酸和碳单质在加热条件下反应,反应中浓硫酸既体现出酸性,又体现出氧化性 |
您最近半年使用:0次
名校
解题方法
5 . (NH4)2SO4在一定条件下发生如下反应: ,将反应后的气体通入一定量的BaCl2溶液中,发现溶液中有白色沉淀生成,还有部分气体从溶液中逸出,检验发现从溶液中逸出的气体无色、无味,溶液中氯化钡恰好完全反应。下列说法正确的是
,将反应后的气体通入一定量的BaCl2溶液中,发现溶液中有白色沉淀生成,还有部分气体从溶液中逸出,检验发现从溶液中逸出的气体无色、无味,溶液中氯化钡恰好完全反应。下列说法正确的是
 ,将反应后的气体通入一定量的BaCl2溶液中,发现溶液中有白色沉淀生成,还有部分气体从溶液中逸出,检验发现从溶液中逸出的气体无色、无味,溶液中氯化钡恰好完全反应。下列说法正确的是
,将反应后的气体通入一定量的BaCl2溶液中,发现溶液中有白色沉淀生成,还有部分气体从溶液中逸出,检验发现从溶液中逸出的气体无色、无味,溶液中氯化钡恰好完全反应。下列说法正确的是A.生成的沉淀中既有BaSO4、又有BaSO3,且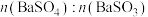 约为 约为 |
B.生成的沉淀中既有BaSO4、又有BaSO3,且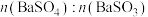 约为 约为 |
| C.因为弱酸不能制强酸,所以该实验中反应后气体通入BaCl2溶液中只有BaSO4沉淀 |
| D.从溶液中逸出的气体只有N2,最后留下溶液中溶质只有较多的NH4Cl |
您最近半年使用:0次
名校
解题方法
6 . 下列各组离子或分子在给定条件的溶液中可能大量共存的是
A.加入铝片有大量氢气产生的溶液中: 、 、 、 、 、 、 |
B.在0.1mol/L的盐酸中: 、 、 、 、 、 、 |
C.在强碱性溶液中: 、 、 、 、 、 、 |
D.碱性无色溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
名校
解题方法
7 . 下图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是
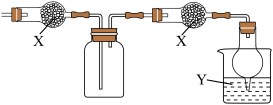
选项 | 试剂X | 收集气体 | 试剂Y |
A. | 碱石灰 | 氯化氢 | 水 |
B. | 碱石灰 | 氨气 | 水 |
C. | 五氧化二磷 | 二氧化硫 | 氢氧化钠溶液 |
D. | 氯化钙 | 一氧化氮 | 氢氧化钠溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
8 . 下列有关反应的离子方程式书写正确的是
A.氯气溶于水: |
B.过量 与“84”消毒液(有效成分NaClO)反应: 与“84”消毒液(有效成分NaClO)反应: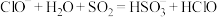 |
C.向 溶液中加入过量浓氨水: 溶液中加入过量浓氨水: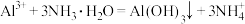 |
D. 通入酸性高锰酸钾溶液: 通入酸性高锰酸钾溶液: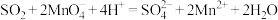 |
您最近半年使用:0次
名校
解题方法
9 . 化学促进了生活、生产、科研的发展,下列相关说法错误的是
| A.在葡萄酒中添加SO2作为抗氧化剂食品保鲜,SO2在保鲜时体现了氧化性 |
| B.华为Mate60手机高清镜头中使用的COC/COP(环状聚烯烃)是高分子化合物,也是混合物 |
| C.中国自主研发的首个5G微基站射频芯片的主要材料是Si |
| D.高铁动车的车厢厢体由不锈钢和铝合金制成,不锈钢和铝合金均属于金属材料 |
您最近半年使用:0次
解题方法
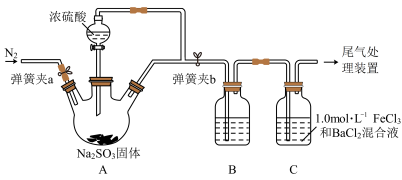
10 . 某同学设计了如图装置用于制取SO2,并验证SO2的部分性质,回答下列问题:___________ 。
(2)某同学为了检验装置中A、B两部分的气密性,进行的操作是关闭弹簧夹a、打开弹簧夹b,用酒精灯在三口烧瓶下微热,观察到B中长导管口有明显气泡现象,他判断气密性良好。你认为是否合理___________ (填“合理”或“不合理”)。
(3)实验前要在装置中鼓入N2,目的是___________ 。
(4)为了验证SO2是酸性氧化物,B中可选用的试剂是___________(填字母)。
(5)欲验证反应生成的气体SO2的还原性,则 B中试剂可选择下列中的___________。
(6)装置C中可观察到白色沉淀现象,SO2与FeCl3溶液反应的离子方程式为___________ 。
(7)为防止污染空气,则尾气处理的离子方程式为___________ 。
(2)某同学为了检验装置中A、B两部分的气密性,进行的操作是关闭弹簧夹a、打开弹簧夹b,用酒精灯在三口烧瓶下微热,观察到B中长导管口有明显气泡现象,他判断气密性良好。你认为是否合理
(3)实验前要在装置中鼓入N2,目的是
(4)为了验证SO2是酸性氧化物,B中可选用的试剂是___________(填字母)。
| A.无色酚酞溶液 | B.蓝色石蕊试剂 |
| C.红色品红溶液 | D.KI淀粉混合溶液 |
(5)欲验证反应生成的气体SO2的还原性,则 B中试剂可选择下列中的___________。
| A.酸性高酸钾溶液 | B.FeCl3溶液 |
| C.溴水 | D.Na2S 溶液 |
(6)装置C中可观察到白色沉淀现象,SO2与FeCl3溶液反应的离子方程式为
(7)为防止污染空气,则尾气处理的离子方程式为
您最近半年使用:0次



