名校
解题方法
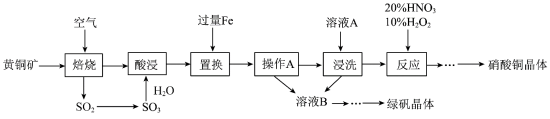
1 . 研究人员拟设计黄铜矿(主要含CuFeS2)制备硝酸铜和绿矾晶体的流程如下:
(1)CuFeS2中铁元素的化合价为___________ 价,已知“焙烧”生成SO2、CuO和Fe2O3,则其化学反应方程式为___________ 。
(2)“置换”步骤中发生的所有反应的离子方程式有___________ 、Fe+Cu2+=Fe2++Cu、Fe+2H+=Fe2++H2↑。
(3)流程中“操作 A”所需的玻璃仪器有_____________ 。
(4)“浸洗”步骤中加溶液A 的目的是_______________ 。
(5)“反应”步骤中,10%H2O2为氧化剂,20%HNO3提供H+,可以避免污染性气体的产生,写出该“反应”的离子方程式:___________ 。
(6)绿矾晶体(FeSO4·7H2O)在空气中极易变质; 验证绿矾晶体已变质的操作为_______________ 。
(1)CuFeS2中铁元素的化合价为
(2)“置换”步骤中发生的所有反应的离子方程式有
(3)流程中“操作 A”所需的玻璃仪器有
(4)“浸洗”步骤中加溶液A 的目的是
(5)“反应”步骤中,10%H2O2为氧化剂,20%HNO3提供H+,可以避免污染性气体的产生,写出该“反应”的离子方程式:
(6)绿矾晶体(FeSO4·7H2O)在空气中极易变质; 验证绿矾晶体已变质的操作为
您最近半年使用:0次
名校
解题方法
2 . 下列装置可以用于相应实验的是
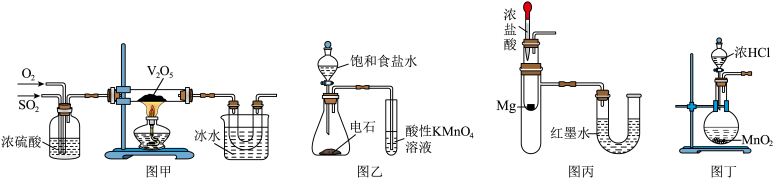
| A.图甲制取并收集SO3 | B.图乙检验乙炔具有还原性 |
| C.图丙中红墨水左高右低 | D.图丁装置制取Cl2 |
您最近半年使用:0次
7日内更新
|
396次组卷
|
2卷引用:2024届江西省南昌市第十九中学高三下学期模拟预测化学试题
3 . 根据实验事实能得出相应结论的是
A.在25℃和40℃测得0.1mol/L  溶液的pH分别为9.37和9.66。 溶液的pH分别为9.37和9.66。 的水解常数: 的水解常数: (40℃)> (40℃)> (25℃) (25℃) |
B. 在苯中的溶解度大于在水中。溶剂的极性:苯>水 在苯中的溶解度大于在水中。溶剂的极性:苯>水 |
C.将有机物X: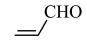 滴入溴的 滴入溴的 溶液中,溶液褪色。可以检验X中的碳碳双键 溶液中,溶液褪色。可以检验X中的碳碳双键 |
D.向溶液Y中滴加盐酸酸化的氯化钡溶液有白色沉淀生成。Y中一定含有 |
您最近半年使用:0次
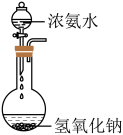
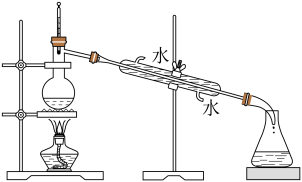
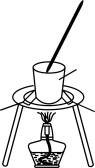
4 . 下列图示与对应的叙述相符或能达到相应目的的是
| |
| A.实验室快速制氨气 | B.提纯苯甲酸 |
|
|
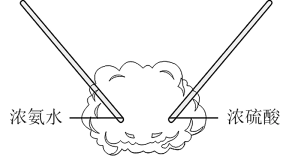
C.绿矾晶体制备 | D.浓氨水与浓硫酸反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
5 . 下列实验操作能达到实验目的的是
选项 | 实验操作 | 实验目的 |
A | 在对甲基苯酚中滴少量酸性 | 证明羟基具有还原性 |
B | 向紫色石蕊溶液中通入 | 验证 |
C | 在医用酒精中加小块钠 | 证明乙醇会与钠反应 |
D | 在AgCl浊液、AgI浊液中分别加入过量的同浓度浓氨水(白色沉淀溶解,黄色沉淀几乎不溶解) | 证明: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
6 . 由下列实验操作和现象,得出的结论正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向某补血口服液中滴加几滴酸性 溶液 溶液 | 酸性 溶液紫色褪去 溶液紫色褪去 | 该补血口服液中一定含有 |
| B | 将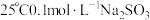 溶液加热到 溶液加热到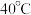 ,用传感器监测溶液 ,用传感器监测溶液 变化 变化 | 溶液的 逐渐减小 逐渐减小 | 温度升高, 水解平衡正向移动 水解平衡正向移动 |
| C | 向 溶液中通入少量 溶液中通入少量 ,然后再加入少量苯 ,然后再加入少量苯 | 有机层呈橙红色 | 氧化性: |
| D | 向两支装有等体积等浓度的双氧水的试管中分别加入 浓度均为 浓度均为 的 的 溶液和 溶液和 溶液 溶液 | 加入 溶液的试管产生气泡快 溶液的试管产生气泡快 | 加入 溶液时,双氧水分解反应的活化能较小 溶液时,双氧水分解反应的活化能较小 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . 实验室可以在 用浓硝酸在硝酸汞催化下氧化乙炔
用浓硝酸在硝酸汞催化下氧化乙炔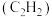 气体来制备草酸,主要装置如图所示。
气体来制备草酸,主要装置如图所示。错误 的是
 用浓硝酸在硝酸汞催化下氧化乙炔
用浓硝酸在硝酸汞催化下氧化乙炔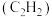 气体来制备草酸,主要装置如图所示。
气体来制备草酸,主要装置如图所示。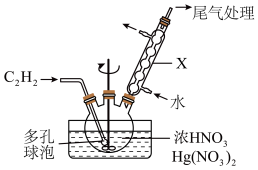
| A.多孔球泡可增加气体与溶液的接触面积 |
B.用电石制得的 中含有的 中含有的 杂质,应用 杂质,应用 溶液除去 溶液除去 |
| C.增大硝酸的质量分数,草酸的产率可能会下降 |
D.实验中会产生氮氧化物等污染性气体,可用 溶液吸收 溶液吸收 |
您最近半年使用:0次
解题方法
8 . 下列反应方程式书写不正确的是
A.Fe与过量的稀硝酸反应:Fe+4H++NO =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| B.用浓氨水检验氯气泄漏:8NH3+3Cl2=6NH4Cl+N2 |
C.实验室法制备氨气:2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O CaCl2+2NH3↑+2H2O |
D.向酸性KMnO4溶液中通入SO2溶液:2MnO +5SO2+4H+=2Mn2++5SO +5SO2+4H+=2Mn2++5SO +2H2O +2H2O |
您最近半年使用:0次
名校
9 . 下列实验操作或装置正确的是
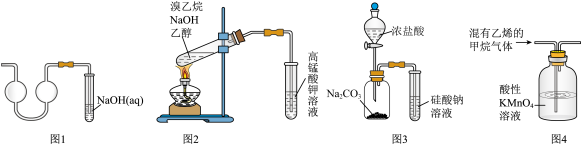
| A.利用图1所示装置吸收制取少量二氧化硫产生的尾气 |
| B.利用图2所示装置检验溴乙烷与NaOH醇溶液共热产生乙烯 |
C.利用图3所示装置证明 酸性强于硅酸 酸性强于硅酸 |
| D.利用图4所示装置可除去甲烷中的乙烯 |
您最近半年使用:0次
2024-04-28更新
|
349次组卷
|
2卷引用:江西省宜春市丰城中学2023-2024学年高二下学期4月期中考试化学试题
10 . 已知R为短周期主族元素,一种白色钠盐M的组成用通式 表示。为了探究R元素,进行如下实验:
表示。为了探究R元素,进行如下实验:
(1)若在M溶液中滴加 溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为
溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为__________ ,M的俗名是__________ 。
(2)若在M溶液中滴加 溶液,生成白色胶状物质,该白色胶状物质的化学式为
溶液,生成白色胶状物质,该白色胶状物质的化学式为______________ 。
(3)若将M溶液加入酸性 溶液中,酸性
溶液中,酸性 溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是
溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是__________ ,则M溶液和酸性 溶液反应使其溶液褪色的离子方程式为
溶液反应使其溶液褪色的离子方程式为________ ,其中还原剂是__________ 。
(4)若在M溶液中加入铜粉,无明显现象,滴加适量稀硫酸,铜粉溶解,溶液变蓝色,生成气体X,将X与单质Y通入足量水中恰好发生化合反应,则同温同压下X与Y的体积比为________ ,铜粉溶解的离子方程式为____________ ,工业上,氨催化氧化可制备X,其反应的化学方程式为__________ 。
 表示。为了探究R元素,进行如下实验:
表示。为了探究R元素,进行如下实验:(1)若在M溶液中滴加
 溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为
溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为(2)若在M溶液中滴加
 溶液,生成白色胶状物质,该白色胶状物质的化学式为
溶液,生成白色胶状物质,该白色胶状物质的化学式为(3)若将M溶液加入酸性
 溶液中,酸性
溶液中,酸性 溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是
溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是 溶液反应使其溶液褪色的离子方程式为
溶液反应使其溶液褪色的离子方程式为(4)若在M溶液中加入铜粉,无明显现象,滴加适量稀硫酸,铜粉溶解,溶液变蓝色,生成气体X,将X与单质Y通入足量水中恰好发生化合反应,则同温同压下X与Y的体积比为
您最近半年使用:0次

 至过量
至过量


