1 . 化学与生活密切相关,下列说法不正确的是
| A.聚氯乙烯可用于不粘锅内侧涂层 |
B.葡萄酒中加适量 起到抗氧化作用 起到抗氧化作用 |
| C.生石灰、食盐等腌制鸭蛋制得松花蛋,原因是蛋白质变性 |
D.内蒙古冬运会上运动员穿的发热服饰材料中的石墨烯与 互为同素异形体 互为同素异形体 |
您最近一年使用:0次
解题方法
2 . 下图为氮、硫及其部分化合物的价类二维图,有关说法正确的是
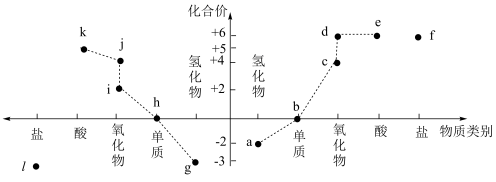
| A.g与e反应产物可以属于f或l | B.e的浓溶液不能干燥a、c、g、i |
| C.将k转化为j必须选用合适还原剂才能实现 | D.除f和l外,上述物质中是电解质的还有2种 |
您最近一年使用:0次
名校
解题方法
3 . 下列过程中的化学反应,相应的离子方程式正确的是
A.Ca(HCO3)2溶液中加入过量氨水: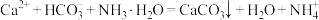 |
B.用漂白液吸收少量二氧化硫气体: |
C.NH4HSO4溶液中加入少量Ba(OH)2溶液: |
D.硫代硫酸钠(Na2S2O3)与稀硫酸反应: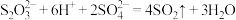 |
您最近一年使用:0次
名校
4 . 下列实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 在对甲基苯酚中滴少量酸性 溶液 溶液 | 证明羟基具有还原性 |
| B | 向紫色石蕊溶液中通入 至过量 至过量 | 验证 具有漂白性 具有漂白性 |
| C | 在医用酒精中加小块钠 | 证明乙醇会与钠反应 |
| D | 在AgCl浊液、AgI浊液中分别加入过量的同浓度浓氨水(白色沉淀溶解,黄色沉淀几乎不溶解) | 证明:Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-21更新
|
152次组卷
|
2卷引用:江西省部分学校2023-2024学年高三下学期二轮复习联考验收化学试卷
5 . 由下列实验操作及现象,能推出相应结论的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将镁条点燃,迅速伸入集满 的集气瓶中 的集气瓶中 | 集气瓶中产生大量白烟,并有黑色颗粒产生 |  具有氧化性 具有氧化性 |
| B | 向制备乙酸乙酯后剩余的反应液中加入碳酸钠溶液 | 有气泡产生 | 说明乙酸有剩余 |
| C | 向双氧水中滴加酸性 溶液 溶液 | 迅速有大量气泡生成 |  对 对 分解具有催化作用 分解具有催化作用 |
| D | 向某甲酸样品中先加入足量NaOH溶液,再做银镜反应实验 | 出现银镜 | 该甲酸样品中混有甲醛 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 高氯酸铜晶体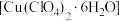 易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:
易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:
Ⅰ.称取12.5g 和9.6g
和9.6g ,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀
,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀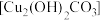 ;
;
Ⅱ.冷却,过滤,用少量蒸馏水洗涤沉淀2~3次;
Ⅲ.在沉淀中慢慢滴加70% 溶液,适度加热搅拌至不再产生气体;
溶液,适度加热搅拌至不再产生气体;
Ⅳ.过滤,得蓝色高氯酸铜溶液;
Ⅴ.在通风橱中蒸发至不再产生白雾,继续蒸发至有晶膜出现,冷却、结晶、过滤、洗涤,得蓝色晶体;
Ⅵ.60℃下,在烘箱中干燥2h,得16.695g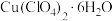 晶体。
晶体。
回答下列问题:
(1)“步骤Ⅰ”中研磨用到的仪器名称是________ ,“步骤Ⅴ”中蒸发需要用到下列仪器中的________ (填字母序号). 和
和 研细的目的是
研细的目的是________________ ,写出它们在溶液中反应生成 的离子方程式:
的离子方程式:________________ ,实际操作中 与
与 的物质的量之比大于
的物质的量之比大于 ,原因是
,原因是________________ 。
(3)“步骤Ⅱ”中检验沉淀是否洗净所需试剂为________ 。
(4)“步骤Ⅴ”在通风橱中进行的原因是________________ 。
(5)某温度下,高氯酸铜同时按以下两种方式分解:(A)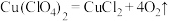 ;(B)
;(B)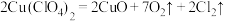 ,若测得
,若测得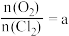 ,则按(A)式分解的高氯酸铜的质量分数为
,则按(A)式分解的高氯酸铜的质量分数为________ (用含a的代数式表示)。
(6)上述过程中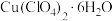 的产率为
的产率为________ 。
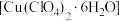 易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:
易溶于水,120℃开始分解,常用于生产电极和燃烧的催化剂等.实验室以硫酸铜为原料制备少量高氯酸铜晶体的步骤如下:Ⅰ.称取12.5g
 和9.6g
和9.6g ,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀
,混合研细后,投入100mL70~80℃热水,快速搅拌,静置得绿色沉淀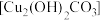 ;
;Ⅱ.冷却,过滤,用少量蒸馏水洗涤沉淀2~3次;
Ⅲ.在沉淀中慢慢滴加70%
 溶液,适度加热搅拌至不再产生气体;
溶液,适度加热搅拌至不再产生气体;Ⅳ.过滤,得蓝色高氯酸铜溶液;
Ⅴ.在通风橱中蒸发至不再产生白雾,继续蒸发至有晶膜出现,冷却、结晶、过滤、洗涤,得蓝色晶体;
Ⅵ.60℃下,在烘箱中干燥2h,得16.695g
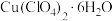 晶体。
晶体。回答下列问题:
(1)“步骤Ⅰ”中研磨用到的仪器名称是
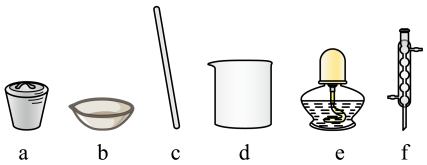
 和
和 研细的目的是
研细的目的是 的离子方程式:
的离子方程式: 与
与 的物质的量之比大于
的物质的量之比大于 ,原因是
,原因是(3)“步骤Ⅱ”中检验沉淀是否洗净所需试剂为
(4)“步骤Ⅴ”在通风橱中进行的原因是
(5)某温度下,高氯酸铜同时按以下两种方式分解:(A)
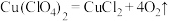 ;(B)
;(B)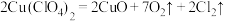 ,若测得
,若测得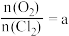 ,则按(A)式分解的高氯酸铜的质量分数为
,则按(A)式分解的高氯酸铜的质量分数为(6)上述过程中
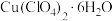 的产率为
的产率为
您最近一年使用:0次
2024-05-20更新
|
84次组卷
|
2卷引用:江西省部分重点中学2024届高三下学期第二次联考化学试题
7 . 化学中有很多化学思想,下列叙述符合化学思想的是
A. 的水溶液可以导电,所以 的水溶液可以导电,所以 是电解质,符合“分类”思想 是电解质,符合“分类”思想 |
B.由Fe与S反应生成FeS,可推知Cu与S反应可生成 ,符合“类比”思想 ,符合“类比”思想 |
| C.对工业生产硝酸产生的废气、废水进行严格处理,符合“绿色化学”思想 |
D. 溶于水的水解反应为 溶于水的水解反应为 ,符合“水解平衡”思想 ,符合“水解平衡”思想 |
您最近一年使用:0次
8 . 硫酸铁和硫酸亚铁均为重要的盐。实验室用废铁屑(含油污)制备 和
和 溶液,并进行相关探究。回答下列问题:
溶液,并进行相关探究。回答下列问题:
Ⅰ.制备0.01 mol⋅L
 溶液和0.04 mol⋅L
溶液和0.04 mol⋅L
 溶液。
溶液。
步骤一:将废铁屑(含油污)依次用热纯碱溶液、蒸馏水清洗后,加入足量 溶液,充分反应后过滤;
溶液,充分反应后过滤;
步骤二:向滤液中分批加入足量双氧水,充分反应后小心煮沸、冷至室温;
步骤三:标定所得 溶液浓度;
溶液浓度;
步骤四:配制100 mL 0.01 mol⋅L
 溶液;
溶液;
步骤五:取部分标定浓度后的 溶液,经转化后配制100 mL 0.04 mol⋅L
溶液,经转化后配制100 mL 0.04 mol⋅L
 溶液。
溶液。
(1)步骤一中用蒸馏水清洗的目的为___________ ;步骤二中,双氧水需足量并分批加入的原因为___________ 。
(2)步骤三标定 溶液浓度的操作:准确量取10.00 mL
溶液浓度的操作:准确量取10.00 mL  溶液于锥形瓶中,依次加入适当过量的
溶液于锥形瓶中,依次加入适当过量的 、适量的
、适量的 ,充分反应后用0.1000 mol⋅L
,充分反应后用0.1000 mol⋅L
 标准溶液滴定,达到滴定终点时消耗标准溶液的体积为20.00 mL(已知:Sn的常见化合价为+2、+4;该实验条件下
标准溶液滴定,达到滴定终点时消耗标准溶液的体积为20.00 mL(已知:Sn的常见化合价为+2、+4;该实验条件下 不与
不与 反应)。
反应)。
①向 溶液中加入
溶液中加入 反应的离子方程式为
反应的离子方程式为___________ ;加入适量 的作用为
的作用为___________ 。
② 溶液的物质的量浓度为
溶液的物质的量浓度为___________ 。
(3)制备0.01 mol⋅L
 溶液的实验中,如图所示仪器不需要使用的是
溶液的实验中,如图所示仪器不需要使用的是___________ (填仪器名称)。 与Ag生成
与Ag生成 和
和 的反应特点。
的反应特点。
提出猜想:上述反应为可逆反应。
验证猜想:取少量Ag粉,向其中加入0.01mol⋅L
 溶液,固体全部溶解;将0.01 mol⋅L
溶液,固体全部溶解;将0.01 mol⋅L
 溶液与0.04 mol⋅L
溶液与0.04 mol⋅L
 溶液等体积混合,产生灰黑色沉淀。
溶液等体积混合,产生灰黑色沉淀。
(4)验证猜想时,第二步实验中所加FeSO₄溶液过量的目的为___________ ;向所得灰黑色沉淀中加入适量浓硝酸,通过___________ (填实验现象),可证明灰黑色沉淀为Ag单质。
(5)实验结论:猜想___________ (填“成立”或“不成立”)。
 和
和 溶液,并进行相关探究。回答下列问题:
溶液,并进行相关探究。回答下列问题:Ⅰ.制备0.01 mol⋅L

 溶液和0.04 mol⋅L
溶液和0.04 mol⋅L
 溶液。
溶液。步骤一:将废铁屑(含油污)依次用热纯碱溶液、蒸馏水清洗后,加入足量
 溶液,充分反应后过滤;
溶液,充分反应后过滤;步骤二:向滤液中分批加入足量双氧水,充分反应后小心煮沸、冷至室温;
步骤三:标定所得
 溶液浓度;
溶液浓度;步骤四:配制100 mL 0.01 mol⋅L

 溶液;
溶液;步骤五:取部分标定浓度后的
 溶液,经转化后配制100 mL 0.04 mol⋅L
溶液,经转化后配制100 mL 0.04 mol⋅L
 溶液。
溶液。(1)步骤一中用蒸馏水清洗的目的为
(2)步骤三标定
 溶液浓度的操作:准确量取10.00 mL
溶液浓度的操作:准确量取10.00 mL  溶液于锥形瓶中,依次加入适当过量的
溶液于锥形瓶中,依次加入适当过量的 、适量的
、适量的 ,充分反应后用0.1000 mol⋅L
,充分反应后用0.1000 mol⋅L
 标准溶液滴定,达到滴定终点时消耗标准溶液的体积为20.00 mL(已知:Sn的常见化合价为+2、+4;该实验条件下
标准溶液滴定,达到滴定终点时消耗标准溶液的体积为20.00 mL(已知:Sn的常见化合价为+2、+4;该实验条件下 不与
不与 反应)。
反应)。①向
 溶液中加入
溶液中加入 反应的离子方程式为
反应的离子方程式为 的作用为
的作用为②
 溶液的物质的量浓度为
溶液的物质的量浓度为(3)制备0.01 mol⋅L

 溶液的实验中,如图所示仪器不需要使用的是
溶液的实验中,如图所示仪器不需要使用的是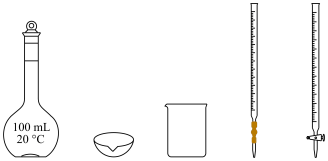
 与Ag生成
与Ag生成 和
和 的反应特点。
的反应特点。提出猜想:上述反应为可逆反应。
验证猜想:取少量Ag粉,向其中加入0.01mol⋅L

 溶液,固体全部溶解;将0.01 mol⋅L
溶液,固体全部溶解;将0.01 mol⋅L
 溶液与0.04 mol⋅L
溶液与0.04 mol⋅L
 溶液等体积混合,产生灰黑色沉淀。
溶液等体积混合,产生灰黑色沉淀。(4)验证猜想时,第二步实验中所加FeSO₄溶液过量的目的为
(5)实验结论:猜想
您最近一年使用:0次
9 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 实验操作和现象 | 结论 | |
| A | 用pH试纸测得0.1 mol·L 的 的 溶液的 溶液的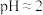 |  |
| B | 向某溶液中滴加足量稀盐酸,无沉淀生成,再滴入 溶液,产生白色沉淀 溶液,产生白色沉淀 | 该溶液中一定含 |
| C | 取少量丙烯醛于试管中,滴加溴水,溴水褪色 | 该有机物中含有碳碳双键 |
| D | 向同浓度的NaCl和 的稀溶液中滴加 的稀溶液中滴加 溶液,先出现白色沉淀,后出现砖红色沉淀。 溶液,先出现白色沉淀,后出现砖红色沉淀。 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 物质的性质决定用途,下列两者对应关系正确的是
| 选项 | 性质 | 用途 |
| A |  具有漂白性 具有漂白性 | 用来漂白纸浆、丝、毛、草帽等 |
| B |  易溶于水 易溶于水 | 用作净水剂 |
| C | 石墨质软 | 用作电极材料 |
| D |  具有强氧化性 具有强氧化性 | 用作供氧剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



