解题方法
1 . 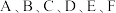 是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐
是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐 与
与 同主族,且与
同主族,且与 同周期;
同周期; 元素的最外层电子数是其次外层电子数的
元素的最外层电子数是其次外层电子数的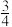 倍,
倍,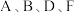 这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.
这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物. 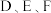 三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:
三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:
(1)写出题中 所代表的元素名称
所代表的元素名称_________ ,指出 所代表的元素在周期表中的位置
所代表的元素在周期表中的位置_________________________ 。
(2)写出 两种元素形成的原子个数比为
两种元素形成的原子个数比为 的物质的电子式为
的物质的电子式为_________________ , 两种元素各自形成的简单离子大小为
两种元素各自形成的简单离子大小为_________________ 
_________________ (写出相应离子符号)
(3)可以验证 和
和 两种元素非金属性强弱的结论是(填编号)
两种元素非金属性强弱的结论是(填编号)_____________ 。
①比较这两种元素常见单质的熔点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
(4)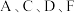 四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为
四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为_____________ 、_____________ ,这两种酸式盐相互反应的离子方程式为___________________ 。
(5) 间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为________________________________ 。
(6)写出 的单质和D的最高价氧化物的水化物间反应化学方程式:
的单质和D的最高价氧化物的水化物间反应化学方程式:_____________________ 。
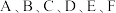 是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐
是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐 与
与 同主族,且与
同主族,且与 同周期;
同周期; 元素的最外层电子数是其次外层电子数的
元素的最外层电子数是其次外层电子数的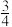 倍,
倍,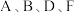 这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.
这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物. 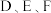 三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:
三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:(1)写出题中
 所代表的元素名称
所代表的元素名称 所代表的元素在周期表中的位置
所代表的元素在周期表中的位置(2)写出
 两种元素形成的原子个数比为
两种元素形成的原子个数比为 的物质的电子式为
的物质的电子式为 两种元素各自形成的简单离子大小为
两种元素各自形成的简单离子大小为
(3)可以验证
 和
和 两种元素非金属性强弱的结论是(填编号)
两种元素非金属性强弱的结论是(填编号)①比较这两种元素常见单质的熔点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
(4)
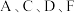 四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为
四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为(5)
 间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为(6)写出
 的单质和D的最高价氧化物的水化物间反应化学方程式:
的单质和D的最高价氧化物的水化物间反应化学方程式:
您最近半年使用:0次
2 . 回答下列问题
(1)浓硫酸是重要的化工原料,有其特殊的性质,某实验小组用如图所示的装置探究铜与浓硫酸的反应.___________ ,该反应中浓硫酸表现_________ 性;
②用可抽动铜丝替代铜片的优点是__________ ;
③若用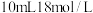 的浓硫酸与足量的铜反应,得到
的浓硫酸与足量的铜反应,得到 的质量范围为
的质量范围为_________ 。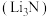 是一种快离子导体,导电率高,遇水剧烈反应生成氢氧化锂和氨气,实验室可用上图装置制备氮化锂.(已知:
是一种快离子导体,导电率高,遇水剧烈反应生成氢氧化锂和氨气,实验室可用上图装置制备氮化锂.(已知: 与
与 在加热条件下反应生成氮气)
在加热条件下反应生成氮气)
①写出 与水反应的化学方程式
与水反应的化学方程式___________ ;
②开始实验时,应该先点燃_____ (填“A”或“C”)处酒精灯;
③实验结束后,发现产品中混有少量 ,产生该杂质的原因可能为
,产生该杂质的原因可能为________ ;
④测 的纯度:取
的纯度:取 粗产品于试管中,向试管内加入少量的水,待固体完全溶解后,加热反应后的液体,将产生的气体用碱石灰干燥后,通入足量浓硫酸中,最终浓硫酸增重
粗产品于试管中,向试管内加入少量的水,待固体完全溶解后,加热反应后的液体,将产生的气体用碱石灰干燥后,通入足量浓硫酸中,最终浓硫酸增重 ,则产品中
,则产品中 的百分含量为
的百分含量为________ (保留三位有效数字)。
(1)浓硫酸是重要的化工原料,有其特殊的性质,某实验小组用如图所示的装置探究铜与浓硫酸的反应.
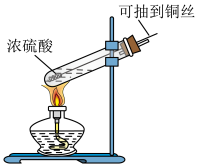
②用可抽动铜丝替代铜片的优点是
③若用
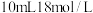 的浓硫酸与足量的铜反应,得到
的浓硫酸与足量的铜反应,得到 的质量范围为
的质量范围为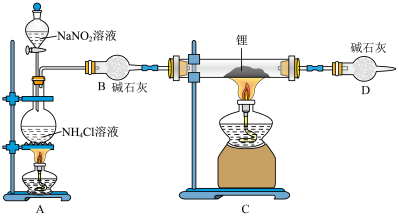
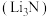 是一种快离子导体,导电率高,遇水剧烈反应生成氢氧化锂和氨气,实验室可用上图装置制备氮化锂.(已知:
是一种快离子导体,导电率高,遇水剧烈反应生成氢氧化锂和氨气,实验室可用上图装置制备氮化锂.(已知: 与
与 在加热条件下反应生成氮气)
在加热条件下反应生成氮气)①写出
 与水反应的化学方程式
与水反应的化学方程式②开始实验时,应该先点燃
③实验结束后,发现产品中混有少量
 ,产生该杂质的原因可能为
,产生该杂质的原因可能为④测
 的纯度:取
的纯度:取 粗产品于试管中,向试管内加入少量的水,待固体完全溶解后,加热反应后的液体,将产生的气体用碱石灰干燥后,通入足量浓硫酸中,最终浓硫酸增重
粗产品于试管中,向试管内加入少量的水,待固体完全溶解后,加热反应后的液体,将产生的气体用碱石灰干燥后,通入足量浓硫酸中,最终浓硫酸增重 ,则产品中
,则产品中 的百分含量为
的百分含量为
您最近半年使用:0次
解题方法
3 . 为控制污染,工业上可以用 酸化的
酸化的 溶液吸收废气中的
溶液吸收废气中的 ,下列说法中不正确的是
,下列说法中不正确的是
 酸化的
酸化的 溶液吸收废气中的
溶液吸收废气中的 ,下列说法中不正确的是
,下列说法中不正确的是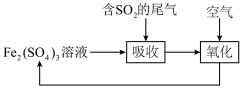
A.“吸收”过程中的离子反应方程式为: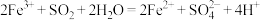 |
B.“氧化”过程中,可将空气换成 |
C. 可以循环使用 可以循环使用 |
D.吸收 含量为 含量为 (体积分数)的 (体积分数)的 的废气,至少需要通入相同条件下 的废气,至少需要通入相同条件下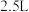 的空气(假设空气中 的空气(假设空气中 的体积分数为 的体积分数为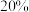 ) ) |
您最近半年使用:0次
4 . “类推”是化学学习常用方法,下列“类推”合理的是
A. 通入 通入 溶液中不产生白色沉淀, 溶液中不产生白色沉淀, 通入 通入 溶液中也不会产生白色沉淀 溶液中也不会产生白色沉淀 |
B. 中通入 中通入 有 有 生成, 生成, 中通入 中通入 也有 也有 生成 生成 |
C.C在足量 中燃烧生成最高价氧化物 中燃烧生成最高价氧化物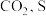 在足量 在足量 中燃烧也生成最高价氧化物 中燃烧也生成最高价氧化物 |
D. 难溶于水, 难溶于水, 也难溶于水 也难溶于水 |
您最近半年使用:0次
解题方法
5 . 下列离子方程式书写正确的是
A.氢氧化钡溶液与硫酸铜溶液混合: |
B.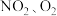 混合通入 混合通入 溶液中: 溶液中: |
C. 溶液中通入 溶液中通入 ,证明非金属性 ,证明非金属性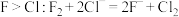 |
D.漂白粉溶液中通入少量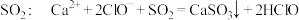 |
您最近半年使用:0次
解题方法
6 . 化学与人类社会的生活、生产密切相关,下列说法中不正确的是
A. 有毒,但可用作食品添加剂 有毒,但可用作食品添加剂 | B.合成氨反应属于人工固氮 |
C.向燃煤中加入少量生石灰可以减少 的排放 的排放 | D.将等体积的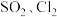 混合通入品红溶液,漂白效果比单独通入 混合通入品红溶液,漂白效果比单独通入 或 或 更好 更好 |
您最近半年使用:0次
名校
解题方法
7 . 硫酸铵为无色结晶或白色颗粒,无气味,溶于水,不溶于乙醇和丙酮。其在一定温度下分解的化学方程式为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.将分解产生的混合气体,通到酸性 溶液中,涉及氧化还原反应的离子方程式为 溶液中,涉及氧化还原反应的离子方程式为 |
B.将分解产生的混合气体,通到 溶液中不能产生白色沉淀 溶液中不能产生白色沉淀 |
C.将分解产生的混合气体,用足量的浓硫酸充分吸收后,可以收集到纯净的 |
D.将分解产生的混合气体,用水充分吸收,生成物中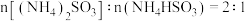 |
您最近半年使用:0次
名校
解题方法
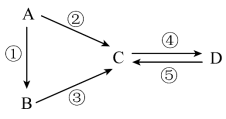
8 . A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:___________ 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出反应③的化学方程式:___________ 。
(3)若C是一种强碱溶液,焰色试验火焰为黄色。写出反应②的离子方程式:___________ 。
(4)若A是太阳能电池用的光伏材料,B是A的氧化物,写出用B制备A的化学方程式___________ 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出反应③的化学方程式:
(3)若C是一种强碱溶液,焰色试验火焰为黄色。写出反应②的离子方程式:
(4)若A是太阳能电池用的光伏材料,B是A的氧化物,写出用B制备A的化学方程式
您最近半年使用:0次
名校
9 . 根据实验操作、现象,所得结论错误的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将SO2分别通入品红的乙醇溶液和品红的水溶液 | 品红的乙醇溶液不褪色,品红的水溶液慢慢褪色 | 使品红褪色的不是SO2,而是SO2与水反应后的产物 |
| B | 将CO通过装有Fe2O3的硬质玻璃管,并对玻璃管加热 | 将所得产物溶于稀盐酸,再滴加KSCN溶液,溶液不变色 | Fe2O3完全被CO还原 |
| C | 以K2CrO4为指示剂,用AgNO3标准溶液滴定溶液中的Br- | 先出现浅黄色沉淀,后出现砖红色沉淀 | 无法确定Ksp(AgBr)和Ksp(Ag2CrO4)的大小 |
| D | 向淀粉溶液中加入适量稀硫酸,水浴加热。冷却至室温后加入NaOH溶液调至碱性,再加入新制氢氧化铜悬浊液,加热 | 试管中出现砖红色沉淀 | 淀粉发生了水解 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向某溶液中滴加盐酸酸化的 溶液,产生白色沉淀 溶液,产生白色沉淀 | 该溶液中不一定含有 |
B | 向浓硝酸中插入红热的木炭,产生红棕色气体 | 红棕色的 一定是由木炭和浓硝酸反应生成的 一定是由木炭和浓硝酸反应生成的 |
C | 向某盐溶液中加入NaOH溶液,将湿润的红色石蕊试纸靠近试管口,试纸不变蓝 | 该溶液中一定不含 |
D | 常温下将铁片浸入足量的浓硫酸中,铁片不溶解 | 常温下铁与浓硫酸不反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



