1 . 通过下列实验操作和现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向2mL   溶液中加入5mL 溶液中加入5mL  NaOH溶液,出现白色沉淀后,继续滴入几滴浓 NaOH溶液,出现白色沉淀后,继续滴入几滴浓 溶液,静置 溶液,静置 | 出现红褐色沉淀 | 同温下,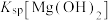 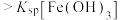 |
| B | 向某溶液中先滴加 溶液,后滴加稀盐酸 溶液,后滴加稀盐酸 | 产生白色沉淀,且沉淀不溶解 | 原溶液中一定含有 |
| C | 分别向等物质的量浓度、等体积的KCl和KI溶液中,滴加2滴稀 溶液,充分振荡 溶液,充分振荡 | KCl溶液中无白色沉淀,KI溶液中有黄色沉淀 | 结合 的能力: 的能力: |
| D | 在淀粉溶液中滴入稀硫酸,加热一段时间,冷却后加入氢氧化钠溶液至溶液呈碱性,再滴加碘水 | 溶液未变蓝色 | 证明淀粉水解完全 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 某单质A经下图所示过程可转化为D,D为强酸或强碱,则单质A不可能为
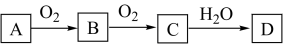
| A.N2 | B.Na | C.C | D.S |
您最近一年使用:0次
3 . 某兴趣小组对FeSO4的一些性质进行探究实验。回答下列问题:
(1)在试管中加入少量FeSO4样品,加水溶解,滴加KSCN溶液,溶液逐渐变_____ 色,说明样品已变质。同学甲认为若要使变质的FeSO4溶液复原,可以向溶液中加入过量的Fe粉,发生反应的离子方程式为______________ 。
(2)已知FeSO4的分解产物中含有SO2和SO3。将纯净FeSO4和有关试剂放入如图所示的装置,打开K1和K2,缓缓通入N2,加热,实验后反应管中残留固体为红棕色粉末。________________ 。
②装置C中盛放的溶液为________ ;装置D中盛放的溶液为________ (填标号)。
A.品红 B.NaOH C.BaCl2 D.浓H2SO4
③盛有NaOH溶液的装置的作用是_____________ 。
④实验时装置D中除有气泡冒出外,还可观察到的实验现象为_____________ 。
(1)在试管中加入少量FeSO4样品,加水溶解,滴加KSCN溶液,溶液逐渐变
(2)已知FeSO4的分解产物中含有SO2和SO3。将纯净FeSO4和有关试剂放入如图所示的装置,打开K1和K2,缓缓通入N2,加热,实验后反应管中残留固体为红棕色粉末。

②装置C中盛放的溶液为
A.品红 B.NaOH C.BaCl2 D.浓H2SO4
③盛有NaOH溶液的装置的作用是
④实验时装置D中除有气泡冒出外,还可观察到的实验现象为
您最近一年使用:0次
名校
解题方法
4 . 表示下列反应的离子方程式中,错误的是
A.SO2使酸性KMnO4溶液褪色: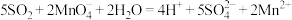 |
B.往NH4HCO3溶液中滴加足量烧碱溶液: |
C.用CuSO4溶液吸收H2S尾气: |
D.铜与足量稀硝酸反应: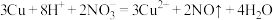 |
您最近一年使用:0次
5 . 硫代硫酸钠( )又名次亚硫酸钠、大苏打、海波,主要用于照相业作定影剂,某学习小组用如图装置制备硫代硫酸钠。
)又名次亚硫酸钠、大苏打、海波,主要用于照相业作定影剂,某学习小组用如图装置制备硫代硫酸钠。
①“绿矾”是指 ,高温受热可完全分解得红棕色固体和气体混合物;
,高温受热可完全分解得红棕色固体和气体混合物;
② 熔点-75.5℃,沸点-10℃;
熔点-75.5℃,沸点-10℃; 熔点16.8℃,沸点44.8℃
熔点16.8℃,沸点44.8℃
③硫代硫酸钠( )具有还原性,受热、遇酸易分解。
)具有还原性,受热、遇酸易分解。
请回答下列问题:
Ⅰ.制取硫代硫酸钠( )
)
(1)A装置中发生反应的化学方程式为___________________ 。
(2)检查装置气密性,加入药品。 和
和 混合溶液用煮沸过的蒸馏水配制,煮沸的目的是
混合溶液用煮沸过的蒸馏水配制,煮沸的目的是_______________ ;B装置的作用是_________________ 。
(3)从锥形瓶中得到 晶体需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的原因是
晶体需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的原因是_______________ 。
(4)将一定量的绿矾在500℃时隔绝空气加热一段时间后检验其固体产物,请设计实验证明:此固体产物不含二价铁:__________________ 。
Ⅱ.探究 的性质
的性质
为探究 的性质,小组将装置C换成钡盐溶液,并先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入
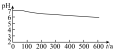
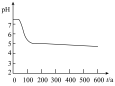
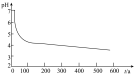
的性质,小组将装置C换成钡盐溶液,并先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入 流速一致。四次实验分别得到如表pH—t图:
流速一致。四次实验分别得到如表pH—t图:
(5)分析pH—t图,写出②中发生反应的离子方程式___________________________ ,上述四次实验中有白色沉淀生成的是__________ (填编号)。
 )又名次亚硫酸钠、大苏打、海波,主要用于照相业作定影剂,某学习小组用如图装置制备硫代硫酸钠。
)又名次亚硫酸钠、大苏打、海波,主要用于照相业作定影剂,某学习小组用如图装置制备硫代硫酸钠。
①“绿矾”是指
 ,高温受热可完全分解得红棕色固体和气体混合物;
,高温受热可完全分解得红棕色固体和气体混合物;②
 熔点-75.5℃,沸点-10℃;
熔点-75.5℃,沸点-10℃; 熔点16.8℃,沸点44.8℃
熔点16.8℃,沸点44.8℃③硫代硫酸钠(
 )具有还原性,受热、遇酸易分解。
)具有还原性,受热、遇酸易分解。请回答下列问题:
Ⅰ.制取硫代硫酸钠(
 )
)(1)A装置中发生反应的化学方程式为
(2)检查装置气密性,加入药品。
 和
和 混合溶液用煮沸过的蒸馏水配制,煮沸的目的是
混合溶液用煮沸过的蒸馏水配制,煮沸的目的是(3)从锥形瓶中得到
 晶体需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的原因是
晶体需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的原因是(4)将一定量的绿矾在500℃时隔绝空气加热一段时间后检验其固体产物,请设计实验证明:此固体产物不含二价铁:
Ⅱ.探究
 的性质
的性质为探究
 的性质,小组将装置C换成钡盐溶液,并先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入
的性质,小组将装置C换成钡盐溶液,并先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入 流速一致。四次实验分别得到如表pH—t图:
流速一致。四次实验分别得到如表pH—t图: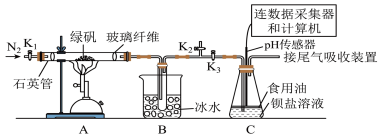
①已煮沸的 (aq) (aq) | ②未煮沸的 (aq) (aq) | ③已煮沸的 (aq) (aq) | ④未煮沸的 (aq) (aq) |
|
|
|
|
(5)分析pH—t图,写出②中发生反应的离子方程式
您最近一年使用:0次
解题方法
6 . 实验室用硫化碱法制备Na2S2O3·5H2O的实验装置如下图所示(夹持装置略)。可观察到装置②溶液中先析出黄色固体,其量先增多后又减少,当溶液的pH达到7左右时,溶液接近无色,说明反应已完成。下列有关实验说法错误的是

| A.装置③的作用是用于检验②中SO2是否被充分吸收 |
| B.为了使SO2在装置②中充分吸收,可以减慢SO2的流速 |
| C.装置①中反应的化学方程式为:H2SO4+Na2S2O3=Na2SO4+SO2↑+H2O |
| D.通过高温蒸发结晶可直接得到产品Na2S2O3·5H2O |
您最近一年使用:0次
名校
7 . 物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图所示是硫及其部分化合物的“价类二维图”,根据图示回答下列问题:___________ 。
(2)足量B通入品红溶液中,溶液褪色,体现了B的___________ 性;足量B通入溴水,溶液褪色,体现了B的___________ 性;足量B通入氢硫酸溶液,有淡黄色的固体生成,体现了B的___________ 性。
(3)气体A和B,不能用D的浓溶液干燥的气体是___________ (填A或B化学式),它与D的浓溶液反应有淡黄色的固体生成,请写出该反应的化学方程式___________ 。
(4)要实现 的转化,可选用下列试剂中的___________(填字母)。
的转化,可选用下列试剂中的___________(填字母)。
(5) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的方法
溶液是否变质的方法___________ 。

(2)足量B通入品红溶液中,溶液褪色,体现了B的
(3)气体A和B,不能用D的浓溶液干燥的气体是
(4)要实现
 的转化,可选用下列试剂中的___________(填字母)。
的转化,可选用下列试剂中的___________(填字母)。A. | B. | C. | D. |
(5)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的方法
溶液是否变质的方法
您最近一年使用:0次
8 . 下列实验操作或做法正确且能达到目的的是
| 选项 | 实验操作或做法 | 目的 |
| A | 向2 mL0.1 mol/LNa2S溶液中滴加0.1 mol/LZnSO4溶液至不再有沉淀产生,再滴加几滴0.1 mol/LCuSO4溶液,出现黑色沉淀 | 验证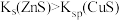 |
| B | 向各盛有5 mLH2O2溶液的两支试管中分别滴入2滴0.1 mol/L的FeCl3溶液和0.1 mol/L的CuSO4溶液 | 比较Fe3+与Cu2+对H2O2分解的催化效果 |
| C | 向盛有淀粉溶液的试管中加入少量稀硫酸,加热,再滴加几滴银氨溶液,水浴加热 | 证明淀粉已发生水解 |
| D | 先用稀硝酸酸化待测液,再滴加BaCl2溶液,生成白色沉淀 | 检验溶液中是否含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列离子方程式书写错误的是
A.碳酸氢钠溶液与硫酸氢钠溶液反应: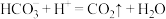 |
B. 通入 通入 溶液中: 溶液中: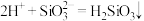 |
C. 通入氯水中: 通入氯水中: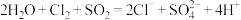 |
D. 通入过量氨水中: 通入过量氨水中: |
您最近一年使用:0次
2024-04-21更新
|
394次组卷
|
4卷引用:广西壮族自治区百所名校2023-2024学年高一下学期3月联合考试化学试题
名校
解题方法
10 . 下列离子方程式书写正确的是
A.向漂白粉溶液中通入少量 : :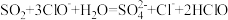 |
B.Fe粉和少量稀硝酸反应: |
C. 溶液与过量 溶液与过量 溶液反应: 溶液反应: |
D.饱和 溶液中通入过量 溶液中通入过量 : : |
您最近一年使用:0次