名校
1 . 某实验小组以BaS溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:
步骤1:制备
按如图所示装置进行实验,得到 溶液,经一系列步骤获得
溶液,经一系列步骤获得 产品。
产品。
步骤2:测定产品中 的含量
的含量
①称取产品1.0000g,用100mL水溶解、酸化、加热至近沸;
②在不断搅拌下,向①所得溶液中逐滴加入热的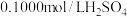 溶液,
溶液,
③沉淀完全后,经陈化、过滤、洗涤、烘干至恒重等步骤,称得白色固体质量为0.9320g。
(1)装置a的名称是___________ ,装置b中发生反应的化学方程式为___________ 。
(2)装置c的作用是___________ ,装置e中可选用的试剂是___________ (填字母)。
A.NaOH溶液 B.饱和食盐水 C.石灰乳 D.浓硫酸
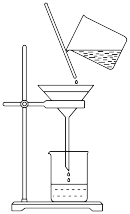
(3)如图过滤操作中不规范的有___________ 处;过滤后,洗涤沉淀的方法是___________ 。___________ 次。
(5)产品中 的质量分数为
的质量分数为___________ (保留三位有效数字)。
 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:步骤1:制备

按如图所示装置进行实验,得到
 溶液,经一系列步骤获得
溶液,经一系列步骤获得 产品。
产品。步骤2:测定产品中
 的含量
的含量①称取产品1.0000g,用100mL水溶解、酸化、加热至近沸;
②在不断搅拌下,向①所得溶液中逐滴加入热的
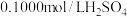 溶液,
溶液,③沉淀完全后,经陈化、过滤、洗涤、烘干至恒重等步骤,称得白色固体质量为0.9320g。
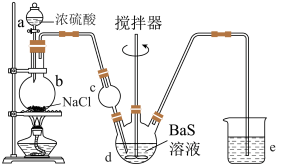
(1)装置a的名称是
(2)装置c的作用是
A.NaOH溶液 B.饱和食盐水 C.石灰乳 D.浓硫酸
(3)如图过滤操作中不规范的有
(5)产品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2023-11-18更新
|
820次组卷
|
7卷引用:2024届广西普通高中学业水平选择性考试高三下学期模拟考试化学试卷
2024届广西普通高中学业水平选择性考试高三下学期模拟考试化学试卷四川省资阳市2024届高三上学期第一次诊断性考试理综化学试题江西省赣州市全南中学2023-2024学年高三上学期11月期中考试化学试题(已下线)实验探究题(已下线)T27-实验综合题(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)T15-实验综合题
2 . 如图是硫酸试剂标签上的部分内容,据此分析下列说法正确的是
| 硫酸化学纯(CP)(500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84 g•cm-3 质量分数:98% |
| A.取50 mL该硫酸,其物质的量浓度为1.84 mol·L-1 |
| B.稀释该硫酸时应将水加入硫酸中,并迅速搅拌 |
| C.该硫酸具有吸水性,可干燥HCl、NH3、Cl2等气体 |
| D.常温下该硫酸可用铁质或铝质容器储存 |
您最近一年使用:0次
2022-09-02更新
|
304次组卷
|
3卷引用:广西桂林市兴安县第三中学2021-2022学年高一下学期期中考试化学试题
3 . 综合利用海水可以制备工业溴、纯碱等物质,其流程示意图如下:

(1)请写出海水淡化的两种方法:___________ 、___________ 。
(2)提取溴的过程经过2次用 使“
使“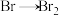 ”,其目的是
”,其目的是___________ ,所发生的离子反应方程式为___________ 。
(3)用 水溶液吸收
水溶液吸收 ,使之转化成
,使之转化成 ,有关反应方程式为
,有关反应方程式为___________ ;从氧化还原角度分析,下列3种物质也能用于吸收 的是
的是___________ (填正确选项序号)。
① ②
② 溶液 ③
溶液 ③ 溶液
溶液
(4)X溶液中的主要阳离子是 和
和___________ (填离子符号)。
(5)在饱和 溶液中先通
溶液中先通 后通
后通 的目的是
的目的是___________ 。
(6)产品纯碱中含有少量碳酸氢钠。若煅烧前固体碳酸氢钠的质量为 ,煅烧后所得纯碱产品的质量为
,煅烧后所得纯碱产品的质量为 。则产品中纯碱的质量分数为
。则产品中纯碱的质量分数为___________ (用含相关字母的代数式表示)。

(1)请写出海水淡化的两种方法:
(2)提取溴的过程经过2次用
 使“
使“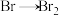 ”,其目的是
”,其目的是(3)用
 水溶液吸收
水溶液吸收 ,使之转化成
,使之转化成 ,有关反应方程式为
,有关反应方程式为 的是
的是①
 ②
② 溶液 ③
溶液 ③ 溶液
溶液(4)X溶液中的主要阳离子是
 和
和(5)在饱和
 溶液中先通
溶液中先通 后通
后通 的目的是
的目的是(6)产品纯碱中含有少量碳酸氢钠。若煅烧前固体碳酸氢钠的质量为
 ,煅烧后所得纯碱产品的质量为
,煅烧后所得纯碱产品的质量为 。则产品中纯碱的质量分数为
。则产品中纯碱的质量分数为
您最近一年使用:0次
解题方法
4 . 某工厂使用的煤中硫的质量分数为0.64%,该工厂每天燃烧这种煤100 t,试计算:
(1)如果煤中的硫全部转化为 ,该厂每天产生
,该厂每天产生 的质量及这些
的质量及这些 在标准状况下的体积
在标准状况下的体积_______________ ;
(2)如果把产生的 全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量
全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量__________________ 。
(1)如果煤中的硫全部转化为
 ,该厂每天产生
,该厂每天产生 的质量及这些
的质量及这些 在标准状况下的体积
在标准状况下的体积(2)如果把产生的
 全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量
全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量
您最近一年使用:0次
2021-12-02更新
|
938次组卷
|
2卷引用:广西钦州市第四中学2022-2023学年高一下学期2月考试化学试题
5 . 某工厂以黄铁矿(主要成分为 )为原料,采用接触氧化法生产
)为原料,采用接触氧化法生产 的流程如图甲所示。
的流程如图甲所示。

(1) 中S元素的化合价为
中S元素的化合价为___________ 。
(2)在“接触室”制备 的反应化学方程式为
的反应化学方程式为___________ 。吸收 时宜选用的试剂为
时宜选用的试剂为___________ (填“水”或“98.3%的浓硫酸”)。
(3)实验室常用浓硫酸来干燥某些气体,利用了浓硫酸的___________ 性。
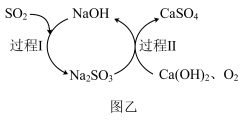
(4)生产过程可用双碱法脱硫处理废气中的 ,原理如图乙所示,其中可循环使用的物质是
,原理如图乙所示,其中可循环使用的物质是___________ ,双碱法脱硫的总反应方程式为___________ 。
(5)为测定空气中 的含量,甲同学将空气样品经过管道通入密闭容器中的
的含量,甲同学将空气样品经过管道通入密闭容器中的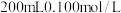 的酸性
的酸性 溶液。已知
溶液。已知 与该溶液反应的离子方程式为:
与该溶液反应的离子方程式为: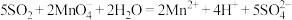 。若管道中空气流量为aL/min,经过b分钟溶液恰好褪色,则该空气样品中
。若管道中空气流量为aL/min,经过b分钟溶液恰好褪色,则该空气样品中 的含量为
的含量为___________ g/L。
 )为原料,采用接触氧化法生产
)为原料,采用接触氧化法生产 的流程如图甲所示。
的流程如图甲所示。
(1)
 中S元素的化合价为
中S元素的化合价为(2)在“接触室”制备
 的反应化学方程式为
的反应化学方程式为 时宜选用的试剂为
时宜选用的试剂为(3)实验室常用浓硫酸来干燥某些气体,利用了浓硫酸的
(4)生产过程可用双碱法脱硫处理废气中的
 ,原理如图乙所示,其中可循环使用的物质是
,原理如图乙所示,其中可循环使用的物质是
(5)为测定空气中
 的含量,甲同学将空气样品经过管道通入密闭容器中的
的含量,甲同学将空气样品经过管道通入密闭容器中的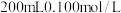 的酸性
的酸性 溶液。已知
溶液。已知 与该溶液反应的离子方程式为:
与该溶液反应的离子方程式为: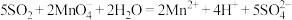 。若管道中空气流量为aL/min,经过b分钟溶液恰好褪色,则该空气样品中
。若管道中空气流量为aL/min,经过b分钟溶液恰好褪色,则该空气样品中 的含量为
的含量为
您最近一年使用:0次
解题方法
6 . 化学物质与食品安全息息相关。下列说法错误的是
| A.过量使用食品添加剂不会对人体造成危害 |
| B.二氧化硫可用于葡萄酒中作抗氧化剂 |
| C.亚硝酸盐的含量属于食品安全检测指标 |
| D.碳酸氢钠在食品工业中常用作膨松剂 |
您最近一年使用:0次
7 . 学习小组在实验字研究SO2并进行相关性质的探究。葡萄酒中SO2最大使用量0.25g∙L-1,取300.00mL葡萄酒,通过适当的方法使所含SO2全部逸出并用H2O2将其全部氧化为H2SO4,然后用0.0900mol∙L-1NaOH标准溶液进行滴定。
(1)如图所示,仪器A的名称_______ 。
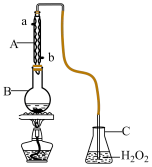
(2)写出 SO2气体与H2O2溶液反应的化学方程式_______ 。
(3)用标准液滴定前排气泡时,应选择图中的_______(填字母)。
(4)上述滴定实验中若滴定终点时溶液的pH=8.8,可选择_______ 为指示剂,选择该指示剂时如何判断反应到达滴定终点_______ 。
(5)滴定前读数时平视凹液面,滴定终点读数时俯视刻度线,则测量结果比实际值_______ (填“偏高”“偏低”或“无影响”)。
(6)滴定至终点时,消耗NaOH溶液20.00mL,则该葡萄酒中SO2的含量是否超标?_______ (填“是”或“否”)
(1)如图所示,仪器A的名称

(2)写出 SO2气体与H2O2溶液反应的化学方程式
(3)用标准液滴定前排气泡时,应选择图中的_______(填字母)。
A.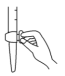 | B.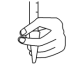 | C.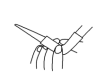 | D.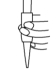 |
(5)滴定前读数时平视凹液面,滴定终点读数时俯视刻度线,则测量结果比实际值
(6)滴定至终点时,消耗NaOH溶液20.00mL,则该葡萄酒中SO2的含量是否超标?
您最近一年使用:0次
2022-09-30更新
|
108次组卷
|
2卷引用:广西壮族自治区南宁市广西民族高中2021-2022学年高二下学期段考化学试题
名校
解题方法
8 . (1)在AlCl3溶液中滴加过量的氨水,反应的化学方程式为__________________ 。
(2)碳酸氢钠与稀硫酸反应的离子方程式__________________ ;铜与浓硫酸共热反应的化学方程式__________________ 。
(3)现有0.284kg质量分数为10%的Na2SO4溶液,则溶液中Na2SO4的物质的量为______ ;配制250mL2.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液的体积_________ mL。
(4)同一主族元素性质具有一定的相似性和递变性;同一主族,从上到下:原子的电子层数逐渐____________ ,原子半径逐渐____________ ;失电子能力逐渐____________ ,金属性逐渐____________ ;得电子能力逐渐 ___________ ,非金属性逐渐____________ 。
(5)A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,C是金属元素;A、C元素原子的最外层都只有一个电子;B和D元素原子的最外层电子数相同,且B元素原子L层电子数是K层电子数的3倍;E元素原子最外层电子数比次外层电子数少1。回答下列问题:
写出E元素的元素符号:________ 画出B、C的原子结构示意图:B.________ C________ 画出D的离子结构示意图:________ 。
(2)碳酸氢钠与稀硫酸反应的离子方程式
(3)现有0.284kg质量分数为10%的Na2SO4溶液,则溶液中Na2SO4的物质的量为
(4)同一主族元素性质具有一定的相似性和递变性;同一主族,从上到下:原子的电子层数逐渐
(5)A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,C是金属元素;A、C元素原子的最外层都只有一个电子;B和D元素原子的最外层电子数相同,且B元素原子L层电子数是K层电子数的3倍;E元素原子最外层电子数比次外层电子数少1。回答下列问题:
写出E元素的元素符号:
您最近一年使用:0次
解题方法
9 . 某化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。

(1)mg铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:
①常温下碳与浓硫酸不反应;
②__ 。
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式__ 。
(3)B中的现象是__ ,C的作用是__ 。
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。则铁碳合金中铁的质量分数为__ (写表达式)。
(5)甲同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因:__ 。
(6)本套装置在设计上存在缺陷,其中导致测得铁的质量分数偏低的是(答一条即可)__ 。

(1)mg铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:
①常温下碳与浓硫酸不反应;
②
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式
(3)B中的现象是
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。则铁碳合金中铁的质量分数为
(5)甲同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因:
(6)本套装置在设计上存在缺陷,其中导致测得铁的质量分数偏低的是(答一条即可)
您最近一年使用:0次
10 . 某化学兴趣小组欲在实验室制备二氧化硫,并探究相关物质的一些性质。根据要求完成下列各小题。
Ⅰ.验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)

(1)仪器A的名称为__________ ,铜与浓硫酸反应的化学方程式是________ 。
(2)实验步骤:连接仪器、______ 、加药品后、打开a、然后滴入浓硫酸,加热。
(3)装置E中足量酸性KMnO4溶液的作用是____ ,请写出装置E中发生反应的离子方程式________ 。
(4)能说明碳元素的非金属性比硅元素的非金属性强的实验现象是_______ 。
Ⅱ.某同学拟用以下方法测定空气中SO2含量(假设空气中无其它还原性气体)。

①你认为不可行的装置是______ (填序号“a”或“b"),理由是____ 。
②使用你所选用的装置测定SO2含量时,还需要测定的物理量是_____ 。
Ⅰ.验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)

(1)仪器A的名称为
(2)实验步骤:连接仪器、
(3)装置E中足量酸性KMnO4溶液的作用是
(4)能说明碳元素的非金属性比硅元素的非金属性强的实验现象是
Ⅱ.某同学拟用以下方法测定空气中SO2含量(假设空气中无其它还原性气体)。

①你认为不可行的装置是
②使用你所选用的装置测定SO2含量时,还需要测定的物理量是
您最近一年使用:0次
2020-07-30更新
|
221次组卷
|
2卷引用:广西河池市九校2020-2021学年高二下学期第二次联考化学试题



