名校
1 . 类推时要注意物质的相似性和特殊性,下列类推结论正确的是
| 选项 | 化学事实 | 类推结论 |
| A | 钠与水反应生成NaOH和 | 高温下铁与水蒸气反应也能生成碱和H2 |
| B | 溶解度: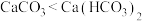 | 溶解度: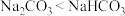 |
| C |  受热分解为 受热分解为 和 和 | Fe(OH)3也能受热分解生成相应价态的金属氧化物和H2O |
| D | Cu与 反应,生成 反应,生成 | Cu与S反应,生成CuS |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列反应的离子方程式正确的是
A.少量 通入 通入 中: 中: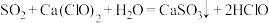 |
B.向二元弱酸 溶液中滴入足量烧碱溶液: 溶液中滴入足量烧碱溶液: |
C. 溶于HI溶液: 溶于HI溶液: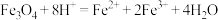 |
D.向含 的溶液通入标准状况下 的溶液通入标准状况下 : : |
您最近一年使用:0次
3 . 某兴趣小组对FeSO4的一些性质进行探究实验。回答下列问题:
(1)在试管中加入少量FeSO4样品,加水溶解,滴加KSCN溶液,溶液逐渐变_____ 色,说明样品已变质。同学甲认为若要使变质的FeSO4溶液复原,可以向溶液中加入过量的Fe粉,发生反应的离子方程式为______________ 。
(2)已知FeSO4的分解产物中含有SO2和SO3。将纯净FeSO4和有关试剂放入如图所示的装置,打开K1和K2,缓缓通入N2,加热,实验后反应管中残留固体为红棕色粉末。________________ 。
②装置C中盛放的溶液为________ ;装置D中盛放的溶液为________ (填标号)。
A.品红 B.NaOH C.BaCl2 D.浓H2SO4
③盛有NaOH溶液的装置的作用是_____________ 。
④实验时装置D中除有气泡冒出外,还可观察到的实验现象为_____________ 。
(1)在试管中加入少量FeSO4样品,加水溶解,滴加KSCN溶液,溶液逐渐变
(2)已知FeSO4的分解产物中含有SO2和SO3。将纯净FeSO4和有关试剂放入如图所示的装置,打开K1和K2,缓缓通入N2,加热,实验后反应管中残留固体为红棕色粉末。

②装置C中盛放的溶液为
A.品红 B.NaOH C.BaCl2 D.浓H2SO4
③盛有NaOH溶液的装置的作用是
④实验时装置D中除有气泡冒出外,还可观察到的实验现象为
您最近一年使用:0次
名校
4 . 某单质A经下图所示过程可转化为D,D为强酸或强碱,则单质A不可能为
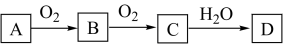
| A.N2 | B.Na | C.C | D.S |
您最近一年使用:0次
5 .  是硫元素中一种重要物质。在生产生活中有容重要用途。
是硫元素中一种重要物质。在生产生活中有容重要用途。
(1)某研究小组用如图装置进行 与
与 溶液反应的相关实验(夹持装置已略去)
溶液反应的相关实验(夹持装置已略去) 时C中观察到的现象为
时C中观察到的现象为__________________________ 。
②根据以上现象,该小组同学认为 与
与 溶液发生氧化还原反应。
溶液发生氧化还原反应。
a.写出 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:___________________________ 。
b.该小组同学向C试管反应后的溶液中加入硝酸酸化的 溶液,若出现白色沉淀,即可证明反应生成了
溶液,若出现白色沉淀,即可证明反应生成了 。该做法
。该做法_________ (填“合理”或“不合理”),理由是___________________________ 。
③为了验证 具有还原性,实验中可以代替
具有还原性,实验中可以代替 溶液的试剂有
溶液的试剂有______________ (填字母)。
A.浓硫酸 B.酸性 溶液 C.碘水 D.NaCl溶液
溶液 C.碘水 D.NaCl溶液
(2)某同学利用如图所示的装置研究 的性质:(熔点:
的性质:(熔点: 为
为 ,
, 为16.8℃,沸点:
为16.8℃,沸点: 为
为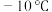 ,
, 为45℃)
为45℃) 催化氧化的反应,其化学方程式是
催化氧化的反应,其化学方程式是___________________________ 。
②甲同学按I、Ⅱ、Ⅲ、IV的顺序连接装置,装置Ⅲ中溶液逐渐褪色,生成 ,同时酸性增强,则该反应的离子方程式是(忽略
,同时酸性增强,则该反应的离子方程式是(忽略 的影响)
的影响)___________________________ 。
③乙同学按I、Ⅱ、IV顺序连接装置,若装置IV中有 溶液,反应后增重4.8g,则装置IV中发生反应的化学方程式是
溶液,反应后增重4.8g,则装置IV中发生反应的化学方程式是___________________________ 。
 是硫元素中一种重要物质。在生产生活中有容重要用途。
是硫元素中一种重要物质。在生产生活中有容重要用途。(1)某研究小组用如图装置进行
 与
与 溶液反应的相关实验(夹持装置已略去)
溶液反应的相关实验(夹持装置已略去) 
 时C中观察到的现象为
时C中观察到的现象为②根据以上现象,该小组同学认为
 与
与 溶液发生氧化还原反应。
溶液发生氧化还原反应。a.写出
 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:b.该小组同学向C试管反应后的溶液中加入硝酸酸化的
 溶液,若出现白色沉淀,即可证明反应生成了
溶液,若出现白色沉淀,即可证明反应生成了 。该做法
。该做法③为了验证
 具有还原性,实验中可以代替
具有还原性,实验中可以代替 溶液的试剂有
溶液的试剂有A.浓硫酸 B.酸性
 溶液 C.碘水 D.NaCl溶液
溶液 C.碘水 D.NaCl溶液(2)某同学利用如图所示的装置研究
 的性质:(熔点:
的性质:(熔点: 为
为 ,
, 为16.8℃,沸点:
为16.8℃,沸点: 为
为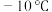 ,
, 为45℃)
为45℃)
 催化氧化的反应,其化学方程式是
催化氧化的反应,其化学方程式是②甲同学按I、Ⅱ、Ⅲ、IV的顺序连接装置,装置Ⅲ中溶液逐渐褪色,生成
 ,同时酸性增强,则该反应的离子方程式是(忽略
,同时酸性增强,则该反应的离子方程式是(忽略 的影响)
的影响)③乙同学按I、Ⅱ、IV顺序连接装置,若装置IV中有
 溶液,反应后增重4.8g,则装置IV中发生反应的化学方程式是
溶液,反应后增重4.8g,则装置IV中发生反应的化学方程式是
您最近一年使用:0次
2024-02-20更新
|
484次组卷
|
4卷引用:广西柳州铁一中学2023-2024学年高一上学期期末考试化学试卷
6 . 某学校兴趣小组在课余时间进行了以下两组化学实验。
实验一:利用下图所示装置来验证铜与浓硫酸的反应产物及产物的某些性质。

(1)请写出铜跟浓硫酸反应的化学方程式___________ 。
(2)装置B的作用是贮存多余的气体。当D处有明显的现象时,关闭弹簧夹K,移去酒精灯,但由于余热的作用,A处仍有气体产生,则B中应放置的液体是___________ (填字母编号)。
(3)反应完毕,该小组发现烧瓶中还有铜片剩余,根据所学知识,他们认为还有一定量的硫酸剩余。下列药品中能够用来证明反应结束后的烧瓶中仍有余酸的是___________ (填字母编号)。
A.银粉 B.BaCl2溶液 C.Na2CO3溶液
实验二:用下列装置进行乙醇催化氧化的实验。
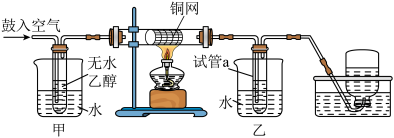
(4)实验过程中铜网出现红色和黑色交替的现象,在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明乙醇催化氧化反应是___________ 反应。
(5)甲和乙两个水浴的作用不相同。甲的作用是___________ ;乙的作用是冷凝,使乙醛液化。
实验一:利用下图所示装置来验证铜与浓硫酸的反应产物及产物的某些性质。

(1)请写出铜跟浓硫酸反应的化学方程式
(2)装置B的作用是贮存多余的气体。当D处有明显的现象时,关闭弹簧夹K,移去酒精灯,但由于余热的作用,A处仍有气体产生,则B中应放置的液体是___________ (填字母编号)。
| A.氯水 | B.NaOH溶液 | C.饱和NaHSO3溶液 | D.酸性KMnO4溶液 |
A.银粉 B.BaCl2溶液 C.Na2CO3溶液
实验二:用下列装置进行乙醇催化氧化的实验。

(4)实验过程中铜网出现红色和黑色交替的现象,在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明乙醇催化氧化反应是
(5)甲和乙两个水浴的作用不相同。甲的作用是
您最近一年使用:0次
2023-11-08更新
|
213次组卷
|
2卷引用:广西柳州铁一中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
7 . 由实验操作和现象,可得出相应正确结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向某溶液中加入少量氯化钡溶液 | 产生白色沉淀 | 溶液中一定含SO |
| B | 在试管中加入少量淀粉和稀硫酸,加热,待冷却后,再加入少量新制的Cu(OH)2,加热 | 未见砖红色沉淀 | 淀粉未发生水解 |
| C | 甲烷与氯气在光照下反应后的混合气体通入石蕊试液 | 试液变红 | 生成的一氯甲烷具有酸性 |
| D | 相同条件下,将同等大小的钠分别加入无水乙醇和水中 | 钠与水反应更剧烈 | 水中羟基的活性大于乙醇中羟基的活性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列实验探究方案不能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向 溶液滴加4滴 溶液滴加4滴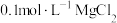 溶液,再滴加4滴 溶液,再滴加4滴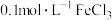 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 | 比较 和 和 的 的 |
| B | 向盛有 水溶液的试管中滴加几滴品红溶液,振荡,观察溶液颜色变化 水溶液的试管中滴加几滴品红溶液,振荡,观察溶液颜色变化 |  具有漂白性 具有漂白性 |
| C | 酸性 溶液中滴加乙醇至过量,观察溶液颜色变化 溶液中滴加乙醇至过量,观察溶液颜色变化 | 乙醇具有还原性 |
| D | 向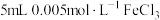 溶液中加入 溶液中加入 溶液,再滴加5滴 溶液,再滴加5滴 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 | 浓度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . (Ⅰ)非金属元素在生活、生产中扮演着非常重要的角色。请根据题意填空。
(1)木棍放在浓硫酸中变黑,体现了浓硫酸的_______ (填“脱水性”或“氧化性”)。
(2)已知玻璃中的成分有 ,实验室盛放碱溶液的试剂瓶应使用
,实验室盛放碱溶液的试剂瓶应使用_______ (填“玻璃塞”或“橡胶塞”)的试剂瓶。
(3) 可与水反应,请写出该反应的离子方程式:
可与水反应,请写出该反应的离子方程式:__________________ 。
(Ⅱ)化学与人类生活、生产密切相关。请根据题意填空。
(4)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应: 。在此反应中,氧化剂为
。在此反应中,氧化剂为_______________ (填化学式),当该反应转移3mol电子时,产生气体的体积为________________ L(标准状况下)。
(5)湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、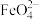 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:_______ 。
(1)木棍放在浓硫酸中变黑,体现了浓硫酸的
(2)已知玻璃中的成分有
 ,实验室盛放碱溶液的试剂瓶应使用
,实验室盛放碱溶液的试剂瓶应使用(3)
 可与水反应,请写出该反应的离子方程式:
可与水反应,请写出该反应的离子方程式:(Ⅱ)化学与人类生活、生产密切相关。请根据题意填空。
(4)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应:
 。在此反应中,氧化剂为
。在此反应中,氧化剂为(5)湿法制备高铁酸钾(
 )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、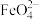 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
您最近一年使用:0次
2023-05-08更新
|
246次组卷
|
2卷引用:广西柳州地区民族高级中学2022-2023学年高一下学期期中考试化学试题
10 . 设 为阿伏加德罗常数值。下列叙述正确的是
为阿伏加德罗常数值。下列叙述正确的是
 为阿伏加德罗常数值。下列叙述正确的是
为阿伏加德罗常数值。下列叙述正确的是A.1mol硫与足量铁反应,转移 个电子 个电子 |
B.1mol炭和足量热浓硫酸反应可生成 个CO分子 个CO分子 |
C.标准状况下,2.24L 和 和 的混合气体中分子数为 的混合气体中分子数为 |
D.标准状况下,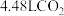 与 与 充分反应转移的电子数目为 充分反应转移的电子数目为 |
您最近一年使用:0次



