1 . 下列说法正确的是
A.某溶液中加入氢氧化钠溶液加热,产生使湿润红色石蕊试纸变蓝气体,该溶液中含有 |
| B.除去混在碳酸钠溶液中的少量碳酸氢钠用加热的方法 |
C.加入 溶液产生白色沉淀,溶液中一定含有 溶液产生白色沉淀,溶液中一定含有 |
| D.某物质焰色反应呈黄色,该物质一定是钠单质 |
您最近一年使用:0次
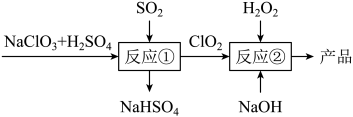
2 . 亚氯酸钠( )是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
 )是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
A. 中氯元素的化合价是+3价 中氯元素的化合价是+3价 |
B.反应②中 被还原 被还原 |
C.若生成 ,理论上消耗 ,理论上消耗 |
D.反应①,参加反应的 和 和 的物质的量之比为 的物质的量之比为 |
您最近一年使用:0次
3 . 下列关于物质检验的说法不正确的是
A.加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,一定含有 |
B.NaCl与 燃烧时火焰颜色相同 燃烧时火焰颜色相同 |
C.待检液加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液中一定含有 |
D.待检液中加入氯化钡溶液有白色沉淀生成,再加入盐酸,沉淀消失且产生无色无味的气体,则待检液中一定含有 |
您最近一年使用:0次
4 . 下列变化不能通过一步化学反应实现的是
A. | B.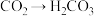 |
C. | D. |
您最近一年使用:0次
解题方法
5 . 人体吸入 会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:
会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:
(1) 具有氧化性,
具有氧化性, 与
与 反应会生成淡黄色沉淀,写出反应的化学方程式:
反应会生成淡黄色沉淀,写出反应的化学方程式:_______ 。
(2) 可以使品红溶液褪色,说明二氧化硫具有
可以使品红溶液褪色,说明二氧化硫具有_______ 性。
(3)石灰石——石膏法。该工艺原理利用石灰石加水制成的浆液( )作为吸收剂,吸收二氧化硫,并生成
)作为吸收剂,吸收二氧化硫,并生成 。再向其中通入烟气氧化生成
。再向其中通入烟气氧化生成 ,写出该工艺中生成
,写出该工艺中生成 的化学方程式:
的化学方程式:_______ 。
(4)近年来,有人提出了一种利用电解饱和氯化钠溶液循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:
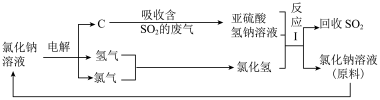
①此种方法中,可以循环利用的物质是_______ (填化学式)。
②写出电解饱和氯化钠溶液的化学方程式:_______ 。
③写出反应I的离子方程式:_______ 。
 会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:
会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:(1)
 具有氧化性,
具有氧化性, 与
与 反应会生成淡黄色沉淀,写出反应的化学方程式:
反应会生成淡黄色沉淀,写出反应的化学方程式:(2)
 可以使品红溶液褪色,说明二氧化硫具有
可以使品红溶液褪色,说明二氧化硫具有(3)石灰石——石膏法。该工艺原理利用石灰石加水制成的浆液(
 )作为吸收剂,吸收二氧化硫,并生成
)作为吸收剂,吸收二氧化硫,并生成 。再向其中通入烟气氧化生成
。再向其中通入烟气氧化生成 ,写出该工艺中生成
,写出该工艺中生成 的化学方程式:
的化学方程式:(4)近年来,有人提出了一种利用电解饱和氯化钠溶液循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:

①此种方法中,可以循环利用的物质是
②写出电解饱和氯化钠溶液的化学方程式:
③写出反应I的离子方程式:
您最近一年使用:0次
名校
6 . 如图是以硫铁矿为原料制硫酸的工业制法,下列说法不正确的是
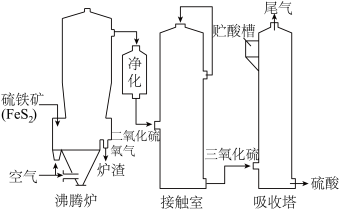

| A.硫铁矿煅烧前要粉碎,是为了增大与空气的接触面积,使燃烧更快、更充分 |
B.通入空气后沸腾炉中发生反应的化学方程式: |
C.从沸腾炉中出来的气体有 和 和 |
D.吸收塔中 可以用水吸收,以便使 可以用水吸收,以便使 吸收更充分 吸收更充分 |
您最近一年使用:0次
2023-04-22更新
|
238次组卷
|
2卷引用:广西壮族自治区河池市2022-2023学年高一上学期期末考试化学试题
解题方法
7 . 我国炼丹术史料中记载有:“丹砂烧之成水银,积变又还成丹砂。”下列有关硫的说法中错误的是
| A.硫单质通常是黄色或淡黄色的固体 | B.硫在空气中燃烧时生成三氧化硫 |
C.硫难溶于水,易溶于 | D.“丹砂烧之成水银”中发生了氧化还原反应 |
您最近一年使用:0次
8 . 用如图所示装置进行 与
与 反应的实验。实验过程中,观察到
反应的实验。实验过程中,观察到 中淡黄色粉末逐渐变为白色,用带火星的木条靠近
中淡黄色粉末逐渐变为白色,用带火星的木条靠近 中导气管口,木条复燃。
中导气管口,木条复燃。

(1)100mL18mol/L浓硫酸与足量的铜反应,产生的SO2的物质的量_______ (填写“大于”、“小于”、“等于”)0.9mol,理由是_______ 。
(2)B中的试剂为_______ ,其主要作用是干燥SO2。
(3)D中试剂的作用是防止过氧化钠吸收空气中的二氧化碳和水蒸气,同时还有一个作用是_______ 。
(4)为检验C中是否有Na2SO4生成,设计如下方案:取少量C中反应后的白色固体溶解于水,加入BaCl2溶液,产生白色沉淀,再加入足量的稀HNO3,仍有白色沉淀不溶解,证明有Na2SO4生成。
该方案是否合理?_______ (填“合理”或“不合理”)。请简要说明理由:_______ 。
(5)进一步实验证明C中反应后的固体中既有Na2SO3又有Na2SO4。试剂有:氯化钡溶液、稀盐酸、稀硫酸。你的操作方法是_______ 。
 与
与 反应的实验。实验过程中,观察到
反应的实验。实验过程中,观察到 中淡黄色粉末逐渐变为白色,用带火星的木条靠近
中淡黄色粉末逐渐变为白色,用带火星的木条靠近 中导气管口,木条复燃。
中导气管口,木条复燃。
(1)100mL18mol/L浓硫酸与足量的铜反应,产生的SO2的物质的量
(2)B中的试剂为
(3)D中试剂的作用是防止过氧化钠吸收空气中的二氧化碳和水蒸气,同时还有一个作用是
(4)为检验C中是否有Na2SO4生成,设计如下方案:取少量C中反应后的白色固体溶解于水,加入BaCl2溶液,产生白色沉淀,再加入足量的稀HNO3,仍有白色沉淀不溶解,证明有Na2SO4生成。
该方案是否合理?
(5)进一步实验证明C中反应后的固体中既有Na2SO3又有Na2SO4。试剂有:氯化钡溶液、稀盐酸、稀硫酸。你的操作方法是
您最近一年使用:0次
9 . 中药常采用硫磺熏蒸法以达到防霉防虫等目的。我国规定党参等中药SO2残留量不得超过400mg·kg-1。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:①SO2残留量是指残留硫的总量,以SO2计;②中药中残留的SO2已大部分转化为SO 。
。
(1)将200g所售党参研碎,用500mL0.01mol·L-1NaOH溶液充分浸泡,得无色浸泡液X,将X分成两等份。
①配制500mL0.01mol·L-1NaOH溶液需要的仪器有托盘天平、药匙、烧杯、量筒、玻璃棒、试剂瓶、____ 。
②用NaOH溶液浸泡的目的是____ (用离子方程式表示)。
(2)甲同学取一份X溶液采用如图所示方案测定党参中SO2残留量:

①加入H2O2的目的是____ 。
②判断BaCl2溶液已过量的方法为____ ;判断沉淀是否洗净所选用的试剂为____ 。
③党参中SO2残留量的表达式为____ mg·kg-1(用含m的式子表示)。
(3)蒸馏碘滴定法可测量中药材中二氧化硫是否超标(亚硫盐酸折算成二氧化硫)。原理是利用如图装置将亚硫酸盐转化为SO2,然后通过碘标准溶液滴定吸收液。
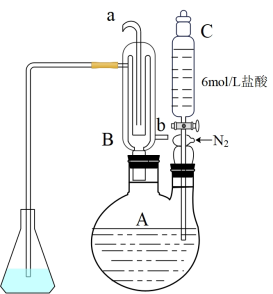
实验步骤如下:
SO2含量的测定
烧瓶A中加中药粉10g,加蒸馏水300mL;锥形瓶中加蒸馏水125mL和淀粉试液1mL作为吸收液;打开冷凝水,通氮气,滴入盐酸10mL;加热烧瓶A并保持微沸约3min后,用0.01000mol/L碘标准溶液一边吸收一边滴定,至终点时消耗碘标准溶液V1mL;
①滴入盐酸前先通氮气一段时间作用是____ 。
②滴定时锥形瓶中反应的离子方程式为____ ,滴定终点的现象是____ 。
 。
。(1)将200g所售党参研碎,用500mL0.01mol·L-1NaOH溶液充分浸泡,得无色浸泡液X,将X分成两等份。
①配制500mL0.01mol·L-1NaOH溶液需要的仪器有托盘天平、药匙、烧杯、量筒、玻璃棒、试剂瓶、
②用NaOH溶液浸泡的目的是
(2)甲同学取一份X溶液采用如图所示方案测定党参中SO2残留量:

①加入H2O2的目的是
②判断BaCl2溶液已过量的方法为
③党参中SO2残留量的表达式为
(3)蒸馏碘滴定法可测量中药材中二氧化硫是否超标(亚硫盐酸折算成二氧化硫)。原理是利用如图装置将亚硫酸盐转化为SO2,然后通过碘标准溶液滴定吸收液。

实验步骤如下:
SO2含量的测定
烧瓶A中加中药粉10g,加蒸馏水300mL;锥形瓶中加蒸馏水125mL和淀粉试液1mL作为吸收液;打开冷凝水,通氮气,滴入盐酸10mL;加热烧瓶A并保持微沸约3min后,用0.01000mol/L碘标准溶液一边吸收一边滴定,至终点时消耗碘标准溶液V1mL;
①滴入盐酸前先通氮气一段时间作用是
②滴定时锥形瓶中反应的离子方程式为
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式的书写及评价均合理的是
| 选项 | 离子方程式 | 评价 |
| A | 将1molCl2通入含1 mol FeI2,溶液中:2Fe2++2I-+2Cl2=2Fe3++4C1-+I2 | 正确; Cl2过量,可将Fe2+、I-均氧化 |
| B | 1mol·L-1的NaA1O2溶液和2.5 mol·L-1的HCl溶液等体积均匀混合;2AlO +5H+ =Al3++Al(OH)3↓+H2O +5H+ =Al3++Al(OH)3↓+H2O | 正确; AlO 与Al(OH)3消耗的H+的物质的量之比为2:3 与Al(OH)3消耗的H+的物质的量之比为2:3 |
| C | 过量SO2通入NaClO溶液中:SO2+H2O+ClO-=HClO+HSO | 正确; 说明酸性:H2SO3强于HClO |
| D | Ca(OH)2溶液与过量NaHCO3溶液反应:HCO +Ca2+ +OH- =CaCO3↓+H2O +Ca2+ +OH- =CaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-03更新
|
325次组卷
|
3卷引用:广西河池市高级中学2021-2022学年高三上学期第二次月考化学试题



