名校
解题方法
1 . 下列反应的离子方程式书写正确的是
A.将少量的Ca(HCO3)2溶液加入NaOH溶液: |
B.硝酸铁溶液中加过量氨水: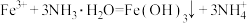 |
C.将CO2通入足量偏铝酸钠溶液中: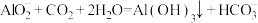 |
D.将少量SO2通入Ca(ClO)2溶液中: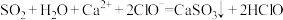 |
您最近一年使用:0次
2 . 下列叙叙述述正确的是
| A.加热氯化铵固体可制取氨气 |
| B.SO2能使KMnO4溶液褪色,是因为SO2具有漂白性 |
| C.SiO2既能和氢氧化钠溶液反应也能和氢氟酸反应,所以是两性氧化物 |
| D.钠粒用铝箔包住,在铝箔上刺些小孔,然后投入水中,放出氢气的量比直接将钠粒投入水中放出的氢气多 |
您最近一年使用:0次
名校
3 . 某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系________ (填“属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为________ (填“酸”或“碱”)性,表示该试样酸碱性的c(H+)或c(OH-)=________ mol·L-1。
(3)煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。______  +
+______ NO+______ =______ Cl-+______  +
+______
(4)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。写出焦炭与水蒸气反应的化学方程式:__________________ 。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是______ (填字母)。
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(5)汽车尾气中NOx和CO的生成及转化。
①汽车启动后,汽缸温度越高,单位时间内NO排放量越大,写出汽缸中生成NO的化学方程式:_________________________________________________________________ 。
②汽车燃油不完全燃烧时产生CO,目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为__________________________________________________ 。
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断待测试样为
(3)煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。
 +
+ +
+(4)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。写出焦炭与水蒸气反应的化学方程式:
②洗涤含SO2的烟气。以下物质可作洗涤剂的是
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(5)汽车尾气中NOx和CO的生成及转化。
①汽车启动后,汽缸温度越高,单位时间内NO排放量越大,写出汽缸中生成NO的化学方程式:
②汽车燃油不完全燃烧时产生CO,目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为
您最近一年使用:0次
2020-08-14更新
|
129次组卷
|
10卷引用:广西壮族自治区崇左市大新县大新中学2019-2020学年高一上学期期末考试化学试题
广西壮族自治区崇左市大新县大新中学2019-2020学年高一上学期期末考试化学试题天津市耀华中学2017-2018学年高一上学期期末考试化学试题鲁科版必修一2019—2020学年高一上学期期末考试模拟试题贵州省施秉县一中2019-2020学年高一上学期期末考试化学试题广西来宾市忻城县高级中学2019-2020学年高一上学期期末考试化学试题(已下线)4.3 防治二氧化硫对环境的污染练习(1)——《高中新教材同步备课》(苏教版 必修第一册)鲁科版(2019)高一必修第一册第3章 物质的性质与转化 总结检测黑龙江省齐齐哈尔三立高级中学2022届高三上学期开学考试化学试题山东省威海乳山市第一中学2022-2023学年高一上学期12月月考化学试题微项目 论证重污染天气“汽车限行”的合理性
名校
解题方法
4 . SO2溶于水后,与水反应生成H2SO3,下列对于H2SO3的性质预测正确的是( )
| A.有氧化性,无还原性,无酸性 |
| B.有氧化性,有还原性,有酸性 |
| C.有还原性,无氧化性,无酸性 |
| D.有还原性,无氧化性,有酸性 |
您最近一年使用:0次
2020-03-12更新
|
191次组卷
|
3卷引用:广西壮族自治区崇左市扶绥县第二中学2019-2020学年高一上学期期末考试化学试题
名校
解题方法
5 . “探险队员”——硫酸,不小心走进了有许多“吃人的野兽”如图所示(即能与硫酸发生化学反应的物质)的小山,逃生线路有多种,但有一种线路是完全行不通,处处为陷阱,即为入口→③→⑤→⑦→⑨→出口,则该线路涉及的物质为( )


| A.Na2CO3、Fe(OH)3、Zn、Fe2O3 | B.SO3、Cu、BaCl2、HCl |
| C.Zn、Fe(OH)3、KNO3、CuO | D.SO3、Cu、NaCl、CuO |
您最近一年使用:0次
2020-03-12更新
|
384次组卷
|
14卷引用:广西壮族自治区崇左市宁明中学2019-2020学年高一上学期期末考试化学试题
广西壮族自治区崇左市宁明中学2019-2020学年高一上学期期末考试化学试题重庆市万州第三中学2020-2021学年高一上学期第一次月考化学试题山东省滨州市博兴县第三中学2020-2021学年高一上学期10月月考化学试题河北省邯郸市大名一中等六校2020-2021学年高一上学期期中考试化学试题安徽省肥东县第二中学2020-2021学年高一上学期第一次月考化学试题河北省石家庄市第二中学西校区2020-2021学年高一上学期10月月考化学试题重庆市清华中学校2021—2022学年高一上学期10月月考化学试题吉林省长春外国语学校2021-2022学年高一下学期期初考试化学试题河北省石家庄市第十五中学2022-2023学年高一上学期期中考试化学试题黑龙江省海林林业局第一中学2021-2022学年高一上学期第一次月考化学试题湖北省荆州市沙市第七中学2021-2022学年高一上学期9月调研考试化学试题广东省连州市连州中学2021-2022学年高一上学期期中考试化学试题湖南省长沙市长郡中学2023-2024学年高一上学期第一次月考化学试题广东省惠州市惠州一中2023-2024学年高一上学期第二次阶段性考试化学试卷
解题方法
6 . 某研究性学习小组利用如图所示装置探究二氧化硫的性质。已知该实验过程可产生足量的二氧化硫。(装置中固定仪器未画出)

(1)A中所装试剂为铜片和__ (填试剂名称),导管F的作用是__ 。
(2)D中的试剂为0.5mol·L-1BaCl2溶液,实验中无明显现象,若改为同浓度的Ba(NO3)2溶液,则出现白色沉淀,此沉淀的化学式为__ ,证明SO2具有__ 性。
(3)装置B用于验证SO2的漂白性,则其中所装溶液为__ (填字母)。
A.酸性高锰酸钾溶液 B.品红溶液
C.石蕊溶液 D.蓝色的碘-淀粉溶液
(4)实验时,B中溶液褪色,并有大量气泡冒出,但始终未见C中饱和澄清石灰水出现浑浊或沉淀。请推测可能的原因,并设计实验验证。
可能原因:__ 。
实验验证:__ 。
(5)E中Na2S溶液用于验证SO2的氧化性,可观察到的现象为__ 。
(6)指出上述装置中的不足之处:__ 。

(1)A中所装试剂为铜片和
(2)D中的试剂为0.5mol·L-1BaCl2溶液,实验中无明显现象,若改为同浓度的Ba(NO3)2溶液,则出现白色沉淀,此沉淀的化学式为
(3)装置B用于验证SO2的漂白性,则其中所装溶液为
A.酸性高锰酸钾溶液 B.品红溶液
C.石蕊溶液 D.蓝色的碘-淀粉溶液
(4)实验时,B中溶液褪色,并有大量气泡冒出,但始终未见C中饱和澄清石灰水出现浑浊或沉淀。请推测可能的原因,并设计实验验证。
可能原因:
实验验证:
(5)E中Na2S溶液用于验证SO2的氧化性,可观察到的现象为
(6)指出上述装置中的不足之处:
您最近一年使用:0次
解题方法
7 . 能证明硫酸为强酸的实验事实是 ( )
| A.能与酸碱指示剂作用 | B.能与磷酸钙反应生成磷酸 |
| C.能与金属锌反应生成氢气 | D.能与食盐固体共热产生气体氯化氢 |
您最近一年使用:0次
2020-02-27更新
|
132次组卷
|
3卷引用:广西壮族自治区崇左市扶绥县第二中学2019-2020学年高一上学期期末考试化学试题
广西壮族自治区崇左市扶绥县第二中学2019-2020学年高一上学期期末考试化学试题云南省曲靖市马龙区第二中学2019-2020学年 高一上学期期末考试化学试题(已下线)课时22 硫及其化合物-2022年高考化学一轮复习小题多维练(全国通用)
解题方法
8 . 硫代硫酸钠(Na2S2O3)可用作分析试剂及鞣革还原剂。它受热、遇酸易分解。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得。实验室模拟该工业过程的装置如图所示。

回答下列问题:
(1)a中试剂为__________ ,b中试剂为__________ ,c中试剂为____________________ 。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是______________ 。
(3)d中的试剂为__________________ 。
(4)实验中要控制SO2生成速率,可以采取的措施有________________ (写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是__________________ 。

回答下列问题:
(1)a中试剂为
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是
(3)d中的试剂为
(4)实验中要控制SO2生成速率,可以采取的措施有
(5)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是
您最近一年使用:0次
2020-02-23更新
|
253次组卷
|
2卷引用:广西壮族自治区崇左市大新县大新中学2019-2020学年高一上学期期末考试化学试题
解题方法
9 . 下列关于硫的说法不正确的是( )
| A.单质硫既有氧化性,又有还原性 | B.硫在空气中的燃烧产物是二氧化硫 |
| C.铜与硫反应生成黑色的硫化铜 | D.硫与氢气反应的氧化剂是硫 |
您最近一年使用:0次
2020-02-18更新
|
159次组卷
|
3卷引用:广西壮族自治区崇左市天等县民族高中2019-2020学年高一上学期期末考试化学试题
解题方法
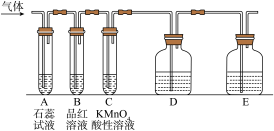
10 . 某课外小组设计了下图所示的实验装置(图中固定装置已略去),进行SO2性质的研究。
(1)从物质分类的角度,SO2属于____ (填“酸性”或“碱性”)氧化物。
①图中D装置可用来验证SO2具有该性质,其中所加入的试剂是________________ 。
②当向该装置通入SO2时,A中实验现象为_________ ,用化学用语解释其原因___________ 。
(2)从元素化合价的角度分析,SO2具有___ 性。
①当向该装置通入SO2一段时间后,可观察C中实验现象为___ ,说明SO2具有_____ 性。
②如验证SO2还具有另一方面的性质,可选择的药品是___ ,实验现象__________ 。
A.过氧化氢 B.浓硫酸C.氯水 D.硫化钠溶液
(3)B中的品红溶液现象是___________ ,证明SO2具有_________ 性。
(4)多余的SO2一般用氢氧化钠溶液吸收,反应的离子方程式_________________ 。
(1)从物质分类的角度,SO2属于
①图中D装置可用来验证SO2具有该性质,其中所加入的试剂是
②当向该装置通入SO2时,A中实验现象为
(2)从元素化合价的角度分析,SO2具有
①当向该装置通入SO2一段时间后,可观察C中实验现象为
②如验证SO2还具有另一方面的性质,可选择的药品是
A.过氧化氢 B.浓硫酸C.氯水 D.硫化钠溶液
(3)B中的品红溶液现象是
(4)多余的SO2一般用氢氧化钠溶液吸收,反应的离子方程式
您最近一年使用:0次
2020-01-17更新
|
134次组卷
|
3卷引用:广西壮族自治区崇左市大新县大新中学2019-2020学年高一上学期期末考试化学试题



