名校
1 . 能正确表示下列反应的离子方程式的是
A.四氧化三铁溶于氢碘酸中: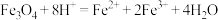 |
B.将过量的 通入 通入 溶液中: 溶液中: |
C.向酸性高锰酸钾溶液中通入 : : |
D.将少量澄清石灰水滴加到碳酸氢钠溶液中: |
您最近一年使用:0次
2 . “科技创造价值,创新驱动发展”,化学与生活、社会密切相关。下列说法错误的是
A.葡萄酒中加入适量 以起到杀菌、抗氧化的作用 以起到杀菌、抗氧化的作用 |
| B.我国成功研制吨级氢液化系统,该系统重新进行液氢汽化时断裂了化学键 |
| C.高纯硅广泛应用于太阳能电池和计算机芯片 |
| D.生产宇航服所用的碳化硅陶瓷和碳纤维材料都是新型无机非金属材料 |
您最近一年使用:0次
3 . 某学校兴趣小组在课余时间进行了以下两组化学实验。
实验一:利用下图所示装置来验证铜与浓硫酸的反应产物及产物的某些性质。

(1)请写出铜跟浓硫酸反应的化学方程式___________ 。
(2)装置B的作用是贮存多余的气体。当D处有明显的现象时,关闭弹簧夹K,移去酒精灯,但由于余热的作用,A处仍有气体产生,则B中应放置的液体是___________ (填字母编号)。
(3)反应完毕,该小组发现烧瓶中还有铜片剩余,根据所学知识,他们认为还有一定量的硫酸剩余。下列药品中能够用来证明反应结束后的烧瓶中仍有余酸的是___________ (填字母编号)。
A.银粉 B.BaCl2溶液 C.Na2CO3溶液
实验二:用下列装置进行乙醇催化氧化的实验。
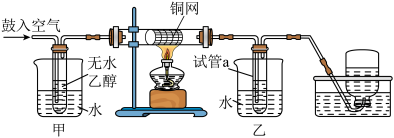
(4)实验过程中铜网出现红色和黑色交替的现象,在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明乙醇催化氧化反应是___________ 反应。
(5)甲和乙两个水浴的作用不相同。甲的作用是___________ ;乙的作用是冷凝,使乙醛液化。
实验一:利用下图所示装置来验证铜与浓硫酸的反应产物及产物的某些性质。

(1)请写出铜跟浓硫酸反应的化学方程式
(2)装置B的作用是贮存多余的气体。当D处有明显的现象时,关闭弹簧夹K,移去酒精灯,但由于余热的作用,A处仍有气体产生,则B中应放置的液体是___________ (填字母编号)。
| A.氯水 | B.NaOH溶液 | C.饱和NaHSO3溶液 | D.酸性KMnO4溶液 |
A.银粉 B.BaCl2溶液 C.Na2CO3溶液
实验二:用下列装置进行乙醇催化氧化的实验。

(4)实验过程中铜网出现红色和黑色交替的现象,在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明乙醇催化氧化反应是
(5)甲和乙两个水浴的作用不相同。甲的作用是
您最近一年使用:0次
2023-11-08更新
|
213次组卷
|
2卷引用:广西柳州铁一中学2023-2024学年高二上学期开学考试化学试题
4 . 以焙烧黄铁矿(主要成分为FeS2杂质为SiO2等)产生的红渣为原料制备颜料——铵铁蓝Fe(NH4)Fe(CN)6.工艺流程如图:

回答下列问题:
(1)红渣的主要成分为___________ (填化学式);滤渣①的主要成分为___________ (填化学式)。
(2)黄铁矿研细的目的是___________ 。
(3)还原工序中,不生成S单质的反应的化学方程式为___________ 。
(4)工序①的操作名称为___________ ,所得母液循环使用。
(5)在“洗涤干燥”中检验产品是否洗净的操作为___________ 。
(6)若用还原工序得到的滤液制备Fe2O3·xH2O和(NH4)2SO4,所需添加试剂分别为___________ 和___________ (填化学式,不引入杂质)。

回答下列问题:
(1)红渣的主要成分为
(2)黄铁矿研细的目的是
(3)还原工序中,不生成S单质的反应的化学方程式为
(4)工序①的操作名称为
(5)在“洗涤干燥”中检验产品是否洗净的操作为
(6)若用还原工序得到的滤液制备Fe2O3·xH2O和(NH4)2SO4,所需添加试剂分别为
您最近一年使用:0次
名校
解题方法
5 . 由实验操作和现象,可得出相应正确结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向某溶液中加入少量氯化钡溶液 | 产生白色沉淀 | 溶液中一定含SO |
| B | 在试管中加入少量淀粉和稀硫酸,加热,待冷却后,再加入少量新制的Cu(OH)2,加热 | 未见砖红色沉淀 | 淀粉未发生水解 |
| C | 甲烷与氯气在光照下反应后的混合气体通入石蕊试液 | 试液变红 | 生成的一氯甲烷具有酸性 |
| D | 相同条件下,将同等大小的钠分别加入无水乙醇和水中 | 钠与水反应更剧烈 | 水中羟基的活性大于乙醇中羟基的活性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
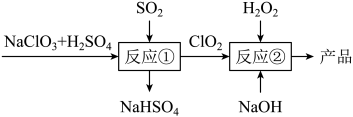
6 . 亚氯酸钠( )是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
 )是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
A. 中氯元素的化合价是+3价 中氯元素的化合价是+3价 |
B.反应②中 被还原 被还原 |
C.若生成 ,理论上消耗 ,理论上消耗 |
D.反应①,参加反应的 和 和 的物质的量之比为 的物质的量之比为 |
您最近一年使用:0次
名校
解题方法
7 . 下列实验装置或操作能达到实验目的的是
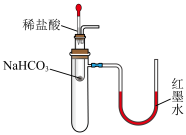 | 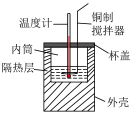 | 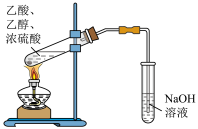 |  |
| A.探究稀盐酸与NaHCO3反应的热效应 | B.中和反应反应热的测定 | C.制备并收集乙酸乙酯 | D.制备SO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-02更新
|
311次组卷
|
3卷引用:广西玉林市博白县中学2023-2024学年高二上学期第一次月考化学试题
8 . 唐朝初年,瘟疫频发,人们把它归因于一种叫“年”的怪兽。一位叫李田的人就把硝石、硫磺和木炭装在竹筒里,点燃后驱赶怪兽。后来人们靠此驱散了山林瘴气,战胜了疫情。中国古代四大发明之一的“黑火药”是由“一硫二硝三木炭”混合而成。
(1)写出“黑火药”爆炸的化学反应方程式___________ 。
(2)“黑火药”爆炸时,空气中还弥漫着一层淡淡的刺鼻的 气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是
气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是___________ (用文字表述,任写一条合理途径)。
(3)某同学将足量的 通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。
通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。
(4)古代曾用硝土[含有 、少量NaCl等]和草木灰(含有
、少量NaCl等]和草木灰(含有 )作原料制取
)作原料制取 。某化学兴趣小组设计了如下实验流程:
。某化学兴趣小组设计了如下实验流程:

①“反应”过程中的离子反应方程式为___________ 。
②如图所示是硝酸钾和氯化钠的溶解度曲线。“一系列操作”包括将滤液___________ 、过滤洗涤、干燥等步骤。

(5)现代国防开矿等使用的烈性炸药,主要成分为硝化甘油 (
(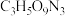 ),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。
),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。
①硝化甘油在人体内能缓慢分解出一种双原子明星分子,其相对分子量是30,少量的该分子在人体内会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛,该明星分子的化学式为___________ ;
②实验室制备硝化甘油的化学方程式为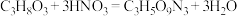 ,用足量浓硝酸、浓硫酸和
,用足量浓硝酸、浓硫酸和 mL
mL  g/cm
g/cm 甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为
甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为___________ 。

③反应得到16g硝化甘油,则产率为___________ (保留整数)。
(1)写出“黑火药”爆炸的化学反应方程式
(2)“黑火药”爆炸时,空气中还弥漫着一层淡淡的刺鼻的
 气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是
气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是(3)某同学将足量的
 通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。
通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。| A.硝酸钾溶液 | B.稀盐酸 | C.氨水 | D.硫化钠溶液 |
 、少量NaCl等]和草木灰(含有
、少量NaCl等]和草木灰(含有 )作原料制取
)作原料制取 。某化学兴趣小组设计了如下实验流程:
。某化学兴趣小组设计了如下实验流程:
①“反应”过程中的离子反应方程式为
②如图所示是硝酸钾和氯化钠的溶解度曲线。“一系列操作”包括将滤液

(5)现代国防开矿等使用的烈性炸药,主要成分为硝化甘油
 (
(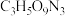 ),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。
),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。①硝化甘油在人体内能缓慢分解出一种双原子明星分子,其相对分子量是30,少量的该分子在人体内会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛,该明星分子的化学式为
②实验室制备硝化甘油的化学方程式为
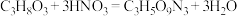 ,用足量浓硝酸、浓硫酸和
,用足量浓硝酸、浓硫酸和 mL
mL  g/cm
g/cm 甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为
甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为
③反应得到16g硝化甘油,则产率为
您最近一年使用:0次
名校
解题方法
9 . 硫酸盐(包含 、
、 )气溶胶是雾霾的主要成分之一,科研人员提出了雾霾微粒中硫酸盐生成的过程如图,下列说法不正确的是
)气溶胶是雾霾的主要成分之一,科研人员提出了雾霾微粒中硫酸盐生成的过程如图,下列说法不正确的是
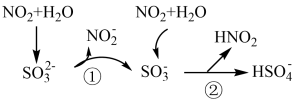
 、
、 )气溶胶是雾霾的主要成分之一,科研人员提出了雾霾微粒中硫酸盐生成的过程如图,下列说法不正确的是
)气溶胶是雾霾的主要成分之一,科研人员提出了雾霾微粒中硫酸盐生成的过程如图,下列说法不正确的是
| A.硫酸盐气溶胶呈酸性 |
B.第①步反应的离子方程式为: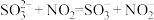 |
C. 是生成硫酸盐的催化剂, 是生成硫酸盐的催化剂, 是中间产物 是中间产物 |
D. 是大气污染物之一,可用NaOH溶液吸收处理 是大气污染物之一,可用NaOH溶液吸收处理 |
您最近一年使用:0次
2023-06-05更新
|
51次组卷
|
2卷引用:湘桂黔名校2022-2023学年高二下学期5月联考化学试题
10 . 1 L 1 mol/L Na2S溶液吸收SO2的量理论上最多可以吸收多少摩尔
| A.1.5 | B.2 | C.2.5 | D.3。 |
您最近一年使用:0次
2023-05-25更新
|
229次组卷
|
2卷引用:2023年第37届中国化学奥林匹克广西预选赛化学试题



